
| A.氧化铝的熔点很高,所以不可以用来冶炼铝 |
| B.氢氧化铝是一种胶状沉淀,有较大表面积,有吸附性,可用作净水剂 |
| C.实验室可以用氢氧化钠与氯化铝来制备氢氧化铝 |
| D.氢氧化铝既可与强酸反应又可与强碱反应,是两性氢氧化物 |
科目:高中化学 来源:不详 题型:单选题
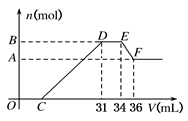
| A.无法求出曲线C点数值 |
| B.合金与硝酸反应时硝酸过量 |
| C.合金中铝的物质的量为0.008 mol |
| D.合金中金属的物质的量共为0.032 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na和K | B.Mg和Al | C.Cu和Al | D.Al和Fe |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
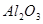 ,含有杂质
,含有杂质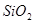 、
、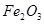 、
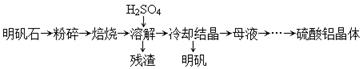
、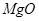 。工业上从铝土矿中提取铝可采用如下工艺流程:
。工业上从铝土矿中提取铝可采用如下工艺流程: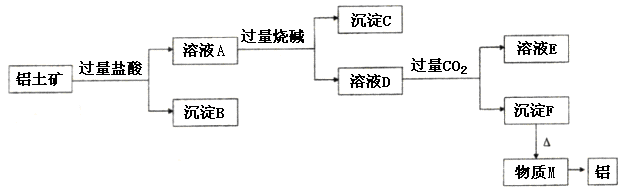
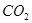 生成沉淀F的离子方程式为_______________________。
生成沉淀F的离子方程式为_______________________。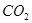 换成加入过量盐酸? (填 能 或 不能)
换成加入过量盐酸? (填 能 或 不能)查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 物质 | α-Al2O3 | γ-A12O3 |
| 性质 | 不溶于水和酸 | 不溶于水,溶于强酸或强碱,加热至1200℃可转化为α- Al2O3 |
| 温度/℃ 溶解度/g | 0 | 20 | 40 | 60 | 80 | 100 |
| Al2(SO4)3 | 31.2 | 36.4 | 46.1 | 59.2 | 73.0 | 89.0 |
| 明矾 | 3.0 | 5.9 | 11.7 | 25 | 71 | 154 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.9.6g | B.6.4g | C.3.2g | D.1.6g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
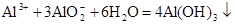 过程的是
过程的是| A.向铝盐溶液中不断滴加氢氧化钠溶液 |
| B.向偏铝酸盐溶液中不断加入盐酸 |
| C.向偏铝酸钠溶液中不断通入二氧化碳气体 |
| D.向氢氧化钠溶液中不断滴加铝盐溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com