
【题目】下列热化学方程式正确的是( )
A.甲烷的标准燃烧热为890.3 kJ?mol﹣1 , 则甲烷燃烧的热化学方程式可表示为:
CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=﹣890.3 kJ?mol﹣1
B.已知:H2(g)+ ![]() O2(g)=H2O(g)△H=﹣Q1kJ/mol,则2H2O(l)=2H2(g)+O2(g)△H=﹣2Q1kJ/mol
O2(g)=H2O(g)△H=﹣Q1kJ/mol,则2H2O(l)=2H2(g)+O2(g)△H=﹣2Q1kJ/mol
C.已知1 g液态肼和足量液态过氧化氢反应生成氮气和水蒸气时放出20.05 kJ的热量,其热化学方程式为
N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=﹣641.6 kJ?mol﹣1
D.已知:强酸和强碱的稀溶液中和热可表示为:H+(aq)+OH﹣(aq)?H2O(l)
△H=﹣57.3kJ/mol,则H2SO4(aq)+Ba(OH)2(aq)=BaSO4(aq)+2H2O(l)△H=﹣114.6kJ/mol
【答案】C
【解析】解:A.甲烷燃烧热是1mol甲烷完全燃烧生成稳定氧化物放出的热量,热化学方程式中水是气体,正确的热化学方程式为:甲烷燃烧的热化学方程式可表示为:
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890.3 kJmol﹣1 , 故A错误;
B.已知H2(g)+ ![]() O2(g)=H2O(g)△H=﹣Q1kJ/mol,若生成1mol液态水时放出的热量会大于Q1kJ,则2H2O(l)=2H2(g)+O2(g)△H>2Q1kJ/mol,故B错误;
O2(g)=H2O(g)△H=﹣Q1kJ/mol,若生成1mol液态水时放出的热量会大于Q1kJ,则2H2O(l)=2H2(g)+O2(g)△H>2Q1kJ/mol,故B错误;
C.1 g液态肼的物质的量为: ![]() =
= ![]() mol,则1mol液态肼完全反应放出的热量为:20.05 kJ×
mol,则1mol液态肼完全反应放出的热量为:20.05 kJ× ![]() =641.6kJ,该反应的化学方程式为:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=﹣641.6 kJmol﹣1 , 故C正确;
=641.6kJ,该反应的化学方程式为:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=﹣641.6 kJmol﹣1 , 故C正确;
D.强酸强碱的中和热为﹣57.3 kJ/mol,而Ba(OH)2(aq)+H2SO4(aq)=BaSO4(S)+2H2O(l)反应过程包括中和热和沉淀热,△H不是114.6 kJ,故D错误;
故选C.
【考点精析】认真审题,首先需要了解反应热和焓变(在化学反应中放出或吸收的热量,通常叫反应热).


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列实验能说明SO2具有漂白作用的是
A.SO2气体能使溴水褪色
B.SO2能使酸性高锰酸钾溶液褪色
C.SO2气体能使含NaOH的酚酞溶液褪色
D.SO2气体能使黄色的草帽辫变白色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在MgCl2和AlCl3的混合液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如图所示。
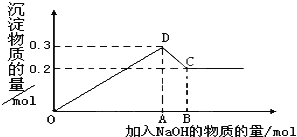
(1)写出下列线段内发生反应的方程式:
OD段__________________________________。
CD段__________________________________。
(2)图中C点表示加入________mol NaOH时。
(3)原溶液中来自MgCl2、AlCl3 的氯离子物质的量浓度之比为_____________。
(4)图中线段OB:OA=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸、硫酸和硝酸是中学阶段常见的“三大酸”.现就三大酸与金属反应的情况,回答下列问题:
(1)稀盐酸不与Cu反应,若在稀盐酸中加入H2O2(常见氧化剂,作氧化剂时还原产物为水)后,则可使铜顺利溶解.该反应的化学方程式为: .
(2)在一定体积的10molL﹣1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9mol.则浓硫酸的实际体积(填“大于”、“等于”或“小于”)180mL.若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为 .
(3)欲迅速除去铝壶底部的水垢,又不损坏铝壶,最好的方法是
A.浓盐酸
B.稀硝酸
C.冷的浓硝酸
D.冷的浓硫酸.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分类法是一种行之有效、简单易行的科学方法,人们在认识事物时可以采取多种分类方法.下列关于“K2SO4”的分类不正确的是( )
A.正盐
B.氧化物
C.钾盐
D.硫酸盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一恒温恒容密闭容器中充入1mol CO2和3mol H2 , 一定条件下发生反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H=﹣49.0kJ/mol
测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.下列说法正确的是( )
A.反应进行到3 min时,该反应达到平衡状态
B.从反应开始到平衡,CO2的转化率为25%
C.第3 min时,氢气的平均反应速率为1.5mol/(L?min)
D.该温度下,反应的平衡常数的值为 ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在强酸性溶液中能大量共存的无色透明离子组是( )
A. K+、Na+、NO3-、MnO4- B. Mg2+、Na+、Cl-、SO42-
C. K+、Na+、Cl-、Cu2+ D. Na+、Ba2+、OH-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用稀盐酸与稀NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: 
(1)该图中有两处未画出,它们是烧杯上方的泡沫塑料盖和 . 泡沫塑料的作用是 .
(2)若NaOH溶液用相同浓度和体积的下列溶液代替,则对中和热数值测定结果将如何影响(填“偏大”、“偏小”、“无影响”):KOH溶液;氨水(NH3H2O) .
(3)某研究小组将V1 mL 1.0mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).由题干及图形可知,V1:V2=时,酸碱恰好完全中和,此反应所用NaOH溶液的浓度应为mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用化学原理可以对工厂排放的废水、废渣等进行有效检测.某工厂对制铬工业污泥中Cr(Ⅲ)回收与再利用工艺如下(硫酸浸液中金属离子主要是Cr3+ , 其次是Fe3+ , Fe2+ , Al3+ , Ca2+ , Mg2+) 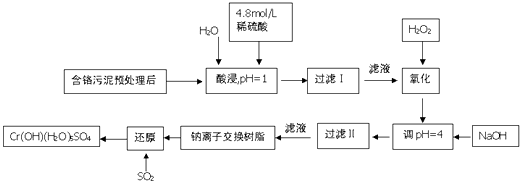
常温下部分阳离子的氢氧化物形成沉淀时溶液的pH见下表:
阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Ca2+ | Cr3+ |
开始沉淀时的pH | 1.9 | 7.0 | 9.6 | 4.2 | 9.7 | ﹣ |
沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8.0 | 11.7 | 9.0(>9.0溶解) |
(1)酸浸时,为了提高浸取率可采取的措施是(至少一条)
(2)调pH=4.0是为了除去(填Fe3+ , Al3+ , Ca2+ , Mg2+)
(3)钠离子交换树脂的原理为Mn++n NaR→MRn+nNa+ , 被交换的杂质离子是(填Fe3+ , Al3+ , Ca2+ , Mg2+)
(4)试配平下列氧化还原反应方程式:Na2Cr2O7+SO2+H2O=Cr(OH)(H2O)5SO4+Na2SO4 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com