
【题目】用稀盐酸与稀NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: 
(1)该图中有两处未画出,它们是烧杯上方的泡沫塑料盖和 . 泡沫塑料的作用是 .
(2)若NaOH溶液用相同浓度和体积的下列溶液代替,则对中和热数值测定结果将如何影响(填“偏大”、“偏小”、“无影响”):KOH溶液;氨水(NH3H2O) .
(3)某研究小组将V1 mL 1.0mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).由题干及图形可知,V1:V2=时,酸碱恰好完全中和,此反应所用NaOH溶液的浓度应为mol/L.
【答案】
(1)环形玻璃搅拌棒;减少热量的损失
(2)无影响;偏小
(3)3:2;1.5
【解析】解:(1)由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒;中和热测定实验成败的关键是保温工作,大小烧杯之间填满泡沫塑料的作用是减少实验过程中的热量损失;所以答案是:环形玻璃搅拌棒;减少热量的损失;(2)NaOH和KOH都是强碱,换成KOH对实验无影响,但一水合氨为弱电解质,电离吸热,导致测定结果偏小,所以答案是:无影响; 偏小;(3)由图象可知V1=30mL时温度最高,说明酸碱恰好完全反应,V1+V2=50mL,则V2=20mL,V1:V2=3:2,则有0.03L×1mol/L=0.02L×c,c=1.5mol/L.所以答案是:3:2; 1.5.


科目:高中化学 来源: 题型:
【题目】以下是氮循环的一部分: 
(1)通常状况下,NO2的颜色是;
(2)反应①的化学方程式是;
(3)NO2易溶于水,并和水发生化学反应.该反应中,氧化剂是;
(4)化合物A的化学式是;
(5)治理汽车尾气的一种方法是用催化剂使NO与CO发生反应:2NO+2CO═2CO2+N2 . 当生成2mol N2时,被还原的NO为mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式正确的是( )
A.甲烷的标准燃烧热为890.3 kJ?mol﹣1 , 则甲烷燃烧的热化学方程式可表示为:
CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=﹣890.3 kJ?mol﹣1
B.已知:H2(g)+ ![]() O2(g)=H2O(g)△H=﹣Q1kJ/mol,则2H2O(l)=2H2(g)+O2(g)△H=﹣2Q1kJ/mol
O2(g)=H2O(g)△H=﹣Q1kJ/mol,则2H2O(l)=2H2(g)+O2(g)△H=﹣2Q1kJ/mol
C.已知1 g液态肼和足量液态过氧化氢反应生成氮气和水蒸气时放出20.05 kJ的热量,其热化学方程式为
N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=﹣641.6 kJ?mol﹣1
D.已知:强酸和强碱的稀溶液中和热可表示为:H+(aq)+OH﹣(aq)?H2O(l)
△H=﹣57.3kJ/mol,则H2SO4(aq)+Ba(OH)2(aq)=BaSO4(aq)+2H2O(l)△H=﹣114.6kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国明代《本草纲目》冲收载药物1892种,其中“烧酒”条目下写道:“自元时始创其法,用浓酒和精人甑,蒸令气上……其清如水,球极浓烈,盖酒露也。”这里所用的“法”悬指
A. 萃取 B. 过滤 C. 蒸馏 D. 干馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从某含有 CuCl2、FeCl2、FeCl3的工业废液中回收铜并制备氯化铁晶体的流程如下:
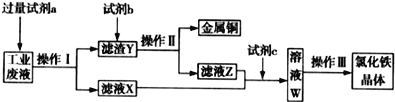
则下列说法正确的是
A. 试剂a是铁、试剂b是稀硫酸
B. 操作Ⅰ、操作Ⅱ、操作Ⅲ所用的仪器完全相同
C. 试剂c是氯气,相应的离子反应为2Fe2++ Cl2=2Cl-+2Fe3+
D. 用KSCN溶液可检验溶液W中是否有Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作中,所使用的仪器能够达到目的是( )
A.用5 mL量筒准确量取4.55 mL水
B.用托盘天平准确地称取6.82 g食盐
C.用广泛pH试纸测得某盐酸的pH为3.5
D.做KMnO4分解实验时用大试管作反应器
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子一定能大量共存的是( )
A. 在无色溶液中:Na+ Fe3+ Cl— SO42-
B. 在含大量Fe3+ 的溶液中:NH4+ K+ NO3- OH-
C. 在强碱溶液中:Na+ K+ NO3- CO32—
D. 滴加紫色石蕊试剂显红的溶液中:K+ Fe2+ Cl— CO32—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100℃时,将0.200mol的四氧化二氮气体充入2L真空的密闭容器中,每隔一定的时间对该容器内的物质进行分析,得到如表格:
| 0 | 2 | 4 | 6 | 8 | 10 |
c(N2O4) | 0.100 | c1 | 0.050 | c3 | a | b |
c(NO2) | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
试填空:
(1)该反应达到平衡时,四氧化二氮的转化率为%,表中c2c3、ab(填“>”、“<”或“=”).
(2)2min时四氧化二氮的浓度c1=mol/L,在0~2min时间段内,四氧化二氮的平均反应速率为mol/(Lmin).
(3)100℃时,该反应的平衡常数K=
(4)若在相同情况下最初向该容器充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的起始浓度是mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知酸性: ![]() >H2CO3>
>H2CO3> ![]() ,综合考虑反应物的转化率和原料成本等因素,将
,综合考虑反应物的转化率和原料成本等因素,将  转变为
转变为  的最佳方法是( )
的最佳方法是( )
A.与稀H2SO4共热后,加入足量的NaOH溶液
B.与稀H2SO4共热后,加入足量的NaHCO3溶液
C.与足量的NaOH溶液共热后,再通入足量CO2
D.与足量的NaOH溶液共热后,再加入适量H2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com