
| A�� | ����Ļ�ѧʽΪHNO3 | |
| B�� | ����C��ʱ��Һ�е������������Ҫ��Ba2+��NH4+ | |
| C�� | �ձ��иռ�����ʱ���۲첻���а�ɫ�������� | |
| D�� | ��A��E����ǿ��I��С����Ҫԭ�����������ܵ��κ��ѵ����ˮ |
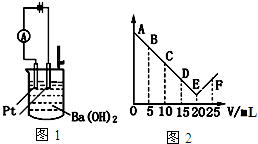
���� A��n��Ba��OH��2��=0.03L��0.1mol/L=0.003mol��n���ᣩ=0.1moL/L��0.02L=0.002mol������ж�ӦΪ��Ԫ�
B����C�㣨������������Ϊ10mL��ʱ���ձ��е�Ba��OH��2��û�б���ȫ�кͣ�
C���������������������ᷴӦ�������ᱵ������
D��Ba��OH��2����������������ˮ��Ba3��PO4��2���ѵ����ˮ������Ũ�Ƚ��ͣ�
��� �⣺A���ڵ�3����Ԫ���У����γɵ�������ǹ��ᣨH2SiO3��������ˮ�������ᣨH3PO4����ǿ�ᣩ�����ᣨH2SO4����Ԫǿ�ᣩ�������ᣨHClO4�������ᣨHClO3���������ᣨHClO�������ᣨHCl����n��Ba��OH��2��=0.03L��0.1mol/L=0.003mol��n���ᣩ=0.1moL/L��0.02L=0.002mol������ж�ӦΪ��Ԫ�ᣬ����ΪH3PO4����A����
B����C�㣨������������Ϊ10mL��ʱ���ձ��е�Ba��OH��2��û�б���ȫ�кͣ���Һ�е������������Ҫ��Ba2+����B����
C���������������������ᷴӦ�������ᱵ�����������ձ��иռ�����ʱ���ܹ۲쵽�а�ɫ�������ɣ���C����
D����A��E����ǿ��I��С����Ҫԭ���������кͷ�Ӧ�ķ���������������ˮ��Ba3��PO4��2���ѵ����ˮ��ʹ��Һ�������ƶ�������Ũ���½�����D��ȷ��
��ѡD��
���� ���⿼����ԭ������Ŀ����������ϵļ�����жϣ���Ŀ�Ѷ��еȣ�ע����ղμӷ�Ӧ�����ʵ����Ĺ�ϵ��Ϊ������Ĺؼ���


 ѧϰʵ����ϵ�д�
ѧϰʵ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ϸ�Ӧ | B�� | �ֽⷴӦ | ||
| C�� | ��Ӧ������л�ѧ������ | D�� | ԭ����ϳɷ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
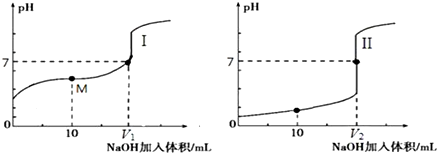
| ����1����2mL 0.005mol•L-1 AgNO3��Һ�м���2mL 0.005mol•L-1KSCN��Һ�����ã� | ���ְ�ɫ������ |
| ����2��ȡ1mL�ϲ���Һ���Թ��У��μ�1��2mol•L-1Fe��NO3��3��Һ�� | ��Һ��Ϊ��ɫ�� |
| ����3������2����Һ�У���������5�� 3mol•L-1AgNO3��Һ�� | ����a���ְ�ɫ��������Һ��ɫ��dz�� |
| ����4������1���µ���Һ�м���5�� 3mol•L-1KI��Һ�� | ���ֻ�ɫ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
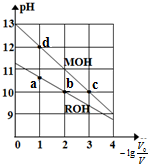 �����£��������ΪV0��Ũ�Ⱦ�Ϊ0.10mol•L-1��MOH��ROH��Һ�зֱ��ˮϡ�������ΪV����ҺpH��-lg$\frac{{v}_{0}}{v}$�ı仯��ͼ��ʾ������������ȷ���ǣ�������
�����£��������ΪV0��Ũ�Ⱦ�Ϊ0.10mol•L-1��MOH��ROH��Һ�зֱ��ˮϡ�������ΪV����ҺpH��-lg$\frac{{v}_{0}}{v}$�ı仯��ͼ��ʾ������������ȷ���ǣ�������| A�� | b��c�������Һ�У�c��R+����c��M+�� | |
| B�� | MOH�ĵ���̶ȣ�c��С��d�� | |
| C�� | ��Һ��ˮ�ĵ���̶ȣ�b��c��a��d | |
| D�� | ��-lg$\frac{{v}_{0}}{v}$=2ʱ��������Һͬʱ�����¶ȣ���$\frac{c��{R}^{+}��}{c��{M}^{+}��}$���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | N2 | H2 | NH3 |
| ��ʼ��mol�� | 2 | 7 | 0 |
| 10s��mol�� | 1.6 | ||
| ƽ�⣨mol�� | 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ijУ��չ�����о���ѧϰ���ӷϾɸɵ���л���̼����MnO2��NH4Cl��ZnCl2�����ʣ������������£��ش��й����⣺
ijУ��չ�����о���ѧϰ���ӷϾɸɵ���л���̼����MnO2��NH4Cl��ZnCl2�����ʣ������������£��ش��й����⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
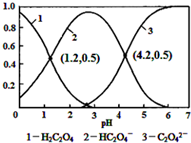
| A�� | pH=1.2��Һ�У�c��K+��+c��H+���Tc��OH-��+c��H2C2O4�� | |
| B�� | pH=2.7��Һ�У�$\frac{{c}^{2}��H{C}_{2}{O}_{4}^{-}��}{c��{H}_{2}{C}_{2}{O}_{4}��}$��c��C2O42-��=1000 | |
| C�� | ����ͬ���ʵ���KHC2O4��K2C2O4������ȫ����ˮ���û��Һ��pHΪ4.2 | |
| D�� | ��pH=1.2����Һ�м�KOH��Һ��pH������4.2�Ĺ�����ˮ�ĵ����һ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com