
【题目】甲、乙、丙均为化合物,其中甲为淡黄色的固体,乙常温下为无色无味液体,丙为常见的无色无味气体.它们有如下图的转化关系,已知D为黄绿色气体,按要求回答下列问题:
(1)甲物质为(填化学式).
(2)1mol乙和足量甲反应可生成mol B物质;1mol丙和足量甲反应可生成mol B物质.
(3)D能使湿润的有色布条褪色,其褪色原因是 .
(4)丙与溶液F反应的化学方程式为 .
【答案】
(1)Na2O2
(2)0.5;0.5
(3)溶于水生成HClO,HClO有强氧化性,能将有色物质氧化为无色物质,而使布条褪色
(4)CO2+NaClO+H2O=NaHCO3+HClO
【解析】解:甲、乙、丙均为化合物,甲为淡黄色的固体,乙常温下为无色无味液体,丙为常见的无色无味气体,甲能既能与乙反应也能与丙反应,可知甲为Na2O2 , 乙为H2O,丙为CO2 , 则A为NaOH,B为O2 , C为Na2CO3 . D为黄绿色气体,则D为Cl2 , D(氯气)与A(氢氧化钠)反应生成NaCl、NaClO,F能与丙(二氧化碳)反应C与I,则F为HClO、E为NaCl、I为NaHCO3 . G与C(碳酸钠)反应得到E(氯化钠)与丙(二氧化碳),则G为HCl.(1)由上述判断可知,甲物质为Na2O2 , 所以答案是:Na2O2;(2)乙与足量的甲发生反应:2Na2O2+2H2O=4NaOH+O2↑,1mol水反应可以生成0.5mol氧气,丙和足量甲发生反应:2Na2O2+2CO2=O2+2Na2CO3 , 1mol二氧化碳反应生成0.5mol氧气,所以答案是:0.5;0.5;(3)D(氯气)能使湿润的有色布条褪色,其褪色原因是:溶于水生成HClO,HClO有强氧化性,能将有色物质氧化为无色物质,而使布条褪色,所以答案是:溶于水生成HClO,HClO有强氧化性,能将有色物质氧化为无色物质,而使布条褪色;(4)丙与溶液F反应是二氧化碳与次氯酸钠反应生成碳酸氢钠与HClO,反应的化学方程式为:CO2+NaClO+H2O=NaHCO3+HClO,所以答案是:CO2+NaClO+H2O=NaHCO3+HClO.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】硫酸亚铁晶体(FeSO47H2O)在医药上作补血剂.某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质.实验步骤如下: 
请回答下列问题:
(1)步骤①滤液中滴加KSCN溶液后滤液变为红色,则该溶液中含有(填离子符号),检验滤液中还存在Fe2+的方法为(注明试剂、现象).
(2)步骤②加入过量H2O2的目的是 .
(3)步骤③中反应的离子方程式为 .
(4)步骤④中一系列处理的操作步骤包括:过滤、、灼烧、、称量.
(5)若实验无损耗,则每片补血剂含铁元素的质量为g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.按照系统命名法,烃分子 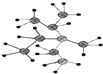 的名称为2,3﹣二甲基﹣3﹣乙基戊烷
的名称为2,3﹣二甲基﹣3﹣乙基戊烷
B.鸡蛋白、大豆蛋白等蛋白质可溶于水,在这些蛋白质溶液中加入(NH4)2SO4或Na2SO4的浓溶液,可使蛋白质的溶解度降低而析出
C.![]() 可发生加成反应、取代反应、氧化反应
可发生加成反应、取代反应、氧化反应
D.有机物 ![]() (俗称“一滴香”)的一种含苯环的同分异构体能发生银镜反应
(俗称“一滴香”)的一种含苯环的同分异构体能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从樟科植物枝叶提取的精油中含有甲、乙两种成分:![]()
(1)①甲和乙中含氧官能团的名称分别为和 .
②请写出甲的一种能同时满足下列3个条件的同分异构体的结构简式 .
a.苯环上有两个不同的取代基
b.能与Br2的CCl4溶液发生加成反应
c.遇FeCl3溶液显呈现紫色
(2)由甲转化为乙的过程为(已略去无关产物):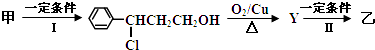
反应I的反应类型为 , Y的结构简式 .
(3)1mol乙最多可与 mol H2发生加成反应.
(4)写出乙与新制Cu(OH)2悬浊液反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下说法不正确的是( )
A.1mol乙醇可以与足量金属钠反应,生成0.5molH2 , 能证明乙醇分子有一个H原子与其余的H原子不同
B.下列反应可证明苯环受甲基的影响,甲苯易被酸性高锰酸钾氧化 ![]()
C.下列反应可证明由于羟基对苯环的影响,导致苯酚的取代比苯容易 
D.苯不能使溴的四氯化碳溶液褪色可以说明苯分子中没有与乙烯分子中类似的碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属非氧化还原反应的是
A. 3CuS+8HNO3==3Cu(NO3)2+2NO↑+3S↓+4H2O
B. 3Cl2+6KOH == 5KCl+KClO3+3H2O
C. 3H2O2+2KCrO2+2KOH==2K2CrO4+4H2O
D. 3CCl4+K2Cr2O7==2CrO2Cl2+3COCl2+2KCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在日常生活中,我们经常看到铁制品生锈、铝制品表面出现白斑等众多的金属腐蚀现象.可以通过下列装置所示实验进行探究.下列说法正确的是( ) 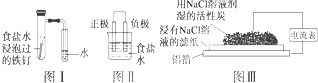
A.按图Ⅰ装置实验,为了更快更清晰地观察到液柱上升,可采用下列方法:用酒精灯加热具支试管
B.图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁
C.铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl﹣由活性炭区向铝箔表面区迁移,并发生电极反应:2Cl﹣﹣2e﹣═Cl2↑
D.图Ⅲ装置的总反应为4Al+3O2+6H2O═4Al(OH)3 , 生成的Al(OH)3进一步脱水形成白斑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t℃时,AgBr在水中的沉淀溶解平衡曲线如下图所示,下列说法不正确的是( )
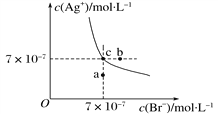
A. 在t℃时,AgBr的Ksp为4.9×10-13
B. 在AgBr饱和溶液中加入NaBr固体,可使溶液由c点变到b点
C. 图中a点对应的是AgBr的不饱和溶液
D. 在t℃时,往AgBr饱和溶液加入KI固体,会产生黄色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com