
【题目】2SO2(g)+O2(g)![]() 2SO3(g),反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ/mol。请回答下列问题:
2SO3(g),反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ/mol。请回答下列问题:

(1)E的大小对该反应的反应热________影响?(填“有或无”)。该反应通常用V2O5作催化剂,加V2O5会使图中B点______(填“升高或降低”);
(2)图中ΔH=__________kJ/mol;
(3)如果反应速率υ(SO2)为0.05 mol/(L·min),则υ(O2)=___________mol/(L·min);
(4)1 mol SO2(g)氧化为1 mol SO3(g)的反应热ΔH1___________1 mol SO2(g)氧化为1 mol SO3(l)的反应热ΔH2。(填“>、<或=”)
(5)已知单质硫的燃烧热为296 kJ/mol,计算由S(s)生成3 mol SO3(g)的ΔH=____________。
【答案】(1)无;降低(2)-198(3)0.025(4)>(5)-1185 kJ/mol
【解析】
试题分析:(1)E表示活化能,E的大小跟反应热大小无关;催化剂改变的反应物的活化能,中学阶段使用催化剂,降低活化分子的活化能,B点会降低。
(2)1molSO2被氧化成1molSO3时的反应热△H=-99kJ/mol,2molSO2完全参加反应时放出的热量是2×99kJ=198kJ,△H=-198kJ/mol,是放热反应。
(3)反应速率之比是化学计量数之比,则υ(O2)=0.025mol/(L·min);
(4)气态三氧化硫的能量高于液态三氧化硫的能力,因此1 mol SO2(g)氧化为1 mol SO3(g)的反应热ΔH1>1 mol SO2(g)氧化为1 mol SO3(l)的反应热ΔH2。
(5)单质硫的燃烧热为296kJmol-1,热化学方程式为:①S(s)+O2(g)=SO2(g)△H1=-296 kJmol-1,已知1mol SO2(g)氧化为1mol SO3的△H=-99kJmol-1,热化学方程式为②SO2(g)+1/2O2(g)![]() SO3(g)△H2=-99 KJmol-1 ;依据盖斯定律,②+①得到:③S(s)+3/2O2(g)=SO3(g)△H=(△H1+△H2)kJ/mol═-395kJmol-1,则③×3得到:3S(s)+9/2O2(g)=3SO3(g)△H=3(△H1+△H2)=-1185kJmol-1。
SO3(g)△H2=-99 KJmol-1 ;依据盖斯定律,②+①得到:③S(s)+3/2O2(g)=SO3(g)△H=(△H1+△H2)kJ/mol═-395kJmol-1,则③×3得到:3S(s)+9/2O2(g)=3SO3(g)△H=3(△H1+△H2)=-1185kJmol-1。


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】食盐中含有杂质CaCl2,一学生设计了如下实验方法分离NaCl和CaCl2:

填空和回答下列问题:
(1)写出生成B物质的化学方程式 。
(2)按此实验方案分离得到的NaCl,经分析含有杂质,是因为上述方案中某一步设计有毛病,这一步的正确设计方案应是 。
(3)若要测定该样品中NaCl和CaCl2的质量比,可称量干燥的B物质和另一物质的质量,这种物质是 (填字母或化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温恒容条件下,下列叙述中不是可逆反应2A(g)+3B(g)![]() 2C(g)达到平衡的标志的是
2C(g)达到平衡的标志的是
①C的生成速率与C的分解速率相等②单位时间生成amolA,同时消耗1.5molB;③各组分的浓度不再变化;④混合气体的密度不再变化;⑤混合气体的总压强不再变化;⑥混合气体的物质的量不再变化;⑦混合气体的平均摩尔质量不再变化;⑧A、B、C的分子数目比为2: 3: 2.
A. ⑤⑥⑧ B. ②⑤⑧ C. ①③④ D. ②④⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别取40mL的0.50mol/L盐酸与40mL0.55mol/L氢氧化钠溶液进行中和热的测定.下列说法错误的是( )

A.稍过量的氢氧化钠是确保盐酸完全反应
B.仪器A的名称是环形玻璃搅拌棒
C.在实验过程中,把温度计上的酸用水冲洗干净后再测量NaOH溶液的温度
D.用Ba(OH)2和硫酸代替盐酸和氢氧化钠溶液,结果也是正确的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现在许多汽车的保险杠是用塑料制造的,取代以前的钢制保险杠。下列不同的人士站在不同的角度对这种改变的看法,不正确的是( )。
A. 汽车制造商:车的外形变得美观,能够提高销量;易于加工,降低成本
B. 车主:车的重量减轻,油耗降低;汽车价格便宜
C. 意外被保险杠撞到的行人:具有缓冲作用,减轻伤害
D. 旁观者:用塑料作保险杠不安全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系![]() ,下列有关物质的推断不正确的是
,下列有关物质的推断不正确的是
A.若甲为焦炭,则丁可能是O2 B.若甲为Fe,则丁可能是盐酸
C.若甲为SO2,则丁可能是氨水 D.若甲为NaOH 溶液,则丁可能是H2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )。
A. 为了使婴儿对食品有更浓厚的兴趣,应在婴儿食品中加入大量的着色剂
B. 为了使火腿肠颜色更鲜红,可多加入一些亚硝酸钠
C. 蛋白质在人体内经消化后生成碳酸、硫酸、尿酸等,故属于酸性食物
D. 常用的抗酸药有氢氧化铜、氢氧化铝、柠檬酸钠、碳酸钙等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大。n、p、q是由这些元素组成的二元化合物,m是元素Y的单质,p是一种淡黄色粉末,q的水溶液可在玻璃器皿上蚀刻标记,0.01mol/Ls溶液的pH为12。上述物质的转化关系如图所示。下列说法正确的是
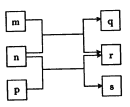
A. 离子半径:X>Y>Z
B. 氧化性:r>m
C. p和q中均含有离子键
D. 等体积等浓度的q溶液与s溶液反应后,溶液呈中性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com