
| 时间 酸 | 1 min | 2 min | 5 min | 15 min | 20 min |
| 实验一:3mol/L 盐酸 | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
| 实验二:1.5mol/L 硫酸 | 均无明显现象(无气泡) | ||||


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
| A、Br-、I-、Cl- |
| B、Br-、Cl-、I- |
| C、I-、Br-、Cl- |
| D、Cl-、I-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验顺序 | 实验内容 | 实验现象 |
| (1) | A+B | 无现象 |
| (2) | B+D | 有气体放出 |
| (3) | C+B | 有沉淀生成 |
| (4) | A+D | 有沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在常温常压下,28g CO气体中含有的分子数为NA |
| B、22.4L氢气中,含有氢原子数为3NA |
| C、56g铁在足量的氯气中燃烧,转移的电子数为2NA |
| D、1L 0.1mol?L-1盐酸中含有的HCl分子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
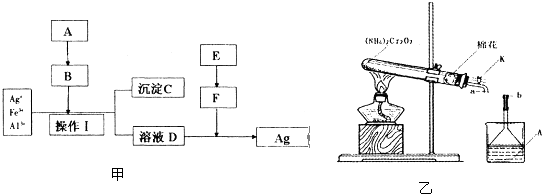
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、燃烧热是指可燃物燃烧时放出的热量 |
| B、凡是吸热反应,在常温下都是不能进行的,必须通过加热才能发生 |
| C、合成氨反应3H2(g)+N2(g)?2NH3(g)△H=-92.4kJ/mol,要使反应放出的热量为92.4kJ,加入的反应物H2和N2的物质的量一定大于3mol和1mol |
| D、用不同量的酸和碱发生中和反应,测得放出的热量数值不同,因此,不同反应的中和热数值不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Ba2+、Cl-?、SO42- |
| B、Na+、CO32-、C1-、K+ |
| C、Mg2+、Ag+、NO3-?、Cl-?? |
| D、H+、Cl-、Na+、CO32-?? |
查看答案和解析>>
科目:高中化学 来源: 题型:
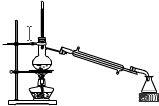 现有A、B两种有机物的液态混合物,如果A、B互溶,且相互不发生化学反应,在常压下,A的沸点为35℃,B的沸点为200℃.回答下列问题:
现有A、B两种有机物的液态混合物,如果A、B互溶,且相互不发生化学反应,在常压下,A的沸点为35℃,B的沸点为200℃.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用1mol的醋酸溶液和1.01mol的氢氧化钠溶液做中和热实验测得中和热的数值为57.3KJ/mol |
| B、通过实验得知在常温常压下,12g固体C和32g气体O2所具有的总能量一定大于44g气体CO2所具有的总能量 |
| C、室温下,用广泛pH试纸测得某溶液的pH为2.3 |
| D、用10mL的量筒量取8.05mL浓硫酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com