
【题目】根据以下3个热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H1=―Q1 kJ/mol
2H2S(g)+O2(g)=2S (s)+2H2O(l) △H2=―Q2 kJ/mol
2H2S(g)+O2(g)=2S (s)+2H2O(g) △H3=―Q3 kJ/mol
(Q1,Q2,Q3>0)下列判断正确的是
A. △H1>△H2>△H3 B. Q1>Q3>Q2
C. △H1<△H2<△H3 D. Q2>Q1>Q3
 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
【题目】向盛有NaBr溶液的试管中加入少量氯水,振荡,再加入适量CCl4,振荡,静置。下列判断正确的是
选项 | A | B | C | D |
上层 | 红棕色 | 黄绿色 | 无色 | 无色 |
下层 | 无色 | 无色 | 红棕色 | 黄绿色 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近期发现,H2S是继NO、CO之后的第三个生命体系气体信号分子。它具有参与调节神经信号传递、舒张血管减轻高血压的功能。回答下列问题:
(1)下图是通过热化学循环在较低温度下由水或硫化氢分别制备氢气的反应系统原理。

通过计算,可知系统(Ⅰ)和系统(Ⅱ)制氢的热化学方程式分别为___________________、__________________。制得等量H2所需能量较少的是_________。
(2)H2S与CO2在高温下发生反应:H2S(g)+CO2(g)![]() COS(g)+H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g)+H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
①H2S的平衡转化率α1=___________,反应平衡常数K=__________。
②在620 K重复实验,平衡后水的物质的量分数为0.03,H2S的转化率α2_________α1,该反应的ΔH________0。(填“>”“<”或“=”)
③向反应器中再分别充入下列气体,能使H2S转化率增大的是__________(填标号)。
A.H2S B.CO2 C.COS D.N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将铁、铜通过导线相连,置于稀硫酸中. 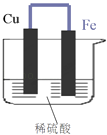
(1)铁片为极,其电极反应式 .
(2)铜片上的现象是 , 其发生的反应的类型是反应.(填“氧化”或“还原”)
(3)若导线中通过了0.6mol电子,Fe的质量理论上减少克.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁酸盐MFe2O4与H2在高温下反应生成新型纳米材料氧缺位铁酸盐(MFe2Ox,3<x<4,M=Mn、Zn、Ni,其均显+2价)。已知铁酸盐MFe2O4被H2高温还原时,发生反应的MFe2O4与H2的物质的量之比为2:1。则下列说法中不正确的是
A. MFe2Ox是还原产物
B. MFe2Ox 中的+2价铁和+3价铁的物质的量之比为1:3
C. x=3.5
D. 若反应中消耗H2(标准状况下)33.6L,则转移的电子为3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应O2(g)+2Cl2(g) ![]() 2Cl2O(g) △H>0,在三个恒温、恒容的密闭容器中分别充人lmolO2与2molCl2,测得平衡时O2的转化率如下表.下列说法正确的是( )
2Cl2O(g) △H>0,在三个恒温、恒容的密闭容器中分别充人lmolO2与2molCl2,测得平衡时O2的转化率如下表.下列说法正确的是( )
容器编号 | 温度(℃) | 容器体积/L | 平衡时O2转化率 | 平衡时压强(Pa) |
① | 200 | V1 | 50% | P1 |
② | 200 | V2 | 70% | P2 |
③ | 350 | V3 | 50% | P3 |
A. 反应速率:③>①>②
B. 平衡时压强:P1>P2
C. 容器体积:V1<V3
D. 若实验②中O2和Cl2用量均加倍,则平衡时O2的转化率小于70%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,对于反应N2(g)+3H2(g) ![]() 2NH3(g)△H=-92.4 kJ·mol-1。N2的平衡转化率(
2NH3(g)△H=-92.4 kJ·mol-1。N2的平衡转化率(![]() )与体系总压强(P)的关系如右图所示。下列说法正确的是( )
)与体系总压强(P)的关系如右图所示。下列说法正确的是( )
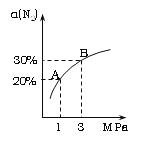
A. 将1.0mol氮气、3.0mol氢气,置于1L密闭容器中发生反应,放出的热量为92.4kJ。
B. 平衡状态由A变到B时,平衡常数K(A) < K(B)
C. 上述反应在达到平衡后,增大压强,H2的转化率提高
D. 升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com