
金属铜不溶于稀硫酸,可溶于铁盐溶液生成铜盐与亚铁盐。现将一定量的铜片加入到100 mL稀硫酸和硫酸铁的混合液中,铜片完全溶解(不考虑盐的水解及溶液体积的变化)
(1)写出铜溶解于上 述混合液的离子方程式_____________________________。
述混合液的离子方程式_____________________________。
(2)若铜完全溶解时,溶液中的Fe3+、Cu2+、H+三种离子的物质的量浓度相等,且测得溶液的pH=1,则溶解铜的质量是________ g,溶液中的c(SO )=________ mol/L。
)=________ mol/L。
(3)若欲在如图所示的装置中发生(1)中的反应,请判断图中的正、负极,并选出适当的物质作电极,写出电极反应式,填在相应的表格中。
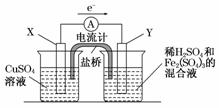
| 正、负极判断 | 电极材料 | 电极反应式 | |
| X极 | |||
| Y极 |
解析:(1)Cu与Fe2(SO 4)3反应生成CuSO4和FeSO4,可知离子方程式为Cu+2Fe3+===Cu2++2Fe2+;
4)3反应生成CuSO4和FeSO4,可知离子方程式为Cu+2Fe3+===Cu2++2Fe2+;
(2)溶液中的Fe3+、Cu2+、H+三种离子的物质的量浓度相等,且测得溶液的pH=1,故c(H+)=c(Cu2+)=0.1 mol/L,故n(Cu2+)=0.1 mol/L×0.1 L=0.01 mol,溶解铜的质量为0.01 mol×64 g/mol=0.64 g;反应后溶液中的阳离子为:Fe3+、Fe2+、Cu2+、H+,而Cu+2Fe3+===Cu2++2Fe2+,可见Fe2+的物质的量浓度为Cu2+的两倍,依据溶液中的电荷守恒规律,故0.1 mol/L×3+0.2 mol/L×2+0.1 mol/L×2+0.1 mol/ L×1=c(SO
L×1=c(SO )×2,解得c(SO
)×2,解得c(SO )=0.5 mol/L。
)=0.5 mol/L。
答案:(1)Cu+2Fe3+===Cu2++2Fe2+
(2)0.64 0.5
(3)
| 正、负极判断 | 电极材料 | 电极反应式 | |
| X极 | 负极 | 铜 | Cu-2e-===Cu2+ |
| Y极 | 正极 | 碳 | 2Fe3++2e-===2Fe2+ |


科目:高中化学 来源: 题型:
过渡金属配合物的一些特有性质的研究正受到许多研究人员的关注,因为这方面的研究无论是理论上还是工业应用上都具有重要意义。
(1)铜离子与氨基酸形成的配合物具有杀菌、消炎和抗肿瘤活性。与铜属于同一周期,且未成对电子数最多的元素基态原子的核外电子排布式为____________________。
(2)CO可以和很多过渡金属形成配合物,如羰基铁[Fe(CO)5]、羰基镍[Ni(CO)4]。CO分子中C原子上有一对孤电子对,C、O原子都符合8电子的稳定结构,CO的结构式为________,与CO互为等电子体的离子为________________________________________________________________________
(填化学式)。C、N、O三种元素的第一电离能由大到小的顺序为____________。
(3)氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子的结构如图K345所示:
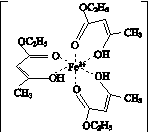
图K345
①此配离子中含有的作用力有______________(填字母)。
A.离子键 B.金属键 C.极性键 D.非极性键
E.配位键 F.氢键 G.σ键 H.π键
②此配合物中碳原子的杂化轨道类型有____________。
(4)Ti3+可形成配位数为6的配合物。现有钛的两种颜色的配合物,一种为紫色,另一种为绿色。相关实验证明,两种物质的组成皆为TiCl3·6H2O。为测定这两种配合物的成键情况,设计了如下实验:分别取等质量的两种物质的样品配成待测溶液;分别往待测溶液中滴入过量的AgNO3溶液并充分反应,均产生白色沉淀;测定沉淀质量并比较,发现由原绿色物质得到的沉淀质量是由原紫色物质得到的沉淀质量的2/3。则原绿色配合物的内界的化学式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法在一定条件下可以实现的是
①酸性氧化物与碱反应 ②弱酸与盐溶液反应可生成强酸 ③没有水生成,也没有沉淀和气体生成的复分解反应 ④两种酸溶液充分反应后的溶液呈中性 ⑤有单质参加的非氧化还原反应 ⑥两种含氧化合物反应的产物有气体
A.①②③④⑤⑥ B.②④⑤⑥
C.①②③⑤ D.③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
根据氧化还原反应:2Ag+(aq)+Cu(s)===Cu2+(aq)+2Ag(s)设计的原电池如图所示,其中盐桥为琼脂-饱和KNO3盐桥。
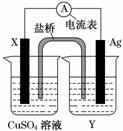
请回答下列问题:
(1)电极X的材料是________;电解质溶液Y是________;
(2)银电极为电池的____极,写出两电极的电极反应式:
银电极:____________;X电极:____________。
(3)外电路中的电子是从______电极流向______电极。
(4)盐桥中向CuSO4溶液中迁移的离子是________(填序号)。
A.K+ B.NO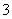
C.Ag+ D.SO
查看答案和解析>>
科目:高中化学 来源: 题型:
某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构如图,电池总反应可表示为:2H2+O2===2H2O,下列有关说法正确的是( )
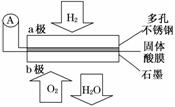
A.电子通过外电路从b极流向a极
B.b极上的电极反应式为:O2+2H2O+4e-===4OH-
C.每转移0.1 mol电子,消耗1.12 L的H2
D.H+由a极通过固体酸电解质传递到b极
查看答案和解析>>
科目:高中化学 来源: 题型:
下列性质的递变中,正确的是
A.O、Na、S的原子半径依次增大 B.LiOH、KOH、CsOH的碱性依次增强
C.HF、NH3、SiH4的稳定性依次增强 D.HCl、HBr、HI的还原性依次减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
将纯锌片和纯铜片按下图所示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是

A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的酸性均减弱
D.产生气泡的速率甲比乙慢
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇。
I:CH4 ( g ) + H2O ( g )=CO ( g ) + 3H2 ( g )
II:CO ( g ) + 2H2 ( g )=CH3OH ( g )
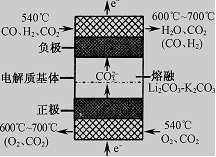
(1)反应(I)制得的混合气体和水煤气成分相同,也能形成燃料电池。下图是利用其作原料,采用熔融碳酸盐为电解质的燃料电池工作原理示意图,则该电池的负极反应式可表示为:
。
(2)在使用甲醇时,若有残留,对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化。实验室用下图装置模拟上述过程:
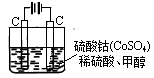
①写出阳极电极反应式 。
②写出除去甲醇的离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com