
【题目】25℃时,下列各组离子在指定溶液中能大量共存的是( )
A.pH =1的溶液中:NH4+、SO42-、ClO-、Na+
B. 的溶液中:Na+、K+、MnO4-、HCO3-
的溶液中:Na+、K+、MnO4-、HCO3-
C.0.1molL-1的Na2SO3溶液中:H+、K+、SO42-、NO3-
D.澄清透明的溶液中:Fe3+、Na+、Cl-、SO42-
科目:高中化学 来源: 题型:
【题目】下列有关AgCl沉淀的溶解平衡的说法中正确的是( )
A.AgCl沉淀生成和沉淀溶解不断进行,但速率相等
B.AgCl难溶于水,溶液中没有Ag+和Cl-
C.升高温度,AgCl沉淀的溶解度减小
D.在有AgCl沉淀生成的溶液中加入NaCl固体,AgCl沉淀溶解的量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NaOH溶液分别加到HA、HB两种弱酸溶液中,两溶液中pH与粒子浓度比值的对数关系如图所示,已知![]() ,下列有关叙述错误的是( )
,下列有关叙述错误的是( )

A.HA、HB两种酸中,HB的酸性弱于HA
B.b点时,![]()
C.同浓度同体积的NaA和NaB溶液中,阴离子总数相等
D.向HB溶液中加入NaOH溶液所得的混合溶液中,
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2.0molPCl3和1.0molCl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)PCl5(g)达平衡时,PCl5为0.4mol,如果此时移走1.0molPCl3和0.50molCl2,在相同温度下再达平衡时PCl5的物质的量是( )
A. 0.4mol
B. 0.2mol
C. 小于0.2mol
D. 大于0.2mol,小于0.4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g)+2D(g),经5min后,测得D的浓度为0.5mol·L-1,C的平均反应速率是0.1mol·L-1·min-1,且此时A、B的物质的量浓度之比为2∶3。下列说法错误的是
xC(g)+2D(g),经5min后,测得D的浓度为0.5mol·L-1,C的平均反应速率是0.1mol·L-1·min-1,且此时A、B的物质的量浓度之比为2∶3。下列说法错误的是
A.x的值是2
B.开始时B的物质的量为3mol
C.5min时,B的物质的量浓度为1.5 mol·L-1
D.5min时,容器中气体总的物质的量为7mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】B和Mg在材料科学领域有广泛的应用和发展前景。
回答下列问题:
(1)下列B原子轨道表达式表示的状态中,能量更高的是________![]() 填“A”或“B”
填“A”或“B”![]() 。
。
A. ![]() B.
B. ![]()
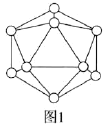
(2)晶体硼中的基本单元如图1所示,其中含有12个B原子。![]() 该单元中含有
该单元中含有![]() 键的数目为________。
键的数目为________。
(3)![]() 是重要的还原剂。其中阴离子的立体构型为________,中心原子的杂化形式为________。
是重要的还原剂。其中阴离子的立体构型为________,中心原子的杂化形式为________。
(4)基态Mg原子的核外电子排布式为________;第三周期主族元素中,电负性小于Mg元素的有________![]() 填元素符号,下同
填元素符号,下同![]() ,原子第一电离能小于Mg原子的有________。
,原子第一电离能小于Mg原子的有________。
(5)![]() 和
和![]() 均可作为耐火材料,其原因是________。
均可作为耐火材料,其原因是________。
(6)![]() 常用于光学仪器,其长方体型晶胞结构如图2所示:
常用于光学仪器,其长方体型晶胞结构如图2所示:
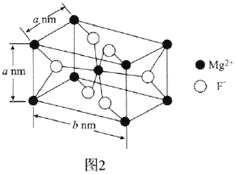
![]() 的配位数为________。
的配位数为________。
![]() 若阿伏加德罗常数的值为
若阿伏加德罗常数的值为![]() ,则
,则![]() 晶体的密度可表示为________
晶体的密度可表示为________![]() 用含a、b、
用含a、b、![]() 的代数式表示
的代数式表示![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】消除氮氧化物、二氧化硫等物质造成的污染是目前研究的重要课题。
(1)工业上常用活性炭还原一氧化氮,其反应为:2NO(g)+C(s) N2(g)+CO2(g)。向容积均为l L的甲、乙、丙三个恒容恒温容器中分别加入足量的活性炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
0min | 40min | 80min | 120min | 160min | ||
甲 | T℃ | 2mol | 1.45 mol | 1 mol | 1 mol | 1 mol |
乙 | 400℃ | 2 mol | 1.5 mol | 1.1 mol | 0.8 mol | 0.8 mol |
丙 | 400℃ | 1 mol | 0.8 mol | 0.65 mol | 0.53 mol | 0.45 mol |
甲容器反应温度T℃______400℃(填“>”“<”或“=”);乙容器中,0~40min内平均反应速率v(CO2)=_____________________;丙容器中达平衡后NO的物质的量为_________mol。
(2)活性炭还原NO2的反应为:2NO2(g)+2C(s) N2(g)+2CO2(g),在恒温条件下,l mol NO2和足量活性炭发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
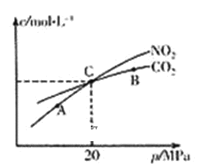
①A、B、C三点中NO2的转化率最高的是_________点(填“A”或“B”或“C”)。
②计算C点时该反应的压强平衡常数KP=_______MPa(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)燃煤烟气脱硫常用如下方法。
方法①:用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫。涉及的部分反应如下:
2CO(g)+SO2(g)=S(g)+2CO2(g) △H1=8.0 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H2=-566.0kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H3=-483.6 1kJ·mol-1
则H2(g)还原SO2(g)生成S(g)和H2O(g)的热化学方程式为:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现需设计一套实验装置来电解饱和食盐水,并测量电解产生的氢气的体积(约6 mL)和检验氯气的氧化性(不应将多余的氯气排入空气中)。
(1)试从下图中选用几种必要的仪器,连成一整套装置,各种仪器接口的连接顺序(填编号)是A接G-F-I,B接__________。
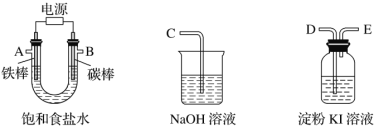
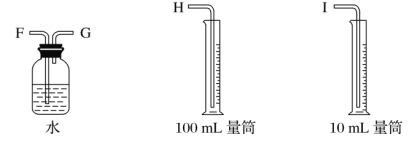
(2)铁棒接直流电源的________极;碳棒上发生的电极反应为_____________________________________。
(3)能说明氯气具有氧化性的实验现象是_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由X、Y和Z合成缓释药物M,下列说法不正确的是
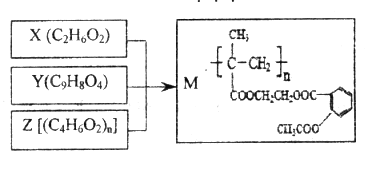
A. M在体内能缓慢发生水解反应
B. X可以由乙烯通过加成反应和取代反应制各
C. 1molY与NaOH溶液反应,最多能消耗3mol NaOH
D. Z由加聚反应制得,其单体的结构简式是CH3CH=CHCOOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com