
【题目】现需设计一套实验装置来电解饱和食盐水,并测量电解产生的氢气的体积(约6 mL)和检验氯气的氧化性(不应将多余的氯气排入空气中)。
(1)试从下图中选用几种必要的仪器,连成一整套装置,各种仪器接口的连接顺序(填编号)是A接G-F-I,B接__________。
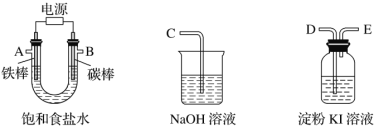
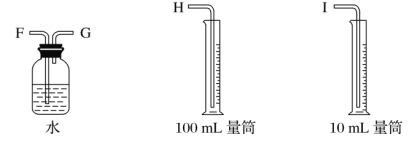
(2)铁棒接直流电源的________极;碳棒上发生的电极反应为_____________________________________。
(3)能说明氯气具有氧化性的实验现象是_______________________________________。
【答案】D、E、C 负极 2Cl——2e—=Cl2↑ 淀粉—KI溶液变成蓝色
【解析】
由电解产生的氢气的体积约6 mL和检验氯气的氧化性可知,铁棒作阴极,铁棒上产生的是氢气;碳棒作阳极,从B口导出的是氯气,碳棒上发生的电极反应为2Cl——2e—=Cl2↑。
(1)根据装置图可知碳棒是阳极,产生氯气。铁棒是阴极,产生的是氢气,可以通过排水法测量氢气的体积,由于氢气的体积约是6mL,所以选择10mL量筒。利用淀粉碘化钾检验氯气的氧化性,利用氢氧化钠溶液吸收多余的氯气,则正确的连接顺序是A 、G、F、I;B、D、E、C;
(2)铁棒是阴极,连接电源的负极,碳棒是阳极,氯离子放电,反应式为2Cl——2e—=Cl2↑;
(3)淀粉—KI溶液变成蓝色能说明氯气具有氧化性。


 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:
【题目】(1)某二元酸(化学式用H2A表示)在水中的电离方程式是H2A═H++HA-,HA-![]() H++A2-;试完成下列问题:
H++A2-;试完成下列问题:
NaHA溶液显__(填“酸性”、“中性”或“碱性”),Na2A溶液显__(填“酸性”、“中性”或“碱性”)。理由是__(用离子方程式表示)。
(2)pH=5的NH4Cl溶液与pH=5的HCl溶液中由水电离出的c(H+)分别是__、__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列各组离子在指定溶液中能大量共存的是( )
A.pH =1的溶液中:NH4+、SO42-、ClO-、Na+
B. 的溶液中:Na+、K+、MnO4-、HCO3-
的溶液中:Na+、K+、MnO4-、HCO3-
C.0.1molL-1的Na2SO3溶液中:H+、K+、SO42-、NO3-
D.澄清透明的溶液中:Fe3+、Na+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况,试判断哪些违反了泡利原理________,哪些违反了洪特规则________。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
(2)![]() 可用于制造火柴,其分子结构如图所示。
可用于制造火柴,其分子结构如图所示。

![]() 分子中硫原子的杂化轨道类型为________。
分子中硫原子的杂化轨道类型为________。
![]() 每个
每个![]() 分子中含有的孤电子对的数目为________。
分子中含有的孤电子对的数目为________。
(3)科学家合成了一种阳离子“![]() ”,其结构是对称的,5个N排成“V”形,每个N都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“
”,其结构是对称的,5个N排成“V”形,每个N都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“![]() ”的化学式为“
”的化学式为“![]() ”的离子晶体,其电子式为________。分子
”的离子晶体,其电子式为________。分子![]() 中键与键之间的夹角为
中键与键之间的夹角为![]() ,并有对称性,分子中每个原子的最外层均满足8电子稳定结构,其结构式为________________。
,并有对称性,分子中每个原子的最外层均满足8电子稳定结构,其结构式为________________。
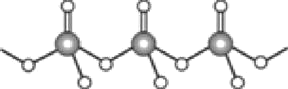
(4)直链多磷酸根阴离子是由两个或两个以上磷氧四面体通过共用顶角氧原子连接起来的,如图所示。则由n个磷氧四面体形成的这类磷酸根离子的通式为________。
(5)碳酸盐中的阳离子不同,热分解温度就不同。下表为四种碳酸盐的热分解温度和金属阳离子半径
碳酸盐 |
|
|
|
|
热分解温度 | 402 | 900 | 1172 | 1360 |
金属阳离子半径 | 66 | 99 | 112 | 135 |
随着金属阳离子半径的增大,碳酸盐的热分解温度逐步升高,原因是_____________。
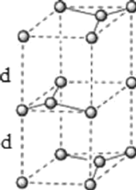
(6)石墨的晶体结构和晶胞结构如图所示。已知石墨的密度为![]() ,
,![]() 键的键长为
键的键长为![]() ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为![]() ,则石墨晶体的层间距为________cm。
,则石墨晶体的层间距为________cm。
 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是

A. 铜电极上发生氧化反应
B. 电池工作一段时间后,甲池的c(SO42-)减小
C. 电池工作一段时间后,乙池溶液的总质量增加
D. 阴阳离子离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。化工生产的副产氢也是氢气的来源。电解法制取有广泛用途的Na2FeO4,同时获得氢气:Fe+2H2O+2OH―= FeO42―+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色FeO42―,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。回答下列问题:

(1)铁作________极,电极反应式为___________________________________________________。
(2)每制得1mol Na2FeO4,理论上可以产生标准状况 ____________ L 气体。
(3)电解一段时间后,c(OH―)降低的区域在_______________________(填“阴极室”或“阳极室”)。
(4)电解过程中,须将阴极产生的气体及时排出,其原因为_____________________。
(5)c(Na2FeO4)随初始c(NaOH)的变化如图2,分析M点c(Na2FeO4)低于最高值的原因_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,CH3COOH和NH3·H2O的电离常数均为1.8×10-5。向20 mL浓度均为0.1 mol/L NaOH和NH3·H2O的混合液中滴加等物质的量浓度的CH3COOH溶液,所得混合液的导电率与加入CH3COOH溶液的体积(V)的关系如图所示。下列说法不正确的是

A. a=20,b=40,且溶液呈中性处于A、B两点之间
B. B点溶液中:c(CH3COO-)>c(Na+)>c(NH![]() )
)
C. 已知lg3≈0.5,则C点的pH≈5
D. A、B、C三点中,B点溶液中水的电离程度最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸、碱、盐都属于电解质,是工业生产、科研领域的重要原料,请按要求回答下列问题:
(1)现有四种稀溶液,分别是:A.硫酸溶液 B.甲酸溶液 C. NaOH溶液 D.氨水
取其中两种溶液发生中和反应,请选择合适的对象完成题目的解答:
①A和C的稀溶液发生中和反应生成1mol水时,放出57.3kJ的热量,请写出此中和反应的热化学方程式______________________________.
②酸碱中和滴定时,须选择合适的指示剂,下列酸碱组合进行滴定时,不能选择甲基橙为指示剂是____(选填字母)
a.A和C b.A和D c. B和 C d. B和D
③B中甲酸的用途之一是用于配制“缓冲溶液”(HCOOH~HCOONa)。请写出甲酸电离方程式___________________________;已知一定温度下,甲酸的电离平衡常数 Ka=1.8×10-4,若用 0.2mol·L-1HCOOH 溶液100mL配制pH为4的缓冲溶液,需加入_______mL(答案保留一位小数) 0.2mol· L-1NaOH溶液。
(2)砷(As)是一些工厂和矿山废水中的污染元素,H3AsO3(亚砷酸)和H3AsO4(亚砷酸)水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度总和的比值)与pH关系分别如图所:
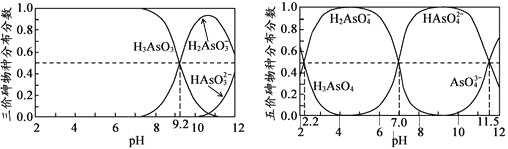
①以酚酞为指示剂,将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加,此时砷元素的主要存在形式为________________(填微粒的化学式)②已知 pKa1 = —lgKa1
H3AsO4第一步电离方程式为H3AsO4![]() H2AsO4- + H+ 电离常数为Ka1,则pKa1=______。
H2AsO4- + H+ 电离常数为Ka1,则pKa1=______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】低碳经济成为人们一种新的生活理念,二氧化碳的捕捉和利用是一个重要研究方向, 既可变废为宝,又可减少碳的排放。工业上可用CO2和H2制备被誉为“21世纪的清洁燃料”二甲醚(CH3OCH3):
如在500℃时,在密闭容器中将炼焦中的CO2转化为二甲醚,其相关反应为:
主反应I:2CO2 (g)+6H2(g)![]() CH3OCH3(g)+3H2O(g) △H1
CH3OCH3(g)+3H2O(g) △H1
副反应II:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
(1)已知:①CO(g)+2H2(g)![]() CH3OH(g) △H=-90.1kJ/mol
CH3OH(g) △H=-90.1kJ/mol
②2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H=-24.5kJ/mol
CH3OCH3(g)+H2O(g) △H=-24.5kJ/mol
③CO(g)+H2O(g)![]() CO2(g)+H2(g) △H= -41.0kJ/mol
CO2(g)+H2(g) △H= -41.0kJ/mol
则主反应I的△H1=______。
(2)在一定温度下某密闭容器中按CO2和H2的浓度比为1:3投料进行反应,测得不同时间段部分物质的浓度如下表:

①10-20min 内,CH3OCH3的平均反应速率v(CH3OCH3)=_______。
②根据以上数据计算主反应I的平衡常数K=______(列式,代入数据,不计算结果)。
(3)欲提高CH3OCH3产率的关键的因素是选用合适的催化剂,其原因是_______。
(4)对于反应II,温度对CO2的转化率及催化剂的效率影响如图所示:下列有关说法不正确的是_______。

A.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于Ml
B.温度低于250°C时,随温度升高甲醇的产率增大
C.M点时平衡常数比N点时平衡常数大
D.实际反应应尽可能在较低的温度下进行,以提高CO2的转化
(5)利用太阳能电池将CO2转化为乙烯、丙烯等有机化工原料,其工作原理如图所示。则a为太阳能电池的_______极,写M极上生成丙烯的电极反应式为_________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com