
某种聚合物锂离子电池放电时的反应为Li1-xCoO2+LixC6=6C+LiCoO2,其电池如图所示。下列说法不正确的是 ( )。
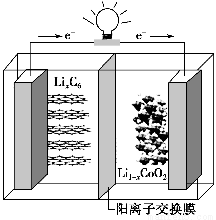
A.放电时,LixC6发生氧化反应
B.充电时,Li+通过阳离子交换膜从左向右移动
C.充电时将电池的负极与外接电源的负极相连
D.放电时,电池的正极反应为Li1-xCoO2+xLi++xe-=LiCoO2
 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源:2014年化学高考题型专练十三 有机物结构及同分异构体数目判断练习卷(解析版) 题型:选择题
相对分子质量为100的烃,且含有4个甲基的同分异构体共有(不考虑立体异构)( )。
A.3种 B.4种 C.5种 D.6种
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练八 化学反应速率和化学平衡分析与判断练习卷(解析版) 题型:选择题
合成氨所需的氢气可用煤和水作原料经过多步反应制得,其中的一步反应为:CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0。反应达到平衡后,为提高CO的转化率,下列措施中正确的是( )。
CO2(g)+H2(g) ΔH<0。反应达到平衡后,为提高CO的转化率,下列措施中正确的是( )。
A.增加压强 B.降低温度 C.增大CO的浓度 D.更换催化剂
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练三 特定条件下离子方程式的书写与判断练习卷(解析版) 题型:选择题
下列离子方程式书写正确的是 ( )。
A.Fe3O4溶于足量稀HNO3:3Fe3O4+28H++NO3—=9Fe3++NO↑+14H2O
B.用食醋检验牙膏中碳酸钙的存在:CaCO3+2H+=Ca2++CO2↑+H2O
C.FeCl2酸性溶液放在空气中变质:2Fe2++4H++O2=2Fe3++2H2O
D.电解MgCl2水溶液的离子方程式:2Cl-+2H2O H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练三 特定条件下离子方程式的书写与判断练习卷(解析版) 题型:选择题
下列所述事实与化学(或离子)方程式不相符的是 ( )。
A.能说明氧化性H2O2>Fe3+:2Fe2++H2O2+2H+=2Fe3++2H2O
B.能说明NH3结合H+能力比H2O强:NH3+H3O+=NH4++H2O
C.能说明盐酸是强酸:2HCl+CaCO3=CaCl2+CO2↑+H2O
D.能说明CH3COOH是弱电解质:CH3COO-+H2O CH3COOH+OH-
CH3COOH+OH-
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练一 化学与科学技术社会环境的关系练习卷(解析版) 题型:选择题
下列有关叙述不正确的是( )。
A.在家用燃煤中加入适量的生石灰能有效减少二氧化硫的排放量
B.利用太阳能、潮汐能、风能发电,可以获取清洁能源
C.大量排放SO2、氮氧化物或CO2都会导致酸雨的形成
D.采用纳米二氧化钛光触媒技术,将汽车尾气中的NO和CO转化为无害气体
查看答案和解析>>
科目:高中化学 来源:2014年化学高考课时演练10甲烷乙烯苯煤石油天然气的综合利用练习卷(解析版) 题型:填空题
下表是A、B、C、D、E五种有机物的有关信息:
A①能使溴的四氯化碳溶液褪色;
②比例模型为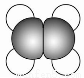
③能与水在一定条件下反应生成C
B①由C、H两种元素组成。
②球棍模型为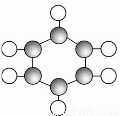
C①由C、H、O三种元素组成;
②能与Na反应;
③与E反应生成相对分子质量为88的酯
D①相对分子质量比C少2;
②能由C催化氧化得到
E①由C、H、O三种元素组成;
②其水溶液能使紫色石蕊试液变红
回答下列问题:
(1)A~E中,属于烃的是___________(填字母)。
(2)A能使溴的四氯化碳溶液褪色,发生反应的化学方程式为_______________。
(3)C催化氧化生成D的化学方程式为_________________________________。
(4)有机物B具有的性质是__________ (填序号)。
①无色无味的液体;②有毒;③不溶于水;④密度比水大;⑤能使酸性KMnO4溶液和溴水褪色
(5)E的水溶液能使紫色石蕊试液变红,说明E的水溶液显酸性,现设计一个实验来比较E与碳酸酸性的强弱,则该实验的原理是________________________(用化学方程式说明)。
查看答案和解析>>
科目:高中化学 来源:2014年化学高考课时演练 7-3化学平衡常数化学反应进行方向练习卷(解析版) 题型:选择题
已知:2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH=-25 kJ/mol 某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
CH3OCH3(g)+H2O(g) ΔH=-25 kJ/mol 某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:

下列说法正确的是( )
①平衡后升高温度,平衡常数>400
②平衡时,c(CH3OCH3)=1.6 mol/L
③平衡时,反应混合物的总能量减少20 kJ
④平衡时,再加入与起始等量的CH3OH,达新平衡后CH3OH转化率增大
⑤此时刻反应达到平衡状态
⑥平衡时CH3OH的浓度为0.08 mol·L-1
A.①②④⑤ B.②⑥
C.②③④⑥ D.②④⑥
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习课时演练 9-1原电池 化学电源练习卷(解析版) 题型:选择题
下列防腐措施中,利用原电池反应使主要金属得到保护的是( )
A.用氧化剂使金属表面生成致密稳定的氧化物保护膜
B.在金属中加入一些铬或镍制成合金
C.在轮船的壳体水线以下部分装上锌锭
D.金属表面喷漆
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com