
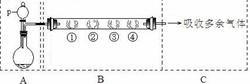
| B中棉花的位置 | ① | ② | ③ | ④ |
| 所蘸试剂 | 石蕊试液 | 品红溶液 | 淀粉和碘水混合液 | 氢硫酸 |
| 现象 | | | 褪色 | 浅黄色 |
| 体现SO2的性质 | | | | |
| | | | | |
| | | | | |
| | 溶液变红 | 溶液褪色 | | |
| | 水溶液显酸性 | 漂白性 | 还原性 | 氧化性 |
 ------------------------1分
------------------------1分 -----------------------------------------1分
-----------------------------------------1分

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.鉴别氯化钠和氯化钾,用焰色反应 | B.用激光笔鉴别氢氧化铁胶体和氯化铁溶液 |
| C.用酒精萃取溴水中的溴 | D.用湿润的红色石蕊试纸,检验氨气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
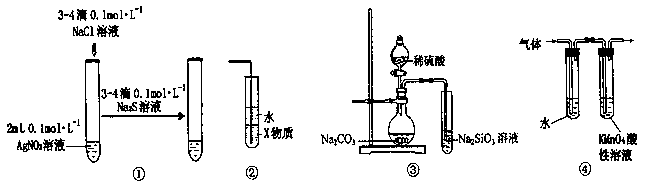
| A.装置①能验证AgCl沉淀可转化为溶解度更小的Ag2S沉淀 |
| B.装置②中X若为四氯化碳,可用于吸收氨气,并防止倒吸 |
| C.装置③的实验可推断硫、碳、硅三种元素的非金属性强弱 |
| D.装置④可检验溴乙烷发生消去反应得到的气体中含有乙烯 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 Fe2O3+SO2↑+SO3↑+14H2O↑;下图的装置可用来检验上述反应中所有的气体产物,请回答下列问题:
Fe2O3+SO2↑+SO3↑+14H2O↑;下图的装置可用来检验上述反应中所有的气体产物,请回答下列问题: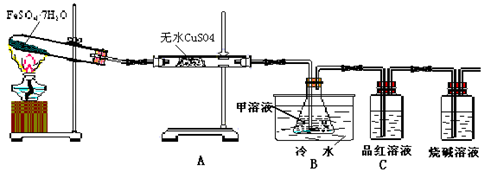
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
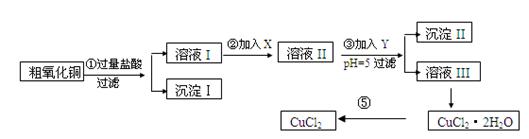
| 物质 | 开始沉淀时pH | 完全沉淀时pH |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Cu(OH)2 | 5.2 | 6.4 |
| 氧化剂 | 调节pH的物质 | ||
| A | 双氧水 | D | 氨水 |
| B | 高锰酸钾 | E | 碱式碳酸铜 |
| C | 氯水 | F | 氧化铜 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 滴定 次数 | 待测溶液的体积 /mL | 标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.B中导气管中产生气泡 | B.B中导气管里 形成一段水柱 形成一段水柱 |
| C.金属片剪口变红 | D.锌被腐蚀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用待测液润洗滴定用的锥形瓶 |
| B.中和滴定时右手操作滴定管,左手摇动锥形瓶,眼睛注视滴定管液面的变化 |
| C.用酸式滴定管量取20.00 mL KMnO4溶液 |
| D.为减小中和滴定误差,锥形瓶必须洗净并烘干后才能使用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com