
| A. | 向硫酸铝溶液中逐滴加入过量氢氧化钠溶液 | |
| B. | 向氯化铁溶液中逐滴加入过量氨水 | |
| C. | 向硅酸钠溶液中逐滴加入过量稀盐酸 | |
| D. | 向氢氧化钙溶液中缓缓通入过量二氧化碳 |
分析 A.向硫酸铝溶液中滴加氢氧化钠溶液至过量,首先生成氢氧化铝沉淀,后来沉淀又与氢氧化钠反应生成偏铝酸钠;
B.向氯化铁溶液中逐滴加入过量氨水,生成红褐色沉淀氢氧化铁;
C.硅酸钠盐酸反应生成硅酸,硅酸不溶于水,和盐酸也不反应;
D.氢氧化钙是碱,能与二氧化碳反应生成碳酸钙沉淀,当二氧化碳过量时继续反应,先生成碳酸氢钙沉淀,碳酸氢可钙溶于水.
解答 解:A.向硫酸铝溶液中滴加氢氧化钠溶液至过量,首先生成氢氧化铝沉淀,后来沉淀又与氢氧化钠反应生成偏铝酸钠,所以看到的现象是“先产生沉淀,然后沉淀又溶解”,所以符合条件,故A正确;
B.向氯化铁溶液中逐滴加入过量氨水生成氢氧化铁和氯化铵,无沉淀溶解现象,故B错误;
C.根据硅酸钠和盐酸的性质,盐酸的酸性比硅酸的强,因此硅酸钠溶液与稀盐酸溶液能发生反应,反应方程式为:Na2SiO3+2HCl═2NaCl+H2SiO3↓,而且而且生成的硅酸有不溶于水,并与盐酸也不反应,因此现象是,有沉淀出现,故C错误;
D.根据氢氧化钙和二氧化碳的性质,当向氢氧化钙溶液中缓缓通入过量二氧化碳时,首先发生Ca(OH)2+CO2═CaCO3↓+H2O,再根据碳酸盐和碳酸氢盐可以相互转化的性质,生成的碳酸钙又和继续通入的二氧化碳继续反应生成可溶于水的碳酸氢钙,反应方程式为CaCO3+CO2+H2O═Ca(HCO3)2,因此现象是:先出现沉淀后沉淀溶解,故D正确;
故选AD.
点评 本题考查物质之间的化学反应,熟悉复分解反应发生的条件及常见物质的溶解性是解答本题的关键,注意有些反应与反应物的量有关,量不同反应现象不同,题目难度中等.


科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=1的溶液中,NH4+、Fe3+、SO42-、Cl- | |
| B. | 通入过量SO2气体的溶液中:Fe3+、NO3-、Ba2+、H+ | |
| C. | c(Al3+)=0.1mol/L的溶液中:Na+、K+、AlO2-、SO42- | |
| D. | 由水电离出的c(H+)=1×10-13mol/L的溶液中:Na+、HCO3-、Cl-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯中所有原子都在同一个平面上 | B. | 不能在空气中燃烧 | ||
| C. | 不能使酸性高锰酸钾溶液褪色 | D. | 光照条件下与氯气发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16O与18O互为同位素;H216O、D216O、H218O、D218O互为同素异形体 | |
| B. | SiH4、PH3、HCl的稳定性逐渐增强 | |
| C. | 乙烯的结构简式CH2CH2 | |
| D. | Ca2+的结构示意图为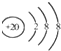 NH4Cl的电子式为 NH4Cl的电子式为 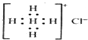 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将块状的C研成粉末状 | |
| B. | 将容器的体积缩小一半 | |
| C. | 保持体积不变,充入N2使体系压强增大 | |
| D. | 保持压强不变,充入N2使容器体积变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
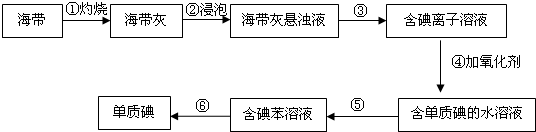
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com