
 .
. 分析 (1)根据A的相对分子量及含碳量计算出含有C原子数,从而可知H原子数,然后结合相对分子质量计算出含有O原子数,从而可确定A的分子式;
(2)根据A的分子式及限制条件判断其取代基类型,然后判断其同分异构体数目.
解答 解:(1)有机物A分子中含苯环,相对分子质量136,其含碳质量分数为70.6%,则A分子中含有C原子数为:$\frac{136×70.6%}{12}$=8,
A分子中碳、氢原子个数相等,A分子中含有8个H原子,则有机物A中含有O原子数为:$\frac{136-12×8-1×8}{16}$=2,
所以A的分子式为:C8H8O2,
故答案为:C8H8O2;
(2)A分子中含有苯环,能发生银镜反应,且有弱酸性,A的苯环侧链可能情况有:①两个取代基-OH和-CH2CHO,②含有3个取代基:-OH、-CHO和-CH3,
其中①的取代基-OH和-CH2CHO存在邻、间、对三种结构;
②中-OH、-CHO和-CH3可以都相邻,总共有3种结构,也可以都处于苯环的键位C上,有1种结构;只有2种取代基相邻时,固定两种,移动另一种取代基,总共有3种组合,每种组合有2种结构,所以总共有3×2=6种结构,
根据分析可知,满足条件的有机物的同分异构体总数目为:3+3+1+6=13,如: ,
,
故答案为:13; .
.
点评 本题考查了有机物分子式、结构简式的确定,题目难度中等,明确守恒思想在确定有机物分子式中的方法为解答关键,(2)为难点、易错点,注意掌握同分异构体的书写原则,试题培养了学生的分析、理解能力及灵活应用能力.


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 最外层电子数大于4的一定是非金属元素 | |
| B. | 元素周期表有18纵列,7横行,故有18个族,7个周期 | |
| C. | 第ⅠA族就是碱金属 | |
| D. | 某ⅡA族元素的原子序数为a,则和其同周期ⅢA的元素的原子序数可能为a+11 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
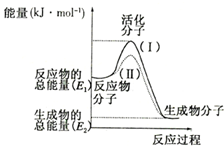 在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mo1表示.请认真观察如图,然后回答问题:
在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mo1表示.请认真观察如图,然后回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:推断题
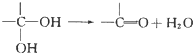
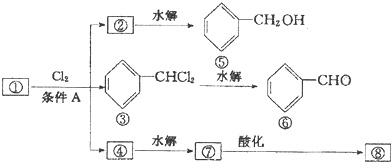
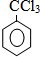 、
、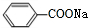 .
.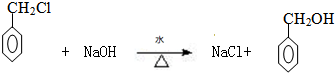 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,5.6L CO2与足量Na2O2反应转移的电子数为0.5NA | |
| B. | 2L 0.5mol•L-1亚硫酸溶液中含有的H +数为2NA | |
| C. | 常温常压下,46g NO2和N2O4的混合气体含有的原子数是3NA | |
| D. | 钠在空气中燃烧可生成多种氧化物,23g钠充分燃烧时转移电子数为1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向硫酸铝溶液中逐滴加入过量氢氧化钠溶液 | |
| B. | 向氯化铁溶液中逐滴加入过量氨水 | |
| C. | 向硅酸钠溶液中逐滴加入过量稀盐酸 | |
| D. | 向氢氧化钙溶液中缓缓通入过量二氧化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能与溴水反应而使溴水褪色 | B. | 能与H2发生加成反应 | ||
| C. | 能与浓硫酸、浓硝酸发生取代反应 | D. | 不能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H4的摩尔质量与6.02×1023个氮分子的质量在数值上相等 | |
| B. | 0.5mol二氧化氮和6.02×1023个氢分子的质量比等于23:2 | |
| C. | 32 g氧气所含的原子数目为2×6.02×1023 | |
| D. | 0.5×6.02×1023个二氧化碳分子所占体积是11.2 L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com