
【题目】亚硝酸氯(ClNO)可由NO与Cl2在通常条件下反应得列,化学方塑式为2NO(g) + Cl2(g)![]() 2ClNO(g)。
2ClNO(g)。
(1)在一定温度下,该反应于一恒容密闭容器中达到平衡,继续通入Cl2,逆反应速率_____( 填增大、减少、不变).
(2)己知几种化学键的键能数据如下表( 亚硝酸氯的结构为Cl-N=O)
化学键 | N≡O | Cl一Cl | Cl一N | N=O |
键能/kJ.mol-1 | 630 | 243 | a | 607 |
2NO(g)+Cl2(g)![]() 2ClNO(g) △H=-111kJ/mol,则a=_______。
2ClNO(g) △H=-111kJ/mol,则a=_______。
(3)在1L的恒容密闭容器中充入2molNO(g)和1mol Cl2(g),在不同温度下测得c(ClNO)与时间的关系如图A:

①该反应的△H_____0(填“>”“<”或“=”)。
②反应开始到10min 时NO 的平均反应速率v( NO) =________mol/(L.min).
③T2时该反应的平衡常数K=________。
(4)一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(Cl2)的变化图象如图B,则A、B、C 三状态中,NO 的转化率最大的是___点,当n(NO)/n(Cl2)=1.5时,达到平街状态ClNO 的体积分数可能是D、E、F三点中的______点。
【答案】 增大 200 < 0.1 2 A D
【解析】(1)在一定温度下,该反应于一恒容密闭容器中达到平衡,继续通入Cl2,压强增大,逆反应速率增大;(2)2NO(g)+Cl2(g)![]() 2ClNO(g) 反应的△H=反应物的键能之和-生成物的键能之和=(2×630+243)-(2a+2×607)=-111kJ/mol,解得a=200;
2ClNO(g) 反应的△H=反应物的键能之和-生成物的键能之和=(2×630+243)-(2a+2×607)=-111kJ/mol,解得a=200;
(3)①根据图像,T2>T1,降低温度c(C1NO)增大,说明平衡向正反应方向移动,说明正反应是放热反应,△H<0;
②反应开始到10min时,c(C1NO)=1mol/L,则v(C1NO)= ![]() =0.1mol/(L·min),则NO的平均反应速率v(NO)=v(C1NO)=0.1mol/(L·min);
=0.1mol/(L·min),则NO的平均反应速率v(NO)=v(C1NO)=0.1mol/(L·min);
③ 2NO(g)+Cl2(g) ![]() 2ClNO(g)
2ClNO(g)
起始(mol/L) 2 1 0
改变(mol/L) 1 0.5 1
平衡(mol/L) 1 0.5 1
T2时该反应的平衡常数K=![]() =
=![]() =2;
=2;
(4)n(NO)/n(C12)的比值越小,NO的转化率越大,NO的转化率最大的是A点,根据曲线的变化趋势,当n(NO)/n(C12)=1.5,达到平衡状态ClNO的体积分数是D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】已知正四面体形分子E和直线型分子G反应,生成四面体形分子L和直线型分子M.(组成E分子的元素的原子序数小于10,组成G分子的元素为第三周期的元素.)如图,则下列判断中正确的是( ) 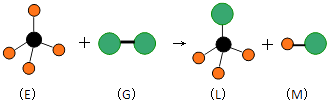
A.常温常压下,L是一种液态有机物
B.E是一种含有非极性键的分子
C.干燥的G 能漂白有色物质
D.上述反应的类型是取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组分别用如图所示装置对原电池和电解原理进行实验探究. 请回答:
Ⅰ.用图 1 所示装置进行第一组实验.
(1)在保证电极反应不变的情况下,不能替代 Cu 作电极的是(填字母序号).
(2)N 极发生反应的电极反应式为 . Ⅱ.用图 2 所示装置进行第二组实验.实验过程中,观察到与第一组实验不同的现象:两极 均有气体产生,Y 极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清. 查阅资料得知,高铁酸根离子(FeO42﹣)在溶液中呈紫红色.
(3)电解过程中,X 极区溶液的 pH(填“增大”“减小”或“不变”).
(4)电解过程中,Y 极发生的电极反应之一为 Fe﹣6e﹣+8OH﹣═Fe4O2﹣+4H2O 若在 X 极收集到672mL 气体,在 Y 极收集到 168mL 气体(均已折算为标准状况时气体体积),则 Y 电极(铁 电极)质量减少g.
(5)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为 2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2 . 该电池正极发生的反应的电极反应式为 . 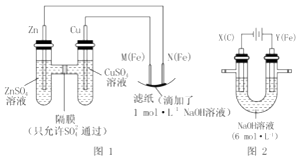
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质用途的说法不正确的是( )
A.明矾可用作净水剂
B.二氧化硫可用于熏蒸粉丝
C.碳酸氢钠可用于治疗胃酸过多
D.镁铝合金可用于制金属门窗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2CO(g)+O2(g)═2CO2(g)△H=﹣566kJ/mol
Na2O2(s)+CO2(g)═Na2CO3(s)+![]() O2(g)△H=﹣226kJ/mol
O2(g)△H=﹣226kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
A.CO的燃烧热为283kJ
B.25℃、101 kPa时,1 mol CO和2 mol CO的燃烧热相等
C.2Na2O2(s)+2CO2(s)═2Na2CO3(s)+O2(g)△H<﹣452 kJ/mol
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2A(g)+B(g) ![]() 2C(g),根据下表中的数据判断下列图象错误的是( )
2C(g),根据下表中的数据判断下列图象错误的是( )
| p1(Mpa) | p2(Mpa) |
400℃ | 99.6 | 99.7 |
500℃ | 96.9 | 97.8 |
A.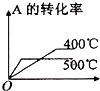
B.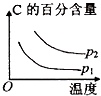
C.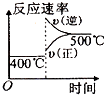
D.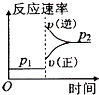
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式不正确的是
A. 铁与氯化铁溶液:2Fe3++ Fe ![]() 3Fe2+
3Fe2+
B. 碳酸钙与盐酸:CO32-+ 2H+![]() CO2↑+ H2O
CO2↑+ H2O
C. 二氧化硅与氢氧化钠溶液:SiO2 + 2OH-![]() SiO32-+ H2O
SiO32-+ H2O
D. 铜与稀硝酸:3Cu + 8H++ 2NO3-![]() 3Cu2+ + 2NO↑+ 4H2O
3Cu2+ + 2NO↑+ 4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】直接排放含SO2会形成酸雨,危害环境。某化学实验小组用如下装置进行有关SO2性质的探究活动。
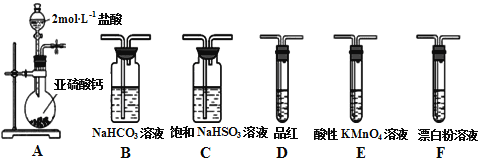
(1)装置A中反应的离子方程式为___________________________________。
(2)选用以上装置和药品探究亚硫酸与次氯酸的酸性强弱:甲同学认为按照A→C→F→尾气处理顺序连接装置可以证明,乙同学认为该方案不合理,其理由是___________________。正确的连接顺序是:A→C→___________→尾气处理(填字母)顺序连接装置。证明亚硫酸的酸性强于次氯酸的酸性的实验现象是__________________________。
(3)将二氧化硫通入以下装置可以制备Na2S2O3:

①装置B的作用是检验装置A中SO2的吸收效率,B中试剂是________________。
②写出装置A中发生反应的化学方程式___________________________________。
③Na2S2O3溶液是定量实验中的常用试剂,测定其浓度的过程如下:
第一步:准确称取a g KIO3(化学式量:214)固体配成溶液;
第二步:加入过量KI固体和H2SO4溶液,滴加指示剂;
第三步:用Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液的体积为V mL。则c(Na2S2O3)=____mol·L-1。(已知:IO3-+5I-+6H+= 3I2+3H2O, 2S2O32-+I2=S4O62-+2I-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com