
已知: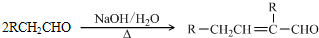
水杨酸酯E为紫外吸收剂,可用于配制防晒霜。E的一种合成路线如下:
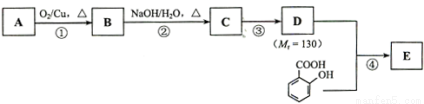
请回答下列问题:
(1)一元醇A中氧的质量分数约为21.6%。则A的分子式为 ;结构分析显示A只有一个甲基,A的名称为 。
(2)B能与新制的Cu(OH)2发生反应,该反应的化学方程式为 。
(3)C有 种结构;若一次取样,检验C中所含官能团,按使用的先后顺序写出所用试剂 ;
(4)第③的反应类型为 ;D所含官能团的名称为 。
(5)写出同时符合下列条件的水杨酸所有同分异构体的结构简式: 。
A、分子中含有6个碳原子在一条线上
B、分子中所含官能团包括水杨酸具有的官能团
(6)第④步的反应条件为 ;写出E的结构简式 。
(1)C4H10O 1-丁醇(或正丁醇)
(2)CH3CH2CH2CHO+2Cu(OH)2+NaOH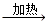 CH3CH2CH2COONa+Cu2O↓+3H2O
CH3CH2CH2COONa+Cu2O↓+3H2O
(3)2;银氨溶液、稀盐酸、溴水(或其他合理答案);
(4)还原反应(或加成反应);羟基;
(5)
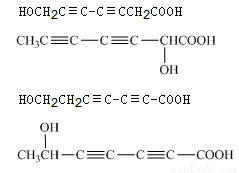
(6)浓硫酸、加热;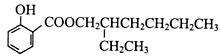
【解析】选本题的意图,就是提醒同学们,特别注意定量关系在有机推断中的应用,把做过的有定量试题归类,特别是有关官能团数目的确定。一元醇A中氧的质量分数约为21.6%,设该饱和一元醇的化学式为CnH2n+2O,16÷21.6%=74,则n=4,且A中只有一个甲基,所以该一元醇是1-丁醇。
(1)通过以上分析知,A的分子式为:C4H10O,结构分析显示A只有一个甲基,A的名称为1-丁醇;
(2)加热条件下,丁醛和新制氢氧化铜反应生成丁酸钠、氧化亚铜和水,反应方程式为:CH3CH2CH2CHO+2Cu(OH)2+NaOH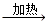 CH3CH2CH2COONa+Cu2O↓+3H2O
CH3CH2CH2COONa+Cu2O↓+3H2O
(3)丁醛发生加成反应生成物的结构简式为:CH3CH2CH2CH(OH)CH(CH2CH3)CHO,CH3CH2CH2CH(OH)CH(CH2CH3)CHO发生消去反应有两种生成物,C中含有醛基和碳碳双键,都能和溴水反应,要检验两种官能团,则应先用银氨溶液检验醛基,然后再用溴水检验碳碳双键,所以所加试剂先后顺序是:银氨溶液、稀盐酸、溴水;
(4)C和氢气发生加成反应(或还原反应)生成D,C中的醛基被还原生成羟基,所以D中含有羟基。
(5)写出水杨酸所有同分异构体的结构简式:水杨酸除了羧基,苯环的不饱和度为4,写6个碳原子在一条直线上时,应该有碳碳叁键两个。
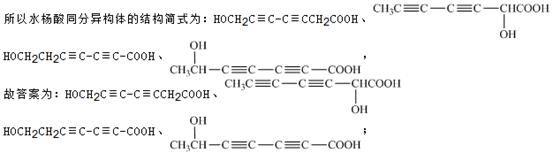
(6)第④步的反应是酯化反应,根据乙酸乙酯的反应条件知,该反应条件是浓硫酸作催化剂、加热,通过以上分析知,E的结构简式为
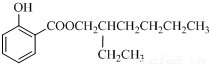


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案科目:高中化学 来源:2014高考名师推荐化学--预测5 题型:简答题
硫酸工业在国民经济中占有极其重要的地位。请回答硫酸工业中的如下问题:
(1)若从下列四个城市中选择一处新建一座硫酸厂,你认为厂址宜选在 郊
区(填标号);
A.有丰富黄铁矿资源的城市 B.风光秀丽的旅游城市
C.消耗硫酸甚多的工业城市 D.人口稠密的文化、商业中心城市
(2)CuFeS2 是黄铁矿的另一成分,煅烧时CuFeS2 转化为CuO、Fe2O3和SO2,
该反应的化学方程式为 。
(3)为提高SO3吸收率,实际生产中通常用 吸收SO3。
(4)已知反应2SO2+O2 SO3 △H <0,现将0.050mol SO2和0.030mol O2
SO3 △H <0,现将0.050mol SO2和0.030mol O2
充入容积为1L的密闭容器中,反应在一定条件下达到平衡,测得反应后容器压
强缩小到原来压强的75%,则该条件下SO2的转化率为________;该条件下的
平衡常数为__________。
(5)由硫酸厂沸腾炉排出的矿渣中含有Fe2O3、CuO、CuSO4(由CuO与SO3 在
沸腾炉中化合而成),其中硫酸铜的质量分数随沸腾炉温度不同而变化(见下表)
沸腾炉温度/℃ | 600 | 620 | 640 | 660 |
炉渣中CuSO4的质量分数/% | 9.3 | 9.2 | 9.0 | 8.4 |
已知CuSO4 在低于660℃时不会分解,请简要分析上表中CuSO4的质量分数随
温度升高而降低的原因 。
(6)在硫酸工业尾气中,SO2是主要大气污染物,必须进行净化处理,处理方
法可用 (填名称)吸收,然后再用硫酸处理,重新生成SO2和一种生产
水泥的辅料,写出这两步反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测3 题型:简答题
工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁[Fe(OH)SO4]的工艺流程如下: 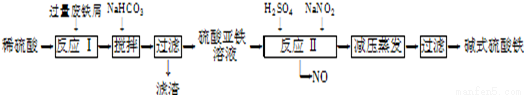
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
开始沉淀 | 2.3 | 7.5 | 3.4 |
完全沉淀 | 3.2 | 9.7 | 4.4 |
回答下列问题:
(1)加入过量废铁屑的目的是 ;加入少量NaHCO3的目的是调节pH,使溶液中的
(填“Fe3+”“Fe2+”或“Al3+”)沉淀,该工艺中“搅拌”的作用是 。
(2)在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,O2与NaNO2在反应中均作 ,若参与反应的O2有11.2L(标准状况),则相当(3)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,可部分水解生成
Fe2(OH)42+ 聚合离子.该水解反应的离子方程式为 。
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁.根据我国质量标准,产品中不得含有Fe2+及NO3-,为检验所得产品中是否含有Fe2+,应使用的试剂为 。(填字母)。
A.氯水 B.KSCN溶液 C.NaOH溶液 D.酸性KMnO4溶液
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测2 题型:实验题
如图是一个制取氯气并以氯气为原料进行特定反应的装置。
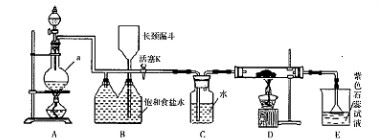
(l)A是氯气发生装置,写出其中的化学反应方程式 。
(2)a仪器的名称为 。
(3)实验开始时,先点燃A处的酒精灯,打开活塞K,让 氯气充满整个装置,再点燃D处酒精灯,连接上E装置。D装置的硬质玻璃管内盛有炭粉,反应产物为CO2和HC1。写出D中反应的化学方程式 ,装置C的作用是 。
氯气充满整个装置,再点燃D处酒精灯,连接上E装置。D装置的硬质玻璃管内盛有炭粉,反应产物为CO2和HC1。写出D中反应的化学方程式 ,装置C的作用是 。
(4)在E处,若漏斗内气体带有黄绿色,则紫色石蕊试液的颜色变化为 。
(5)若将E处烧杯中溶液改为澄清石灰水,反应过程中现象为 (填序号)。
①有白色沉淀生成;②无白色沉淀生成;③先生成白色沉淀,而后白色沉淀消失。
(6)D处反应完毕后,关闭活塞K,移去酒精灯,由于余热的作用,A处仍有Cl2
产生,则装置B中的现象是 ;若发现装置B中该现象不明显,可能的
原因是 ;查找原因时可用肥皂水或湿润的碘化钾淀粉试纸等,若用蘸
有浓氨水的玻璃棒检查时观察到有白烟产生,写出该氧化还原反应的化学方程
式 。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测2 题型:选择题
对可逆反应N2(g)+3H2(g) 2NH3(g),△H=-92.4 kJ.mol-1下列叙
2NH3(g),△H=-92.4 kJ.mol-1下列叙
述正确的是
A.达到化学平衡时,若升高温度,则正反应速率减小,逆反应速率增大
B.若单位时间内消耗x mol N2,同时生成2x mol NH3,则反应达到平衡状态
C.若达到平衡时,共放出46.2kJ热量,则有l mo1NH3(g)生成
D.达到平衡后,将容器体积减小为原来的一半,重新达到平衡后,c(NH3)变为原平衡时的2倍
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测17 题型:选择题
下列关于物质结构、性质的说法正确的是
A.因为酸性:HCl>H2CO3,所以非金属性:Cl>C
B.同一周期元素的原子,半径越小越容易失去电子
C.K的原子半径比Na的原子半径大,K与水反应比Na与水反应更剧烈
D.离子化合物中可能含有共价键,共价化合物中可能含有离子键
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测17 题型:选择题
甲、乙、丙是三种不含相同离子的可溶性电解质。它们所含的离子如下表所示
阳离子 | NH4+、Na+、Mg2+ |
阴离子 | OH-、 NO3-、SO42- |
取等质量的三种化合物配制相同体积的溶液,其物质的量浓度:c(甲)>c(乙)>c(丙),下列说法错误的是
A.甲中一定含Na+
B.乙中一定含NH4+
C.丙中一定含Mg2+
D.丙中一定含SO42-
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测16 题型:选择题
在日常生活中,我们经常看到铁制品生锈、铝制品表面出现白斑等众多的金属腐蚀现象。可以通过下列装置所示实验进行探究。下列说法正确的是
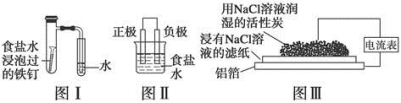
A.按图Ⅰ装置实验,为了更快更清晰地观察到液柱上升,可采用下列方法:用酒精灯加热具支试管
B.图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁
C.铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl-由活性炭区向铝箔表面区迁移,并发生电极反应:2Cl--2e-===Cl2↑
D.图Ⅲ装置的总反应为4Al+3O2+6H2O===4Al(OH)3,生成的Al(OH)3进一步脱水形成白斑
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测14 题型:推断题
【化学与技术】
下图是某企业设计的硫酸—磷肥—水泥联产、海水—淡水多用、盐—热—电联产的三大生态产业链流程图。
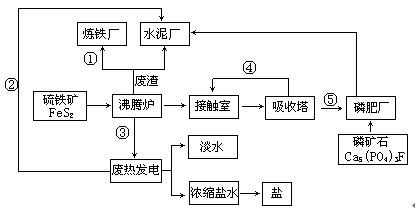
根据上述产业流程回答下列问题:
(1)该流程①、②、③、④、⑤为能量或物质的输送,请分别写出输送的主要物质的化学式或能量形式:① 、② 、③ 、④ 、⑤ 。
(2)沸腾炉发生反应的化学方程式 。磷肥厂的主要产品是普钙(磷酸二氢钙和硫酸钙),写出由磷矿石和硫酸反应制普钙得化学方程式 。
(3)用1吨硫铁矿(FeS2的质量分数为36%)接触法制硫酸,制硫酸的产率为65%,则最后能生产出质量分数为98%的硫酸 吨。
(4)热电厂的冷却水是 ,该流程中浓缩盐水除提取盐以外还可提取的物质有 (写出一种即可)。
(5)根据现代化工厂设计理念请提出高炉炼铁厂废气、废渣及多余热能的利用设想。 , (写出两点即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com