
【题目】下列实验操作中,先后顺序正确的是
A.稀释浓硫酸时,先在烧杯中加入一定体积的浓硫酸,后注入蒸馏水
B.酸碱中和滴定时,锥形瓶先用标准液洗涤后,再注入待测液
C.在制取干燥纯净的氯气时,先使氯气通过饱和食盐水,后通过浓硫酸
D.为检验酸性溶液中的![]() 和
和![]() ,先加硝酸银溶液,滤去沉淀后加硝酸钡溶液
,先加硝酸银溶液,滤去沉淀后加硝酸钡溶液
【答案】C
【解析】
![]() 稀释浓硫酸时,要考虑浓硫酸的物理性质,密度比水大,易溶于水,溶于水时放出大量的热,如果把水倒入浓硫酸中,水会浮在上面,放出的热足以使水沸腾,从而造成液滴飞溅,导致事故发生,所以稀释时一定要把浓硫酸慢慢倒入水中,并用玻璃棒不断搅拌,故A错误;
稀释浓硫酸时,要考虑浓硫酸的物理性质,密度比水大,易溶于水,溶于水时放出大量的热,如果把水倒入浓硫酸中,水会浮在上面,放出的热足以使水沸腾,从而造成液滴飞溅,导致事故发生,所以稀释时一定要把浓硫酸慢慢倒入水中,并用玻璃棒不断搅拌,故A错误;
B.锥形瓶先用标准液洗涤后,再注入待测液,物质的量增大,测定结果偏高,故B错误;
C.实验室是利用二氧化锰和浓盐酸加热反应生成氯气,![]() 浓
浓![]() ,浓盐酸易挥发,所以制取的氯气中含有氯化氢,因在溶液中制取,所以制取的氯气中含有水蒸气,氯化氢极易溶于水,氯气能溶于水,且与水反应,
,浓盐酸易挥发,所以制取的氯气中含有氯化氢,因在溶液中制取,所以制取的氯气中含有水蒸气,氯化氢极易溶于水,氯气能溶于水,且与水反应,![]() ,食盐水溶液中的氯离子抑制氯气的溶解,降低氯气的溶解度,所以可用饱和的食盐水洗去氯气中的氯化氢;浓硫酸有吸水性,且不和氯气反应,所以可用浓硫酸干燥氯气,故C正确;
,食盐水溶液中的氯离子抑制氯气的溶解,降低氯气的溶解度,所以可用饱和的食盐水洗去氯气中的氯化氢;浓硫酸有吸水性,且不和氯气反应,所以可用浓硫酸干燥氯气,故C正确;
D.检验酸性溶液中的![]() 和
和![]() ,若先加入
,若先加入![]() 溶液,生成的白色沉淀不能确定一定就是AgCl,也可能是
溶液,生成的白色沉淀不能确定一定就是AgCl,也可能是![]() ,即不能先检验
,即不能先检验![]() ;应该先加入足量的硝酸钡溶液,会和硫酸钠反应生成硫酸钡白色沉淀,该化学反应为
;应该先加入足量的硝酸钡溶液,会和硫酸钠反应生成硫酸钡白色沉淀,该化学反应为![]() ,过滤滤液中再加入硝酸银,则会和氯化钠反应生成氯化银沉淀,该化学反应为
,过滤滤液中再加入硝酸银,则会和氯化钠反应生成氯化银沉淀,该化学反应为![]() ,故D错误;
,故D错误;
故选C


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案科目:高中化学 来源: 题型:
【题目】某学习小组的同学根据“侯氏制碱法”的原理:
①NH3+H2O+CO2+NaCl===NaHCO3↓+NH4Cl
②2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
利用如下实验装置制备Na2CO3。
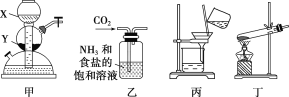
下列叙述正确的是( )
A.若X为稀硫酸,Y为碳酸钙,则可用装置甲制取CO2
B.装置乙中会有白色沉淀析出
C.将装置丙中所得滤液蒸干可得到NH4Cl固体
D.用装置丁加热NaHCO3固体可制得Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以乙醇、浓硫酸、液溴为原料制备1,2-二溴乙烷的装置如下图所示

1,2二溴乙烷和液溴的主要物理性质如下:
物质 | 熔点/℃ | 沸点/℃ | 密度/(g·cm-3) | 溶解性 |
1,2-二溴乙烷 | 9.79 | 131.4 | 2.18 | 难溶于水,易溶于醇、醚等 |
液溴 | -7.2 | 58.78 | 3.12 | 微溶于水,能溶于醇、醚等 |
(1)装置A中反应的化学方程式是________;装置D试管中反应的化学方程是________;
(2)装置B的作用是_____,装置C的作用是____。
(3)设计实验分离出1,2-二溴乙烷的操作步骤为:a.将反应后D中试管内的液体倒入仪器甲中,然后再注入适量试剂X;b.充分振荡,静置,使其分层。
①仪器甲是______(填名称);
②试剂X是______;
A.水 B.乙醇 C.四氯化碳 D.NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是.![]()
A.在盛有硫酸亚铁铵溶液的试管中,滴加几滴新制氯水,无明显现象,然后滴加KSCN溶液,若观察到溶液变为血红色,则说明硫酸亚铁铵中含有![]()
B.测量某溶液的pH,pH试纸一旦用水湿润,一定会产生实验误差
C.灼烧海带可以在坩埚中进行,也可以在蒸发皿中进行
D.实验室用已知浓度的醋酸溶液滴定未知浓度的氢氧化钠溶液时,选用酚酞做指示剂比用甲基橙做指示剂时带来的误差要小一点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种熔融碳酸盐燃料电池原理示意图如下。下列有关该电池的说法正确的是( )
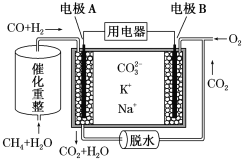
A.电池工作时,CO32-向电极B移动
B.电极B上发生的电极反应为O2+2CO2+4e-=2 CO32-
C.电极A上H2参与的电极反应为H2+2OH--2e-=2H2O
D.反应CH4+H2O 3H2+CO,每消耗1 mol CH4转移12 mol电子
3H2+CO,每消耗1 mol CH4转移12 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质常温下发生水解,对应的离子方程式正确的是
A.Na2CO3:CO32-+2H2O![]() H2O+CO2↑+2OH-
H2O+CO2↑+2OH-
B.NH4Cl:NH4++H2O![]() NH3·H2O+OH-
NH3·H2O+OH-
C.CuSO4:Cu2++2H2O![]() Cu(OH)2+2H+
Cu(OH)2+2H+
D.NaF:F-+H2O=HF+OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是



甲 乙 丙
A. 图甲中纯水仅升高温度,就可以从a点变到c点
B. 图甲中在b点对应温度下,将pH=2的H2SO4溶液与pH=10的NaOH溶液等体积混合后,溶液显中性
C. 图乙表相同温度下pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强
D. 用0.0100mol/L硝酸银标准溶液,滴定浓度均为0.1000mol/L,C1-、Br-及I-的混合溶液,由图丙曲线,可确定首先沉淀的是Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应2SO2(g)+O2(g)![]() 2SO3(g)是硫酸制造工业的基本反应。将0.050 mol SO2(g)和0.030mol O2(g)注入体积为1.0L的密闭反应器,并置于某较高温度下的恒温环境中,达化学平衡后,测得反应器中有0.040 mol SO3(g),求该温度下反应的平衡常数及SO2、O2的平衡转化率________。
2SO3(g)是硫酸制造工业的基本反应。将0.050 mol SO2(g)和0.030mol O2(g)注入体积为1.0L的密闭反应器,并置于某较高温度下的恒温环境中,达化学平衡后,测得反应器中有0.040 mol SO3(g),求该温度下反应的平衡常数及SO2、O2的平衡转化率________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钡在氧气中燃烧时得到一种钡的氧化物晶体,结构如图所示,有关说法正确的是
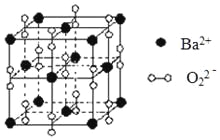
A.与每个Ba2+距离相等且最近的Ba2+共有6个
B.晶体中Ba2+的配位数为8
C.晶体的化学式为Ba2O2
D.该氧化物是含有非极性键的离子化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com