
【题目】某学习小组的同学根据“侯氏制碱法”的原理:
①NH3+H2O+CO2+NaCl===NaHCO3↓+NH4Cl
②2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
利用如下实验装置制备Na2CO3。
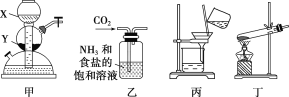
下列叙述正确的是( )
A.若X为稀硫酸,Y为碳酸钙,则可用装置甲制取CO2
B.装置乙中会有白色沉淀析出
C.将装置丙中所得滤液蒸干可得到NH4Cl固体
D.用装置丁加热NaHCO3固体可制得Na2CO3
科目:高中化学 来源: 题型:
【题目】若将等物质的量的CO和H2混合气体充入恒温恒容密闭容器中进行反应:CO(g)+2H2(g)![]() CH3OH(g),下列事实能说明此反应已达到平衡状态的是( )
CH3OH(g),下列事实能说明此反应已达到平衡状态的是( )
A.容器内气体密度保持不变
B.用CO、H2、CH3OH表示反应的速率之比为1:2:1
C.单位时间内生成nmolCO的同时生成2nmolH2
D.混合气体的平均相对分子质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.2mol/L的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,下列叙述正确的是( )

A. A曲线表明原NaOH溶液中通入CO2后,所得溶液中的溶质成分是Na2CO3和NaHCO3
B. B曲线中消耗盐酸0<v(HCl)<25mL时发生的离子反应为:OH-+H+=H2O H++CO32-=HCO3-
C. B曲线表明原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为224mL
D. 原NaOH溶液的物质的量浓度为1.0mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A.H2SO4溶液与氢氧化钠反应:OH-+H+=H2O
B.铝与NaOH溶液反应:Al+2OH-= ![]() +H2↑
+H2↑
C.AlCl3溶液与氨水反应:AlCl3+3OH-=Al(OH)3↓+3Cl-
D.Cl2与氢氧化钠溶液反应:Cl2+2OH-=2ClO-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】针对下列实验现象表述不正确的是
A. 用同一针筒先后抽取80 mL氯气、20 mL水,振荡,气体完全溶解,溶液变为黄绿色
B. 在表面皿中加入少量胆矾,再加入3 mL浓硫酸,搅拌,固体由蓝色变白色
C. 向二氧化硫水溶液中滴加氯化钡溶液,再滴加双氧水,产生白色沉淀
D. 将点燃后的镁条伸入充满二氧化碳的集气瓶,镁条剧烈燃烧,有白色、黑色固体生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们对苯的认识有一个不断深化的过程。已知分子式为 C6H6的结构有多种,其中的两种为:
Ⅰ.![]() Ⅱ.
Ⅱ.
(1)这两种结构的化学性质区别表现在:Ⅰ不能____(填字母,下同),而Ⅱ能____。
A.被酸性KMnO4溶液氧化
B.与溴水发生加成反应
C.与氢气发生加成反应
(2)已知Ⅰ结构下,该物质能在一定条件下与液溴反应,其反应方程式为________________。
(3)今发现C6H6还可能有另一种如下图所示的立体结构,该结构的四氯代物有______种。
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年科学家提出“绿色自由”构想。把含有大量![]() 的空气吹入
的空气吹入![]() 溶液中,再把
溶液中,再把![]() 从溶液中提取出来,并使之与
从溶液中提取出来,并使之与![]() 反应生成可再生能源甲醇。其工艺流程如图所示:
反应生成可再生能源甲醇。其工艺流程如图所示:

(1)分解池中主要物质是______;
(2)在合成塔中,若有![]() 与足量
与足量![]() 恰好完全反应,生成气态的水和甲醇,可放出5370kJ的热量,写出该反应的热化学方程式______;
恰好完全反应,生成气态的水和甲醇,可放出5370kJ的热量,写出该反应的热化学方程式______;
(3)该工艺在那些方面体现了“绿色自由”构想中的“绿色”______。(答二条)
(4)一定条件下,向2L恒容密闭容器中充入1mol![]() 和3mol
和3mol![]() ,在不同催化剂作用下发生反应I、反应II与反应III,相同时间内
,在不同催化剂作用下发生反应I、反应II与反应III,相同时间内![]() 的转化率随温度变化如图所示:
的转化率随温度变化如图所示:

![]() 图中c点的转化率为
图中c点的转化率为![]() ,即转化了
,即转化了![]()
①催化剂效果最佳的反应是______ (填“反应I”,“反应II”,“反应III”)。
②b点v (正)______ v (逆)(填“>”,“<”,“=”)。
③若此反应在a点时已达平衡状态,a点的转化率比c点高的原因是______。
④c点时该反应的平衡常数K=______。
⑤一定条件下,向2L恒容密闭的上述容器中再充入1mol![]() 和3mol
和3mol![]() ,达到新的化学平衡后,
,达到新的化学平衡后,![]() 的浓度较原平衡浓度______
的浓度较原平衡浓度______![]() 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变”![]() 。
。
(5)科学家还研究了其它转化温室气体的方法,利用图所示装置可以将![]() 转化为气体燃料
转化为气体燃料![]() 该装置工作时,N电极的电极反应式为______。
该装置工作时,N电极的电极反应式为______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应A(g)+ 4B(g)![]() C(g)+ D(g),在四种不同情况下的反应速率如下,其中反应进行得最快的是( )
C(g)+ D(g),在四种不同情况下的反应速率如下,其中反应进行得最快的是( )
A. vA=0.15mol/(L·min) B. vB=0.6 mol/(L·min)
C. vC=0.4 mol/(L·min) D. vD=0.01 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中,先后顺序正确的是
A.稀释浓硫酸时,先在烧杯中加入一定体积的浓硫酸,后注入蒸馏水
B.酸碱中和滴定时,锥形瓶先用标准液洗涤后,再注入待测液
C.在制取干燥纯净的氯气时,先使氯气通过饱和食盐水,后通过浓硫酸
D.为检验酸性溶液中的![]() 和
和![]() ,先加硝酸银溶液,滤去沉淀后加硝酸钡溶液
,先加硝酸银溶液,滤去沉淀后加硝酸钡溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com