
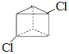
����Ŀ�����ǶԱ�����ʶ��һ��������Ĺ��̡���֪����ʽΪ C6H6�Ľṹ�ж��֣����е�����Ϊ��
��.![]() ��.
��.
(1)�����ֽṹ�Ļ�ѧ������������ڣ�������____(����ĸ����ͬ)��������____��
A��������KMnO4��Һ����
B������ˮ�����ӳɷ�Ӧ
C�������������ӳɷ�Ӧ
(2)��֪���ṹ�£�����������һ����������Һ�巴Ӧ���䷴Ӧ����ʽΪ________________��
(3)����C6H6����������һ������ͼ��ʾ������ṹ���ýṹ�����ȴ�����______�֡�
![]()
���𰸡�AB ABC ![]() +Br2
+Br2 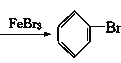 +HBr 3
+HBr 3
��������
(1)���ṹ�У�����̼ԭ�Ӽ䲻����̼̼˫�������Բ�����ϩ�������ʣ�������ܱ�����KMnO4��Һ����������ˮ���ܷ����ӳɷ�Ӧ�������������������ӳɷ�Ӧ��
�����ṹ�к���̼̼˫���������ܱ�����KMnO4��Һ����������ˮ�ܷ����ӳɷ�Ӧ���������������ӳɷ�Ӧ��
(2)���ṹ�£�����������һ����������Һ�巴Ӧ��������ֻ��һ����ԭ���ܱ���ԭ��ȡ����ͬʱ�����廯�⣻
(3)C6H6����������һ������ͼ��ʾ������ṹ����Ϊ����̼ԭ�ӹ�����������ԭ�ӣ��������ȴ����������ڶ��ȴ�������࣬�ɴ�����������ԭ�ӵ�����̼ԭ�Ӽ�ľ��뿼�ǡ�
![]()
(1)���ṹ�У�����̼ԭ�Ӽ䲻����̼̼˫�������Բ�����ϩ�������ʣ�������ܱ�����KMnO4��Һ����������ˮ���ܷ����ӳɷ�Ӧ�������������������ӳɷ�Ӧ����Ϊ��AB��
�����ṹ�к���̼̼˫���������ܱ�����KMnO4��Һ����������ˮ�ܷ����ӳɷ�Ӧ���������������ӳɷ�Ӧ����Ϊ��ABC��
(2)���ṹ�£�����������һ����������Һ�巴Ӧ��������ֻ��һ����ԭ���ܱ���ԭ��ȡ����ͬʱ�����廯�⣻��Ϊ��![]() +Br2
+Br2 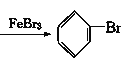 +HBr��
+HBr��
(3)��Ϊ����̼ԭ�ӹ�����������ԭ�ӣ��������ȴ����������ڶ��ȴ�������࣬�ɴ˿ɵó�����ȴ���Ľṹ��ʽ����Ϊ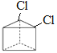 ��
��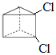 ��
�� ���֣���Ϊ��3��
���֣���Ϊ��3��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������(H2N2O2)��һ�ֶ�Ԫ�ᣬ��������N2O���塣
��1�������������е�Ԫ�صĻ��ϼ�Ϊ_____________________��
��2�������£���0��01mol��L-1��NaOH��Һ�ζ�10mL0��01mol��L-1��H2N2O2��Һ�������ҺpH��NaOH��Һ����Ĺ�ϵ��ͼ��ʾ��
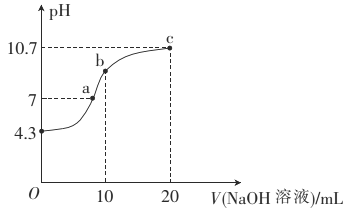
��д��H2N2O2��ˮ��Һ�еĵ��뷽��ʽ��______________��
��b��ʱ��Һ��c(H2N2O2)_____�������������������� ����������ͬ��c(N2O22-)��
��a��ʱ��Һ��c(Na+)____c(HN2O2-)+c(N2O22-)��
��3����������Һ����������������Һ��ϣ����Եõ���ɫ����������������������÷�ɢϵ�еμ���������Һ������ɫ�����ͻ�ɫ��������ʱ����ɢϵ��![]() =______��[��֪Ksp(Ag2N2O2)=4��2��10-9��Ksp(Ag2SO4)=1��4��10-5]
=______��[��֪Ksp(Ag2N2O2)=4��2��10-9��Ksp(Ag2SO4)=1��4��10-5]
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���10 mL 0.1 mol��L��1 CuCl2��Һ�еμ�0.1 mol��L��1��Na2S��Һ���μӹ�������Һ�У�lgc(Cu2��)��Na2S��Һ���(V)�Ĺ�ϵ��ͼ��ʾ�������й�˵����ȷ���ǣ� ��(��֪��Ksp(ZnS)��3��10��25)

A.a��b��c�����У�ˮ�ĵ���̶�����Ϊb��
B.Na2S��Һ�ʼ��Ե�ԭ�� S2����2H2O![]() H2S+ 2OH��
H2S+ 2OH��
C.a��b��c�����У� b����Һ��S2������С
D.��100 mL Zn2����Cu2��Ũ�Ⱦ�Ϊ10��5mol��L��1�Ļ����Һ����μ���10��4 mol��L��1��Na2S��Һ��Cu2���ȳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦFe��Fe2(SO4)3��3FeSO4�������仯������ͼ��ʾ��

(1)�÷�ӦΪ_____(��������������������)��Ӧ��
(2)��Ҫʹ�÷�Ӧ�ķ�Ӧ���ʼӿ죬���д�ʩ���е���_____(����ĸ)��
A.����ƬΪ���� B.�����¶� C.��Сѹǿ D.����������Na2SO4����
(3)����������Ӧ��Ƴ�ԭ��أ���ͭΪ��ԭ��ص�ijһ�缫���ϣ���ͭΪ____(����������������)����Fe�缫�Ϸ����ĵ缫��ӦΪ_____����Һ�е���������______(����������������)���ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС���ͬѧ�����������Ƽ����ԭ����
��NH3��H2O��CO2��NaCl===NaHCO3����NH4Cl
��2NaHCO3![]() Na2CO3��H2O��CO2��
Na2CO3��H2O��CO2��
��������ʵ��װ���Ʊ�Na2CO3��
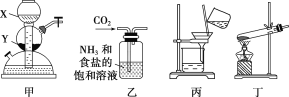
����������ȷ����(����)
A.��XΪϡ���ᣬYΪ̼��ƣ������װ�ü���ȡCO2
B.װ�����л��а�ɫ��������
C.��װ�ñ���������Һ���ɿɵõ�NH4Cl����
D.��װ�ö�����NaHCO3������Ƶ�Na2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йؽ�����ұ���У���ȷ����:
A.�Ժ�ˮΪԭ���Ƶþ��Σ��ٵ�⾫�ε�ˮ��Һ��ȡ��
B.�ú�ˮ��ʯ�����Ϊԭ�ϣ���һϵ�й����Ƶ�����þ����H2��ԭ����þ�Ƶ�þ
C.������ʯ����̿��������Ϊԭ�ϣ�ͨ����Ӧ������CO�ڸ����»�ԭ����ʯ�Ƶ���
D.�����ȷ���ԭMnO2��Cr2O3���Ƶý�����1mol�����������ٵ���MnO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
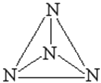
����Ŀ���������ѧ�һ���˼����о���ֵ��![]() ���ӽṹ��ͼ��ʾ
���ӽṹ��ͼ��ʾ![]() �������й����ʽṹ��˵����ȷ���ǣ� ��
�������й����ʽṹ��˵����ȷ���ǣ� ��
A.N������![]() �ӻ���
�ӻ���![]() ��Ϊ
��Ϊ![]() ��
��
B.N�ĵ縺�Դ���O������![]() �ķе����
�ķе����![]()
C.![]() Ϊԭ�Ӿ��壬ÿ��N����λ��Ϊ3
Ϊԭ�Ӿ��壬ÿ��N����λ��Ϊ3
D.Nԭ�Ӻ�����5��δ�ɶԵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ҫ��MgO��SiO2��ɣ�����������Fe2O3��FeO��Al2O3�����ʡ�����������������þ�Ĺ���������ͼ��ʾ��
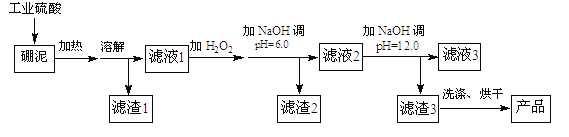
��֪ijЩ�������������PH���±���ʾ��
�������� | ��ʼ����ʱ��pH | ��ȫ����ʱ��pH |
Mg(OH)2 | 9.3 | 10.8 |
Fe(OH)2 | 7.6 | 9.6 |
Fe(OH)3 | 2.7 | 3.7 |
Al(OH)3 | 3.7 | 4.7 |
��1��MgO�ĵ���ʽΪ____��
��2������2����Ҫ�ɷ��� ____��������2�м������������NaOH��Һ�����������ӷ���ʽΪ______��
��3������NaOH����pH=12.0ʱ�����������ӷ���ʽΪ___________��
��4������Mg(OH)2�뺬SO2��������Ӧ����MgSO4������ʹ�������÷�Ӧ�Ļ�ѧ����ʽΪ______��
��5����ȡa������Ϊԭ�ϣ����õ�b��Mg(OH)2��Ʒ����������������þԪ������ʧ������������MgO����������Ϊ__���ú���a��b�Ĵ���ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����ʳ����·���ˮ�⣬��Ӧ�����ӷ���ʽ��ȷ����
A.Na2CO3��CO32����2H2O![]() H2O��CO2����2OH��
H2O��CO2����2OH��
B.NH4Cl��NH4����H2O![]() NH3��H2O��OH��
NH3��H2O��OH��
C.CuSO4��Cu2����2H2O![]() Cu(OH)2��2H��
Cu(OH)2��2H��
D.NaF��F����H2O��HF��OH��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com