
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:
下列说法正确的是( )
A.在常温、常压下,11.2 L N2含有的分子数为0.5NA
B.标准状况下,22 .4 L H2和O2的混合物所含分子数为NA
.4 L H2和O2的混合物所含分子数为NA
C.标准状况下,18 g H2O的体积是22.4 L
D.1 mol SO2的体积是22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
以下一些氧化物和单质之间可发生如图所示的反应:

其中,氧化物(Ⅰ)是红棕色固体、氧化物(Ⅱ)、(Ⅲ)、(Ⅳ)在反应条件下都是气体。
(1)氧化物(Ⅰ)的化学式(分子式)是________,氧化物(Ⅱ)的化学式(分子式)是________。
(2)反应①的化学方程式是________________ ,
反应②的化学方程式是________________,
反应③的化学方程式是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,当它们的体积比为3∶2∶1时,3种溶液中Cl-的物质的量之比为( )
A.1∶1∶1 B.1∶2∶3 C.3∶2∶1 D.3∶4∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
0.25 mol A的质量是16 g,A的相对分子质量(或相对原子质量)是( )
A.32 g·mol―1 B.64 g·mol―1 C.32 D.64
查看答案和解析>>
科目:高中化学 来源: 题型:
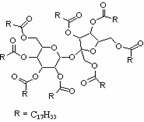
有一瘦身用的非天然油脂,其结构如下, 下列说法正确的是
A.该非天然油脂属于高级脂肪酸的甘油酯
B.该非天然油脂与氢氧化钠溶液共热,其水解产物不与溴水反应
C.该非天然油脂为高分子化合物
D.该非天然油脂在稀硫酸的作用下水解最终生成三种有机化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
过氧化钙可以用于改善地表水质,处理含重金属粒子废水和治理赤潮,也可用于应急供氧等。工业上生产过氧化钙的主要流程如下:
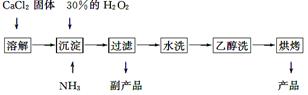
已知CaO2·8H2O呈白色,微溶于水,加热至350 ℃左右开始分解放出氧气。
(1)用上述方法制取CaO2·8H2O的化学方程式是______________________________;
(2)检验“水洗”是否合格的方法是___________________________________________;
(3)沉淀时常用冰水控制温度在0 ℃左右,其可能原因是______________________;
(4)测定产品中CaO2的含量的实验步骤:
第一步:准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2 mol·L-1的H2SO4溶液,充分反应。
第二步:向上述锥形瓶中加入几滴淀粉溶液。高 考 资 源 网
第三步:逐滴加入浓度为c mol·L-1的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液V mL。
【已知:I2+2S2O32-=2I-+S4O62-】
①第一步发生的反应的化学方程式为 ;
CaO2的质量分数为____________(用字母表示);
②某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的CaO2的质量分数可能________(填“不受影响”、“偏低”或“偏高”),原因是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列可用来鉴别SO2和CO2气体的试剂有
①澄清石灰水②氢硫酸③氯水④酸性高锰酸钾⑤硝酸钡溶液⑥紫色石蕊试液⑦品红溶液
A.②③④⑤⑦ B.①④⑤⑥⑦ C.①②③⑥⑦ D.②③④⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极)。已知:铅蓄电池在放电时发生下列电极反应:负极Pb+SO
如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极)。已知:铅蓄电池在放电时发生下列电极反应:负极Pb+SO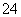 -2e-===PbSO4
-2e-===PbSO4
正极PbO2+4H++SO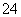 +2e-===PbSO4+2H2O
+2e-===PbSO4+2H2O
(1)请写出电解饱和食盐水的化学方程式__ ▲ __ 。
(2)若在电解池中C极一侧滴酚酞试液,电解一段时间后未呈红色,说明铅蓄电池的A极为 ▲ __极。
(3)用铅蓄电池电解1L饱和食盐水(食盐水足量、密度为1. 15 g/cm3)时,
①若铅蓄电池消耗H2SO42mol,则可收集到H2的体积(标准状况下)为 ▲ __ L。
②若消耗硫酸amol,电解后除去隔膜,所得溶液中NaOH的质量分数表达式为(假设氯气全部排出) ▲ __ (用含a的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com