
【题目】下表是实验室制备气体的有关内容:
编号 | 实验内容 | 实验原理 | 发生装置 |
① | 制氧气 | H2O2→O2 | |
② | 制氨气 | NH4Cl→NH3 | |
③ | 制氯气 | HCl→Cl2 |
(1)上述气体中:从制备过程看,必须选择合适的氧化剂才能实现的是______________(填气体的化学式,下同);从反应中有无电子转移的角度看,明显不同于其他气体的是___________,写出实验室制取该气体的化学方程式
(2)根据表中所列实验原理,从下列装置中选择合适的发生装置,将其编号填入上表的空格中。

(3) 若用上述制备O2的装置制备NH3,则选择的试剂为____________________。
(4) 制备Cl2需用8 mol/L的盐酸100mL,现用12 mol/L的盐酸来配制。
①需要12 mol/L的盐酸的体积为 mL(精确到0.1 mL)
②在容量瓶的使用方法中,下列操作不正确的是 (填写标号)。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时用量筒量取浓盐酸后用玻璃棒引流入容量瓶中,缓慢加入蒸馏水到接近标线1cm~2cm处,用胶头滴管滴加蒸馏水直到凹液面的最低处和标线相平
D.定容后盖好瓶塞,用食指顶住,用另一只手手指托住瓶底,把容量瓶倒转和摇动多次
【答案】(1) Cl2 ;NH3 ;Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
(2) ① C ② B ③A或C
(3) 浓氨水和氢氧化钠(或生石灰等)
(4) ①66.7 ②BC
【解析】
试题分析:(1)H2O2→O2发生自身氧化还原反应;NH4Cl→NH3发生非氧化还原反应;HCl→Cl2氯元素被氧化,必须选择合适的氧化剂才能实现。明显不同于其他气体的是氨气,写出实验室制取氨气的化学方程式Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O。(2)①用过氧化氢制取氧气,属于固液不加热型,选C装置;②NH4Cl→NH3属于固体加热型,选B装置;③HCl→Cl2,若用浓盐酸与二氧化锰需要加热制取氯气,选择A装置。若用浓盐酸与高锰酸钾制取氯气,不需要加热,选择C装置;(3) (3) 装置C是固液不加热制取气体的装置,若C装置制备NH3,则选择的试剂为浓氨水和氢氧化钠;(4) ①根据稀释前后溶质物质的量不变,8mol/L×0.1L=12mol/L×VL,V=0.0667L;②使用容量瓶前要检查它是否漏水,A正确;容量瓶用蒸馏水洗净后,不能再用待配溶液润洗,B错误;配制溶液时用量筒量取浓盐酸后,在烧杯中稀释,再用玻璃棒引流入容量瓶中,缓慢加入蒸馏水到接近标线1cm~2cm处,用胶头滴管滴加蒸馏水直到凹液面的最低处和标线相平,故C错误;定容后盖好瓶塞,用食指顶住,用另一只手手指托住瓶底,把容量瓶倒转和摇动多次,故D正确。
CaCl2+2NH3↑+2H2O。(2)①用过氧化氢制取氧气,属于固液不加热型,选C装置;②NH4Cl→NH3属于固体加热型,选B装置;③HCl→Cl2,若用浓盐酸与二氧化锰需要加热制取氯气,选择A装置。若用浓盐酸与高锰酸钾制取氯气,不需要加热,选择C装置;(3) (3) 装置C是固液不加热制取气体的装置,若C装置制备NH3,则选择的试剂为浓氨水和氢氧化钠;(4) ①根据稀释前后溶质物质的量不变,8mol/L×0.1L=12mol/L×VL,V=0.0667L;②使用容量瓶前要检查它是否漏水,A正确;容量瓶用蒸馏水洗净后,不能再用待配溶液润洗,B错误;配制溶液时用量筒量取浓盐酸后,在烧杯中稀释,再用玻璃棒引流入容量瓶中,缓慢加入蒸馏水到接近标线1cm~2cm处,用胶头滴管滴加蒸馏水直到凹液面的最低处和标线相平,故C错误;定容后盖好瓶塞,用食指顶住,用另一只手手指托住瓶底,把容量瓶倒转和摇动多次,故D正确。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】1mol某烃能与2mol HCl加成,加成后产物上的氢原子最多能被8mol Cl2取代,则该烃可能为
A.乙炔 B.乙烯
C.苯 D.1,3-丁二烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A. 可以用溴水鉴别丙烯和苯
B. 用无水硫酸铜可以检验酒精中是否含有水
C. 可以用氢氧化钠溶液鉴别乙醇和乙酸
D. 可以用烧灼的方法鉴别真丝布料和纯棉布料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色透明溶液中,能大量共存的离子组是 :( )
A.Na、K+、SO42-、HCO3
B.Cu 2+、K+、SO42-、NO3-
C.NH4+、K+、Cl-、OH
D.Fe3+、K+、SCN-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活息息相关,下列说法正确的是( )
A.我国居民传统膳食以糖类为主,淀粉、脂肪都是糖类物质
B.人体内的蛋白质不断分解,最终生成水和二氧化碳排出体外
C.长期烧水的水壶内壁容易形成一层水垢,可以用食醋除去
D.明矾净水时发生了化学及物理变化,能起到杀菌、消毒的作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲配制480mL0.5mol·L-1的NaOH溶液,试回答下列问题。
(1)计算:需要NaOH固体的质量为___________。
(2)假定最终称量小烧杯的质量为____________(填“32.6g”或“32.61g”)。
在标尺(图)上画出游码位置(画“△”表示)。
![]()
(3)某学生实际配制的NaOH溶液的浓度为0.51mol·L-1,原因可能是________。
A.使用滤纸称量NaOH固体 |
B.容量瓶中原来存有少量水 |
C.溶解后的烧杯未经多次洗涤 |
D.用胶头滴管加水定容时俯视刻度 |
E.加水时超过刻度线,用胶头滴管吸出
F.转移溶液时未经冷却
(4)假设该同学成功配制了0.400mol·L-1的盐酸,他又用该盐酸中和含100 mL的NaOH溶液,则该同学需取________mL盐酸。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】里用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4·H2O),过程如下:
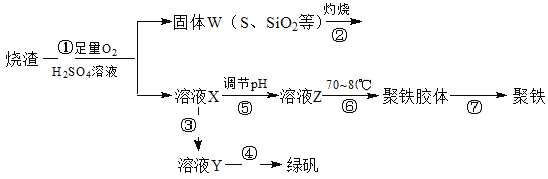
请回答下列问题:
(1)写出过程①中FeS和O2、H2SO4反应的化学方程式:___________________。
(2)将过程②中产生的气体通入下列溶液中,溶液会褪色的是_________。
A.品红溶液 B.紫色石蕊试液 C.酸性高锰酸钾溶液 D.溴水
(3)过程③中,需要加入的物质是_______________(化学式)。
(4)过程④中,蒸发结晶需要使用酒精灯、三角架、泥三角,还需要的仪器有_____________。
(5)过程⑥中,将溶液Z加热到70~80℃,目的是:__________________________。
(6)检验X溶液中的金属阳离子,通常使用的试剂和现象是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 钛被称为继铁、铝之后的第三金属,制备金属钛的一种流程如下:
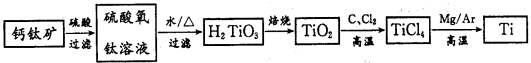
回答下列问题:
(1)已知TiCl4在通常情况下是无色液体,熔点为-37℃,沸点为136℃,可知TiCl4为___________晶体。
(2)钙钛矿晶体的结构如图所示。钛离子位于立方晶胞的角顶,被____个氧离子包围成配位八面体;钙离子位于立方晶胞的体心,被____个氧离子包围。
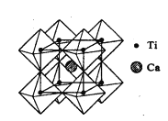
(3)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下:
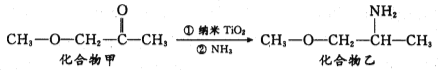
化合物甲中C原子的杂化方式为_______________;化合物乙的沸点明显高于化合物甲,主要原因是_______________________________。
II. 金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:
(4)镍元素在元素周期表中的位置为 。
(5)NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点NiO________FeO(填“<”或“>”);
(6)甲醛(H2C=O)在Ni催化作用下加氢可得甲醇(CH3OH)。甲醇分子内的O—C—H键角______(填“大于”“等于”或“小于”)甲醛分子内的O—C—H键角。
(7)Ni的氯化物与氨水反应可形成配合物[Ni(NH3)4]Cl2,2mol该配合物中含有σ键______mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com