
【题目】中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700℃时制造出纳米级金刚石粉末。该成果发表在世界权威的《科学》杂志上,立刻被科学家们高度评价为“稻草变黄金”。同学们对此有下列一些理解,其中错误的是
A. 制造过程中元素种类没有改变 B. CCl4是一种化合物
C. 这个反应是氧化还原反应 D. 金刚石属于金属单质
科目:高中化学 来源: 题型:
【题目】下列关于能量变化的说法正确的是
A. 冰融化成水放出热量
B. 金属与酸反应吸收能量
C. 生成物的总能量一定低于反应物的总能量
D. 化学键的断裂和形成是化学反应中能量变化的主要原因
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸异戊酯是组成蜜蜂信息素的成分之一,实验室制备乙酸异戊酯的反应装置示意图和有关数据如下:
![]()
相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 水中溶解度 | |
异戊醇 | 88 | 0.8123 | 131 | 微溶 |
乙 酸 | 60 | 1.0492 | 118 | 溶 |
乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |
实验步骤:在A中加入4.4 g的异戊醇,6.0 g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50分钟,反应液冷却至室温后,倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤,分液出来的产物加入少量无水硫酸镁固体,静置片刻,过滤除去硫酸镁固体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。回答下列问题:
(1)装置B的名称是:_____________________。
(2)在洗涤操作中,第一次水洗的主要目的是:_________________________;
第二次水洗的主要目的是:__________________________________________。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后________(填标号),
A.直接将乙酸异戊酯从分液漏斗上口倒出
B.直接将乙酸异戊酯从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口放出
(4)本实验中加入过量乙酸的目的是:___________________________。
(5)实验中加入少量无水硫酸镁的目的是:_________________________________。
(6)在蒸馏操作中,仪器选择及安装都正确的是:_____________(填标号)。
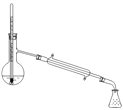

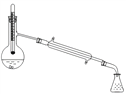
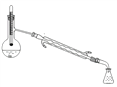
a b c d
(7)本实验的产率是:_________。
A.30 % B.40% C.50% D.60%
(8)在进行蒸馏操作时,若从130 ℃开始收集馏分,产率偏_________(填“高”或者“低”)。原因是___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在溶液中,反应A+2B![]() C分别在三种不同实验条件下进行,它们的起始状态均为c(A) = 0.100 mol·L-1 c(B) = 0.200 mol·L-1 、c(C) = 0 mol·L-1 。在三种条件下,反应物A的浓度随时间的变化如图所示。下列说法中正确的是
C分别在三种不同实验条件下进行,它们的起始状态均为c(A) = 0.100 mol·L-1 c(B) = 0.200 mol·L-1 、c(C) = 0 mol·L-1 。在三种条件下,反应物A的浓度随时间的变化如图所示。下列说法中正确的是

A. 反应的平衡常数:①<② B. 反应A+2B![]() C的△H >0
C的△H >0
C. 实验②平衡时B的转化率为60% D. 实验③平衡时c(C) = 0.04 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg-H2O2电池是一种化学电源,以Mg和石墨为电极,海水为电解质溶液,示意图如下。下列说法不正确的是

A. 石墨电极是该电池的正极
B. 石墨电极上发生还原反应
C. Mg电极的电极反应式:Mg-2e-=Mg2+
D. 电池工作时,电子从Mg电极经导线流向石墨电极,再从石墨电极经电解质溶液流向Mg电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,合成氨反应的热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g);△H=﹣92.4kJ/mol,在该温度下,取1mol N2和3mol H2放在密闭容器内反应.下列说法正确的是( )
2NH3(g);△H=﹣92.4kJ/mol,在该温度下,取1mol N2和3mol H2放在密闭容器内反应.下列说法正确的是( )
A. 在有催化剂存在的条件下,反应放出的热量为92.4 kJ
B. 有无催化剂该反应放出的热量都为92.4 kJ
C. 若再充入1 mol H2,到达平衡时放出的热量应为92.4 kJ
D. 反应放出的热量始终小于92.4 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A.FeCl2溶液中通入Cl2:Fe2++Cl2= Fe3++2Cl-
B.澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-= CaCO3↓+H2O
C.FeS固体放入稀硝酸溶液中:FeS+2H+= Fe2++H2S↑
D.AlCl3溶液中加入过量氨水:Al3++4OH-=AlO2-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水是人类生存和发展的宝贵自然资源。下列有关水资源保护的说法中,不正确的是( )
A.轧钢厂排出的含盐酸的废水,可用熟石灰中和处理
B.重金属离子对人体危害很大,可采用沉淀反应除之
C.化肥中含有植物营养素,可大量使用以改善水环境
D.近年来,采用二氧化氯.臭氧等用于饮水消毒
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com