
【题目】甲、乙、丙、丁、戊、己六种有机物的化学式如下表所示:
物质 | 甲 | 乙 | 丙 | 丁 | 戊 | 己 |
化学式 | CH4 | C2H4 | C3H8 | C4H8 | C2H6O | C2H4O2 |
下列与这些有机物有关的说法不正确的是
A. 甲、丙均不能使酸性高锰酸钾溶液褪色B. 丁的结构可能有5种(不考虑立体异构)
C. 等质量的乙、戊完全燃烧时耗氧量相等D. 己可能发生银镜反应而不发生水解反应
【答案】C
【解析】
A、考查有机物官能团的性质,甲和丙都属于烷烃,烷烃的化学性质相对稳定,不能使酸性高锰酸钾溶液、溴水褪色,故A说法正确;
B、本题考查同分异构体的判断,丁的化学式为C4H8,可能是单烯烃,也可能是环烷烃,如为单烯烃,可能结构简式为CH2=CHCH2CH3、CH3CH=CHCH3、CH2=C(CH3)2,如为环烷烃,可能的结构简式为 、
、![]() ,共有五种,故B说法正确;
,共有五种,故B说法正确;
C、考查有机物的燃烧,等质量时,烃转化成CHy/x,y/x越大,消耗氧量越多,含氧衍生物拆写成烃和H2O的形式,乙的化学式为C2H4,戊可以写成C2H4·H2O,相同质量,因此戊耗氧量小于乙,故C说法错误;
D、考查有机物同分异构体,己的化学式为C2H4O2,首先想到的是CH3COOH,题中能发生银镜反应,说明含有醛基,不发生水解,说明不含有酯基,因此结构简式可能为HOCH2CHO,故D说法正确。


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】如图甲是利用一种微生物将废水中的尿素[CO(NH2)2]的化学能直接转化为电能,并生成环境友好物质的装置,同时利用此装置的电能在铁上镀铜。下列说法中正确的是
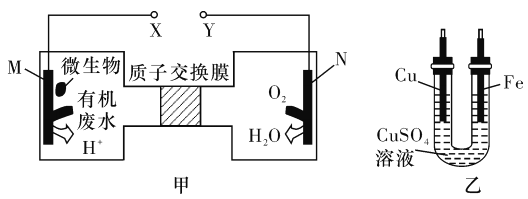
A. 铜电极应与X相连接
B. H+经过质子交换膜由右向左移动
C. 当N电极消耗0. 25 mol气体时,则铁电极增重16 g
D. M电极反应式:CO(NH2)2+H2O-6e- =CO2↑+N2↑+6H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
A.标准状况下,11.2L H2O含有的分子数为0.5NA
B.46g NO2和N2O4的混合物含有的原子数为3NA
C.20g NaOH固体溶于1L 水可制得0.5mol/L的NaOH溶液
D.同温同压下,体积相同的氢气和氩气所含的原子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示不同化学元素所组成的化合物,以下说法错误的是

A.若①为某种大分子的组成单位,则①最可能是氨基酸
B.若②是“生命的燃料”,则②可能是葡萄糖
C.若③为能携带遗传信息的大分子物质,则③一定是DNA
D.若④为参与动物血液中脂质运输的物质,则④可能为胆固醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】抗心律失常药物心律平的合成路线如下:

已知:① R-OH + Cl-R![]() R-O-R + HCl
R-O-R + HCl
②R-CHO+![]()
![]()
![]() + H2O
+ H2O
请回答:
(1)A属于链烃,则A中所含的官能团是______。
(2)B中无甲基,A→B的反应类型是______反应。
(3)C的结构简式是______。
(4)E中含有三元环,且无羟基,则D→E的化学方程式是______。
(5)结合官能团的性质,解释F→G的转化中需酸化的原因:______。
(6)H的结构简式是______。
(7)I→J的化学方程式是______。
(8)在I→J的反应中,生成J的同时会有副产物K,K与J互为同分异构体,则K的结构简式是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:p[c(HX)/c(X-)]=-lg[c(HX)/c(X-)]。室温下,向0. 10 mol/LHX溶液中滴加0.10 mol/L NaOH溶液,溶液pH随p[c(HX)/c(X-)]变化关系如图。下列说法不正确的是
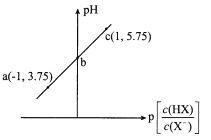
A. 溶液中水的电离程度:a<b<cB. 图中b点坐标为(0,4.75)
C. c点溶液中:c(Na+) =l0c(HX)D. 室温下HX的电离常数为10-4. 75
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用如下反应制取P4:2Ca(PO4)2 +6SiO2+10C![]() 6CaSiO3+P4+10CO
6CaSiO3+P4+10CO
回答下列问题:
(1)基态硅原子的核外电子排布式为___。
(2)Si、P、S元素第一电离能大小关系为___。
(3)P4中P原子的杂化方式是___ ,P4的空间结构为___ ,键角∠PPP=___。
(4)与CO互为等电子的阴离子是___ (填化学式)。
(5)晶体硅与金刚石结构相似,下图为晶体硅的晶胞结构。已知硅原子的半径为r nm,晶体硅的密度是___g/cm3。
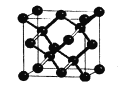
(6)硅的含氧化合物都以硅氧四面体(SiO4)作为基本结构单元,如图a所示,可简化为图b。

硅、氧原子通过共用氧原子形成各种不同的硅酸根负离子,如图c和图d,图c的化学式____________。在无限长链的硅酸根中硅氧原子之比为____。

硅、氧原子除可形成长链外,也可形成层状和立体网状结构。在立体网状结构中,硅、氧原子数之比为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同周期的X、Y、Z三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序是:HZO4![]() H2YO4
H2YO4 ![]() H3XO4,下列判断正确的是 ( )
H3XO4,下列判断正确的是 ( )
①阴离子的还原性按X、Y、Z顺序减弱
②单质的氧化性按X、Y、Z顺序增强
③元素的原子半径按X、Y、Z顺序减小
④气态氢化物的稳定性按X、Y、Z顺序减弱
①②A. ②③ B. ①②③ C. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下浓度均为0.1 mol·L-1的下列溶液的pH如表:
溶质 | NaF | Na2CO3 | NaClO | NaHCO3 |
pH | 8.1 | 11.6 | 9.7 | 8.4 |
下列有关说法正确的是( )
A. 在相同温度下,同浓度的三种酸溶液的导电能力顺序:H2CO3<HClO<HF
B. 等体积、等物质的量浓度的NaClO溶液与NaF溶液中离子总数大小:N前<N后
C. 若将少量CO2通入NaClO溶液至溶液中,离子方程式为:ClO-+CO2+H2O=HClO+CO32-
D. 向Na2CO3溶液中通入少量的HF气体,化学方程式为Na2CO3+2HF = CO2+H2O+2NaF
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com