
在80℃、101.3kPa下,用图中装置进行如下实验
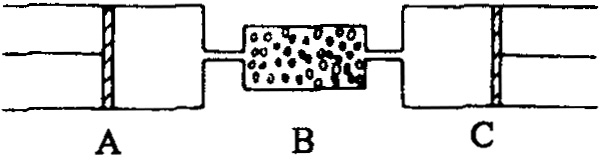
A、C两筒内分别装有无色气体,它们可能含有![]() 等气体.B管内装有固体.推动A的活塞使A筒中的气体缓缓地全部通过B后进入C筒,C中的气体由无色变成红棕色,但其体积换算成同温同压下却未变化.
等气体.B管内装有固体.推动A的活塞使A筒中的气体缓缓地全部通过B后进入C筒,C中的气体由无色变成红棕色,但其体积换算成同温同压下却未变化.
(1)C中发生反应的化学方程式是________,已知原C中气体是单一气体,它是________.将反应后C筒中的气体,用水充分吸收,在同温同压下,气体体积减少一半,则与水反应前C中的气体是________.
(2)若实验开始前A、C中气体的体积分别为1.4DL和2.24L(标准状况),且A中气体经过B管后,B管增重1.40kg,通过计算和推理可判定管中的气体是________,其质量为________g.
|
本题要从给出的
同时,还可确定B管内的固体物质是
A筒中的气体究竟是 若使C中
当
当 对A、C中气体的定量计算思维过程如下: 设在1.40L
混合气中 A中混合气的质量为 应当注意的是上述计算结果代入试题进行检验: 从B管内出来的
0.84L
反应后C筒中是1.68L
剩余气体1.12L恰为原气体2.24L体积的一半,说明计算结果完全符合题意. |


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
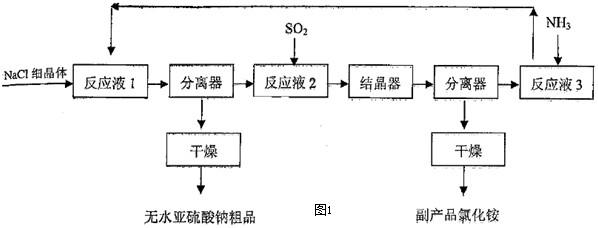
| 原料 | 理论值 | 实际值 | 利用率 |
| SO2 | 50.79 | 54.4 | 93.36% |
| NaCl | 92.86 | 101.0 | 91.94% |
| NH3 | 26.98 | 30.5 | 88.46% |
| 副产品NH4Cl | a | 87.1 | -------- |
查看答案和解析>>
科目:高中化学 来源:上海市杨浦区2013年高考一模化学试题 题型:022
硫有多种化合物,许多含硫化合物在工业上有重要的用途.
1.工业上可用黄铁矿、焦炭在有限的空气中燃烧制备硫磺.
3FeS2+12C+8O2A是________(写化学式).若得到192克的硫磺,则产生标准状况下的A气体________L.
2.硫的氯化物常做橡胶工业的硫化剂.硫与氯气在一定条件下反应,得到两种硫的氯化物B和D.B物质中的含硫量为0.3107,D物质中的含氯量为0.5259,B的相对分子质量比D小32.计算确定这两种氯化物的分子式分别为________.
3.硫化氢有毒.在120℃、101 kPa,将H2S和O2在密闭容器中点燃,充分反应后又恢复到了原来的温度和压强时,气体体积减少30%,求原混合其气体中H2S的体积分数.写出推导过程.(不考虑硫化氢的分解)
4.硫代硫酸钠是重要的还原剂,可用亚硫酸钠和硫粉在水溶液中加热制得.取15.12 g Na2SO3溶于80.0 mL水中,加入5.00 g硫粉,用小火加热至微沸,反应约1小时后过滤,将滤液蒸发至体积为30.0 mL,再冷却到10℃,则理论上析出Na2S2O3?5H2O多少克?写出推导过程.(已知:Na2S2O3的溶解度,10℃时为60.0 g/100 g水,100℃时为207 g/100 g水.100℃时,Na2S2O3饱和溶液的密度为1.14 g/mL).
查看答案和解析>>
科目:高中化学 来源: 题型:
图8-6?
(1)C中发生的反应,其化学方程式是 。已知原C中的气体是单一气体,它是 ,理由是 。?
(2)将反应后C筒内气体用水充分吸收,在同温同压下,气体体积减少一半,则与水反应前 C中的气体是 。?
(3)若实验开始前A、C中气体体积(换算成标准状况)分别为?
查看答案和解析>>
科目:高中化学 来源: 题型:
80℃,101.3 kPa下,用图86装置进行如下实验。A、C两筒内分别装有无色气体,它们可能是NH3、O2、N2、H2S、NO、CO2等气体,B筒内装有Na2O2固体,推动A的活塞使A筒内气体缓缓地全部通过B后进入C筒,C筒内气体由无色变为红棕色,但其体积换算成同温同压下却并未变化(不考虑2NO2![]() N2O4)。?
N2O4)。?
![]()
图8-6?
(1)C中发生的反应,其化学方程式是 。已知原C中的气体是单一气体,它是 ,理由是 。?
(2)将反应后C筒内气体用水充分吸收,在同温同压下,气体体积减少一半,则与水反应前 C中的气体是 。?
(3)若实验开始前A、C中气体体积(换算成标准状况)分别为?1.40 L? 和2.24 L,且A中的气体经过B管后,B管增重了?1.40 g?。经计算和推理可判定A中的气体是 ,其质量为 g(不必写出计算和推理过程)。?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com