
【题目】(1)紫薯营养丰富,具有特殊的保健功能。下表是100 g紫薯粉的营养成分含量表:
营养成分 | 含量(每100 g) | 营养成分 | 含量(每100 g) |
水分 | 9.9 g | 钙元素 | 23.00 mg |
脂肪 | 0.2 g | 铁元素 | 1.10 mg |
蛋白质 | 4.8 g | 硒元素 | 0.02 mg |
淀粉 | 82.5 g | 花青素 | 0.10 g |
纤维素 | 2.7 g | 其他 | …… |
①以上营养成分中,______是人体中含有的微量元素。
②紫薯粉中的脂肪在人体内会水解成高级脂肪酸和______。
③蛋白质在人体内水解的最终产物是氨基酸,其结构可表示为R—CH(NH2)—X,则“—X”的名称为___。
④在酶的作用下,淀粉水解为葡萄糖,葡萄糖再转化为乙醇和二氧化碳。写出葡萄糖转化为乙醇的化学方程式______。
(2)合理饮食、正确使用药物对人体健康至关重要。
①“中国居民平衡膳食宝塔”如图所示,位于最上层且每天不超过25g的能量物质是______。
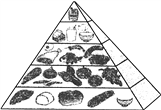
②某品牌饼干的配料标签如图所示,其中苯甲酸钠的作用是______。

③三硅酸镁(Mg2Si3O8·nH2O)具有治疗胃酸过多的作用,写出其与胃酸反应生成SiO2·H2O等物质的化学方程式______。
(3)材料的生产与使用是人类文明和生活进步的一个重要标志。
①我国C919大型客机的机身蒙皮使用的是第三代铝锂合金材料,选用铝锂合金的优点是______(任答一点)。
②铁路建设中如何防止铁轨的腐蚀是工程技术人员攻克的难题之一。钢铁在潮湿的空气中易发生吸氧腐蚀如图所示,则正极的电极反应式为______。
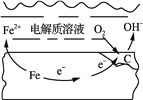
③玻璃中加入适量的溴化银(AgBr)和氧化铜的微小晶粒,经过适当的热处理,可以制成变色玻璃,请写出强光照射变色玻璃时发生反应的化学方程式______。
【答案】 铁、硒 甘油 或 丙三醇 羧基 C6H12O6![]() 2C2H5OH+2CO2↑ 油脂 防腐剂 Mg2Si3O8·nH2O+4HCl=2MgCl2+3SiO2·H2O+(n-1)H2O 密度小,硬度大,机械性能好,耐腐蚀等(合理答案均给分) O2 + 2H2O + 4e-=4OH- 2AgBr
2C2H5OH+2CO2↑ 油脂 防腐剂 Mg2Si3O8·nH2O+4HCl=2MgCl2+3SiO2·H2O+(n-1)H2O 密度小,硬度大,机械性能好,耐腐蚀等(合理答案均给分) O2 + 2H2O + 4e-=4OH- 2AgBr![]() 2Ag+ Br2
2Ag+ Br2
【解析】(1)①微量元素指:凡是占人体总重量的万分之一以下的元素,如铁、锌、铜、锰、铬、硒、钼等,因此紫薯粉中含有人体的微量元素是铁和硒;②脂肪是高级脂肪酸与甘油发生酯化反应得到的产物,因此脂肪在人体内水解产物是高级脂肪酸和甘油;③蛋白质在人体内水解的最终产物是氨基酸,含有氨基和羧基,其结构可表示为R—CH(NH2)—X,则“—X”的名称为羧基;④葡萄糖在酶的催化下转化为乙醇,同时生成二氧化碳,反应的化学方程式为C6H12O6![]() 2C2H5OH+2CO2↑;(2)①中国居民平衡膳食宝塔”位于第“5”层且每天不超过25g的能量物质是油脂;②苯甲酸钠是防腐剂有防腐作用;③Mg2Si3O8·nH2O属于硅酸盐,把它改写成氧化物形式为2MgO·3SiO2·nH2O,当它和盐酸反应时,相当于MgO和盐酸作用,因此反应的化学方程式为:Mg2Si3O8·nH2O+4HCl=2MgCl2+3SiO2·H2O+(n-1)H2O;(3)①铝锂合金的优点是密度小,硬度大,机械性能好,耐腐蚀等;②钢铁在潮湿的空气中易发生吸氧腐蚀如图所示,则正极氧气得电子产生氢氧根离子,其电极反应式为O2 + 2H2O + 4e-=4OH-;③强光照射变色玻璃时溴化银分解生成银和溴单质,发生反应的化学方程式2AgBr
2C2H5OH+2CO2↑;(2)①中国居民平衡膳食宝塔”位于第“5”层且每天不超过25g的能量物质是油脂;②苯甲酸钠是防腐剂有防腐作用;③Mg2Si3O8·nH2O属于硅酸盐,把它改写成氧化物形式为2MgO·3SiO2·nH2O,当它和盐酸反应时,相当于MgO和盐酸作用,因此反应的化学方程式为:Mg2Si3O8·nH2O+4HCl=2MgCl2+3SiO2·H2O+(n-1)H2O;(3)①铝锂合金的优点是密度小,硬度大,机械性能好,耐腐蚀等;②钢铁在潮湿的空气中易发生吸氧腐蚀如图所示,则正极氧气得电子产生氢氧根离子,其电极反应式为O2 + 2H2O + 4e-=4OH-;③强光照射变色玻璃时溴化银分解生成银和溴单质,发生反应的化学方程式2AgBr![]() 2Ag+ Br2。
2Ag+ Br2。


科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大,其中一种为金属元素。m、n、p、q、r、s是由这些元素组成的二元或三元化合物,t是元素Y的常见单质,m 是一种具有特殊颜色的气体,p 可作漂白剂、供氧剂。上述物质的转化关系如图所示。下列说法中不正确的( )
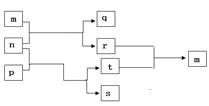
A. 四种元素简单离子半径:X〉Y〉Z〉W
B. p、s中的化学键类型完全相同
C. X、Y的简单氢化物的沸点:Y〉X
D. 常温下,0.01mol/L q溶液的pH为2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸俗称草酸,其钠盐和钾盐易溶于水,钙盐难溶于水。草酸晶体(H2C2O4·2H2O)无色、熔点为101℃。易溶于水,150℃-160℃大量升华,170℃以上分解。回答下列问题:
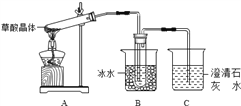
(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物,装置C中可观察到的现象是__________________________,由此可知草酸晶体分解的产物中有______________,装置B的主要作用是_____________________________________。
(2)乙组同学认为草酸晶体分解的产物中含有H2O和CO,为进行验证,选用下图中的装置进行实验。
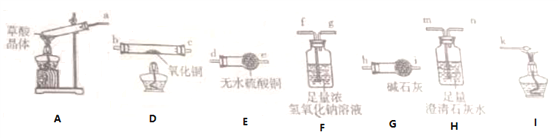
实验装置连接的合理顺序为a→___________________→k(填小写字母),能证明草酸晶体分解产物中有CO的现象是______________________________________________________________,草酸晶体受热分解的化学方程式为_______________________________________________________________。
(3)用酸性KMnO4溶液滴定反应结束后的F溶液,测定Na2C2O4的浓度
实验步骤:取20.00mLF中的溶液于锥形瓶中,再向锥形瓶中加入足量稀H2SO4,用0.1600mol/L酸性高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶被25.00mL。
①高锰酸钾溶液应装在_________(填“酸式”或“碱式”)滴定管中。
②滴定终点的现象是_______________________________________________________。
③计算F溶液中Na2C2O4的物质的量浓度为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知酸H2B在水溶液中存在下列关系:①H2B=H++HB-,②HB-![]() H++B2-,则下列说法中一定正确的是
H++B2-,则下列说法中一定正确的是
A. 在Na2B溶液中一定有:c(OH![]() )=c(H
)=c(H![]() )+c(HB
)+c(HB![]() )+2c(H2B)
)+2c(H2B)
B. NaHB溶液可能存在以下关系:c(Na![]() )>c(HB
)>c(HB![]() )>c(OH
)>c(OH![]() )>c(H
)>c(H![]() )
)
C. NaHB水溶液中一定有:c(Na![]() )+c(H
)+c(H![]() )=c(HB
)=c(HB![]() )+c(OH
)+c(OH![]() )+c(B
)+c(B![]() )
)
D. NaHB溶液一定呈酸性,Na2B溶液一定呈碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物![]() 有多种同分异构体,其中属于酯类且氯原子直接连接在苯环上的同分异构体有多少种(不考虑立体异构)
有多种同分异构体,其中属于酯类且氯原子直接连接在苯环上的同分异构体有多少种(不考虑立体异构)
A.19种 B.9种 C.15种 D.6种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列各图曲线表征的信息,得出的结论不正确的是


A. 图1表示常温下向体积为10 mL 0.1 mol·L-1NaOH溶液中逐滴加入0.1 mol·L-1CH3COOH溶液后溶液的pH变化曲线,则b点处有:c(CH3COOH)+c(H+)=c(OH-)
B. 图2表示用水稀释pH相同的盐酸和醋酸时溶液的pH变化曲线,其中Ⅰ表示醋酸,Ⅱ表示盐酸,且溶液导电性:c>b>a
C. 图3表示H2与O2发生反应过程中的能量变化,H2的燃烧热为285.8 kJ·mol-1
D. 由图4得出若除去CuSO4溶液中的Fe3+,可采用向溶液中加入适量CuO,调节溶液的pH至4左右
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的化工原料。氯化氢催化氧化制氯气的化学方程式为4HCl+O2![]() 2Cl2+2H2O。该反应中,作为氧化剂的物质是___________,被氧化的物质是____________,若反应中消耗了4 mol HCl,则生成________mol Cl2。
2Cl2+2H2O。该反应中,作为氧化剂的物质是___________,被氧化的物质是____________,若反应中消耗了4 mol HCl,则生成________mol Cl2。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组研究铁与水蒸气的反应,两位同学分别进行了如下实验。
实验Ⅰ | 实验Ⅱ |
|
|
请回答:
(1)实验Ⅰ中湿棉花的作用是______________。
(2)实验Ⅰ中反应的化学方程式是__________。
(3)甲同学观察到实验Ⅰ中持续产生肥皂泡,实验Ⅱ中溶液B呈现红色。说明溶液A中含有___________。
(4)乙同学观察到实验Ⅰ中持续产生肥皂泡,但实验Ⅱ中溶液B未呈现红色。溶液B未呈现红色的原因是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com