
【题目】已知酸H2B在水溶液中存在下列关系:①H2B=H++HB-,②HB-![]() H++B2-,则下列说法中一定正确的是
H++B2-,则下列说法中一定正确的是
A. 在Na2B溶液中一定有:c(OH![]() )=c(H
)=c(H![]() )+c(HB
)+c(HB![]() )+2c(H2B)
)+2c(H2B)
B. NaHB溶液可能存在以下关系:c(Na![]() )>c(HB
)>c(HB![]() )>c(OH
)>c(OH![]() )>c(H
)>c(H![]() )
)
C. NaHB水溶液中一定有:c(Na![]() )+c(H
)+c(H![]() )=c(HB
)=c(HB![]() )+c(OH
)+c(OH![]() )+c(B
)+c(B![]() )
)
D. NaHB溶液一定呈酸性,Na2B溶液一定呈碱性
科目:高中化学 来源: 题型:
【题目】下列关于资源综合利用和环境保护的化学方程式与工业生产实际不相符的是
A. 海水提溴时用SO2吸收Br2蒸气:SO2 + Br2 + 2H2O=H2SO4 + 2HBr
B. 将煤气化为可燃性气体:C(s) + H2O(g)![]() CO(g) + H2(g)
CO(g) + H2(g)
C. 用电解法从海水中提取镁:2MgO(熔融)![]() 2Mg + O2↑
2Mg + O2↑
D. 燃煤时加入CaCO3脱硫:2CaCO3 + 2SO2 + O2![]() 2CaSO4 + 2CO2
2CaSO4 + 2CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明N2O与CO在Fe+作用下发生反应的能量变化及反应历程如图所示,下列说法错误的是
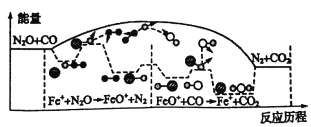
A. 反应总过程△H<0
B. Fe+使反应的活化能减小
C. 总反应若在2L的密闭容器中进行,温度越高反应速率一定越快
D. Fe++N2O→FeO++N2、FeO++CO→Fe++CO2两步反应均为放热及应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X元素的阳离子与Y的阴离子具有相同的核外电子排布,则下列比较中正确的是( )
A.原子序数: X<YB.原子半径:X<Y
C.离子半径:X<Y D.原子最外层电子数:X<Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意回答下列问题
(I)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水.当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101kPa下测得的热量).
(1)反应的热化学方程式为 .
(2)又已知H2O(l)=H2O(g)△H=+44kJ/mol.则16g液态肼与液态双氧水反应生成液态水时放出的热量是kJ.
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是 .
(4)(II)某实验小组测定中和热做了三次实验,所用NaOH溶液的浓度为0.55molL﹣1 , 盐酸的浓度为0.5molL﹣1 , 每次取NaOH溶液和盐酸溶液各50mL,并记录如表原始数据.
实验序号 | 起始温度t1/℃ | 终止温度(t2)/℃ | 温差(t2﹣t1)/℃ | ||
盐酸 | NaOH溶液 | 平均值 | |||
① | 25.1 | 24.9 | 25.0 | 28.3 | 3.3 |
② | 25.1 | 25.1 | 25.1 | 28.4 | 3.3 |
③ | 25.1 | 25.1 | 25.1 | 28.5 | 3.4 |
已知盐酸、NaOH溶液密度近似为1.00gcm﹣3 , 中和后混合液的比热容c═4.18×10﹣3 kJg﹣1℃﹣1 , 则该反应的中和热为△H= .
(5)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热会(填“偏大”、“偏小”或“不变”),其原因是 .
(6)在中和热测定实验中存在用水洗涤温度计上的盐酸溶液的步骤,若无此操作步骤,则测得的中和热(填“偏大”、“偏小”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)紫薯营养丰富,具有特殊的保健功能。下表是100 g紫薯粉的营养成分含量表:
营养成分 | 含量(每100 g) | 营养成分 | 含量(每100 g) |
水分 | 9.9 g | 钙元素 | 23.00 mg |
脂肪 | 0.2 g | 铁元素 | 1.10 mg |
蛋白质 | 4.8 g | 硒元素 | 0.02 mg |
淀粉 | 82.5 g | 花青素 | 0.10 g |
纤维素 | 2.7 g | 其他 | …… |
①以上营养成分中,______是人体中含有的微量元素。
②紫薯粉中的脂肪在人体内会水解成高级脂肪酸和______。
③蛋白质在人体内水解的最终产物是氨基酸,其结构可表示为R—CH(NH2)—X,则“—X”的名称为___。
④在酶的作用下,淀粉水解为葡萄糖,葡萄糖再转化为乙醇和二氧化碳。写出葡萄糖转化为乙醇的化学方程式______。
(2)合理饮食、正确使用药物对人体健康至关重要。
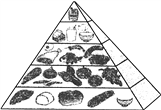
①“中国居民平衡膳食宝塔”如图所示,位于最上层且每天不超过25g的能量物质是______。
②某品牌饼干的配料标签如图所示,其中苯甲酸钠的作用是______。

③三硅酸镁(Mg2Si3O8·nH2O)具有治疗胃酸过多的作用,写出其与胃酸反应生成SiO2·H2O等物质的化学方程式______。
(3)材料的生产与使用是人类文明和生活进步的一个重要标志。
①我国C919大型客机的机身蒙皮使用的是第三代铝锂合金材料,选用铝锂合金的优点是______(任答一点)。
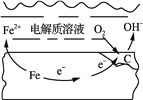
②铁路建设中如何防止铁轨的腐蚀是工程技术人员攻克的难题之一。钢铁在潮湿的空气中易发生吸氧腐蚀如图所示,则正极的电极反应式为______。
③玻璃中加入适量的溴化银(AgBr)和氧化铜的微小晶粒,经过适当的热处理,可以制成变色玻璃,请写出强光照射变色玻璃时发生反应的化学方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微量元素摄入不当也会导致代谢疾病,下列做法的主要目的与补充微量元素有关的是( )
A.咖啡加糖
B.炒菜加味精
C.酱油加铁强化剂
D.加工食品加防腐剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在温度一定的条件下,N2(g)+ 3H2(g) ![]() 2NH3(g)在密闭容器中反应并达到平衡时,混合气体的平均摩尔质量为
2NH3(g)在密闭容器中反应并达到平衡时,混合气体的平均摩尔质量为 ![]() ,N2与NH3的浓度均为c mol·L1。若将容器的体积压缩为原来的1/2,当达到新的平衡时,下列说法中不正确的是( )
,N2与NH3的浓度均为c mol·L1。若将容器的体积压缩为原来的1/2,当达到新的平衡时,下列说法中不正确的是( )
A.新的平衡体系中,N2的浓度小于2c mol·L1大于c mol·L1
B.新的平衡体系中,NH3的浓度小于2c mol·L1大于c mol·L1
C.新的平衡体系中,混合体的平均摩尔质量大于 ![]()
D.新的平衡体系中,气体密度是原平衡体系的2倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com