
����Ŀ����ͼʾʵ��װ��������CO2��CO���岢���ͼ��aΪһ���أ�bΪ��Һ©���Ļ�����ͨ��Y�ιܺͿ��طֱ��c��d���ձ������װ���ڵĿ������ž���Ϊʹʵ��ɹ����ס��ҡ����ֱ�ʢ�ŵ���Һ���� ��

A��NaHCO3������Һ 12 mol/L���� 18.4 mol/L H2SO4
B��Na2CO3������Һ 2 mol/LH2SO4 NaOH������Һ
C��NaOH������Һ 2 mol/LH2SO4 18.4 mol/L H2SO4
D��18.4 mol/L H2SO4 NaOH������Һ 18.4 mol/L H2SO4

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
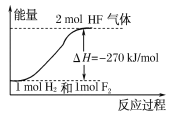
����Ŀ����֪��H2(g)��F2(g)===2HF(g) ��H����270 kJ/mol������˵����ȷ����( )
A������������ֽ����������ͷ����ķ�Ӧ�Ƿ��ȷ�Ӧ
B��1 mol H2��1 mol F2��Ӧ����2 molҺ̬HF�ų�������С��270 kJ
C������ͬ�����£�1 mol H2��1 mol F2�������ܺʹ���2 mol HF���������
D���÷�Ӧ�е������仯������ͼ����ʾ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ��������������칤����������ˮ����������Ϊ�˱�����̬���������ȫ������������������Ҫ�ٴ롣���д�ʩ���������Ϲ���ʵʩ����
A���ƹ�ʹ��ȼú������������SO2��Ⱦ
B�������ؽ�����ũҩ���ѷֽ��л�����ŷ�
C���Ӵ�ʯ�͡�ú̿�Ŀ����ٶȣ����ӻ�ʯȼ�ϵĹ�Ӧ��
D����������Դ���������������CO2�ͷ����������ʵĴ����ŷ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ص������������( )
A�����Գ���ˮ(AOW)����������H1N1��������Ϊ��������ǿ������
B��ˮ�������õ�Ư�ۺ����������ߵ�����ԭ����ͬ
C�����ع��͡���ֹʳ�ã����������Ʒ���
D�������谷����ţ���������Ӻ����������к�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������з�Ӧ�У�HCl����ԭ�����ǣ� ��
A. NaOH + HCl = NaCl + H2O
B. Zn + 2HCl = ZnCl2 + H2��
C. MnO2 + 4HCl��Ũ��![]() MnCl2 + 2H2O + Cl2��
MnCl2 + 2H2O + Cl2��
D. CuO + 2HCl = CuCl2 + H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[ѡ�� 3�������ʽṹ������]
X��Y��Z��W��Q��R ��Ϊǰ������Ԫ�أ���ԭ���������������������Ϣ���±���ʾ��

�ش��������⣺
��1��Y Ԫ�صĻ�̬ԭ�ӵĵ����Ų�ʽΪ ,���һ�������� Z Ԫ��ԭ�ӵĵ�һ������ (����������������)
��2��X ���Ȼ�����۵�� Q ���Ȼ�������� (����������������)��������
��3������֤ʵԪ�� W �ĵ�����ǿ������Һ��Ӧ�� W(OH)4]-���ɣ��� W(OH)4]-�д��� (����ĸ)
a�����Թ��ۼ� b���Ǽ��Թ��ۼ� c����λ�� d�����
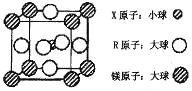
��4������ X��R ��þ����Ԫ�ص�ij�־�����г����ԣ���ṹ����ͼ��ʾ�����þ���Ļ�ѧʽΪ �� ������ÿ��þԭ����Χ��������� R ԭ���� ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����( )
A. ��ѧ��Ӧ��������Ϊ��Ӧ�������������������������� B. ����Ҫ���Ⱦ��ܷ����ķ�Ӧ�Ƿ��ȷ�Ӧ
C. ��ѧ����������һ����ʽ,����������ת��Ϊ����,Ҳ��ת��Ϊ���� D. �Ȼ��ƾ����ۻ�ʱ,���Ӽ����ƻ�,��������,������ѧ�仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȷ���ǣ� ��
A. c(NH4+)��ȵ�(NH4)2SO4��Һ��NH4HSO4��Һ��NH4Cl��Һ�У�����Ũ�ȴ�С��ϵ�ǣ� c[(NH4)2SO4]< c[(NH4HSO4] < c(NH4Cl)
B. ����ȥCuCl2��Һ�л���������FeCl3���ɼ���CuO
C. 0.2mol/L HCl��Һ������0.05mol/L Ba(OH)2��Һ��Ϻ���Һ��pH=1
D. 0.2mol/L��NaHCO3��Һ��c(H+)+c(H2CO3)=c(CO32-)+c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ϵġ��ر�αװ����ʹ���±��������ɫ�ʡ����ⷴ���뻷���Ǻϡ�BASF����20����70���������ϵ���ͺ���αװ��ԭȾ�ϣ���Ⱦ��Ϊ���ɫ���ɫ���仯ѧ�ṹΪ��

������������⣺
��1��Ⱦ��BASF�ķ���ʽ�ɱ�ʾΪC2n+24HxN2O6����x=___________��
��2��1mol��������Na��Ӧ���������������ڴ��������¼ӳ��������������������ֵ�����ʵ������ֱ�Ϊ_____________��____________��
��3����n=3ʱ������̼ԭ���ϵ�һ��ȡ���������__________�֡�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com