
【题目】在标准状况下有:①6.72LCH4,②3.01×1023个HCl分子,③13.6gH2S,④0.2molNH3。下列对这四种气体的描述正确的是( )
a. 体积②>③>①>④ b. 密度②>③>④>①
c. 质量②>③>①>④ d. 氢原子个数①>③>④>②
A. abc B. bcd C. abd D. abcd
【答案】D
【解析】
试题a、甲烷的体积是6.72L,3.01×1023个HCl分子的体积=11.2L,13.6g H2S的体积=![]() ×22.4L/mol=8.96L,0.2mol NH3的体积=0.2mol×22.4L/mol=4.48L,所以气体体积大小顺序是②>③>①>④,a正确; b.相同条件下,气体摩尔体积相同,根据ρ=
×22.4L/mol=8.96L,0.2mol NH3的体积=0.2mol×22.4L/mol=4.48L,所以气体体积大小顺序是②>③>①>④,a正确; b.相同条件下,气体摩尔体积相同,根据ρ=![]() 知,密度与其相对分子质量成正比,所以密度大小顺序是②>③>④>①,b正确;c、甲烷的质量是
知,密度与其相对分子质量成正比,所以密度大小顺序是②>③>④>①,b正确;c、甲烷的质量是![]() =4.8g、3.01×1023个HCl分子的物质的量是0.5mol,质量是0.5mol×36.5g/mol=18.25g、③H2S的质量是13.6g、④0.2 mol NH3的质量是0.2mol×17g/mol=3.4g,质量②>③>①>④,c正确;d、甲烷的物质的量
=4.8g、3.01×1023个HCl分子的物质的量是0.5mol,质量是0.5mol×36.5g/mol=18.25g、③H2S的质量是13.6g、④0.2 mol NH3的质量是0.2mol×17g/mol=3.4g,质量②>③>①>④,c正确;d、甲烷的物质的量![]() ,含氢原子1.2mol;②3.01×1023个HCl分子,含有氢原子0.5mol;③13.6 g H2S物质的量
,含氢原子1.2mol;②3.01×1023个HCl分子,含有氢原子0.5mol;③13.6 g H2S物质的量![]() =0.425mol,含氢原子个0.85mol;④0.2 mol NH3,含氢原子个0.6mol;氢原子个数①>③>④>②,d正确;故选D。
=0.425mol,含氢原子个0.85mol;④0.2 mol NH3,含氢原子个0.6mol;氢原子个数①>③>④>②,d正确;故选D。


 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源: 题型:
【题目】已知 100mL MgCl2 和 AlCl3 混合溶液中,c(Cl-)=1.2mol/L,c(Mg2+)=0.3mol/L。欲使 Mg2+全部沉淀而分离出来,至少需 4 mol/L NaOH 溶液( )
A. 25mL B. 30mL C. 35mL D. 100mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如右图所示,由此确定,原溶液中可能含有的阳离子是

A. Mg2+、Al3+、Fe2+ B. H+、Mg2+、Al3+
C. H+、Ba2+、Al3+ D. 只有Mg2+、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常状况下,CO是一种无色、无味、有毒的气体,难溶于水,与酸、碱、盐溶液均不反应。已知乙二酸晶体加热分解的方程式为:H2C2O42H2O ![]() 3H2O + CO2↑+ CO↑,不考虑其他因素干扰,如何利用下列装置验证反应产物中含有CO2和CO(装置不能重复使用)。酒精喷灯可作高温热源。请回答下列问题:
3H2O + CO2↑+ CO↑,不考虑其他因素干扰,如何利用下列装置验证反应产物中含有CO2和CO(装置不能重复使用)。酒精喷灯可作高温热源。请回答下列问题:
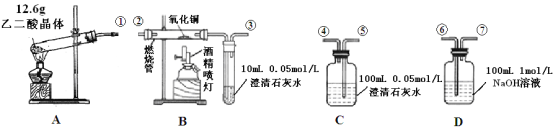
(1)检验装置A气密性的方法是___________________________________________
(2)按气流方向连接各仪器,用数字表示接口的连接顺序: ①→_________________;
(3)证明CO存在的实验现象是_______________________________________________;
(4)本实验尾气处理的方法是_______________________________________;
(5)根据题给的数据,假设反应产生的气体全部排出,并与吸收液充分反应(提示:B、C中澄清石灰水均先变浑浊,后又变澄清),D中溶质及对应的物质的量是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是人类共同关注的重要问题。页岩气是从页岩层中开采出来的一种非常重要的天然气资源,页岩气的主要成分是甲烷,是公认的洁净能源。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和H2)。CH4与H2O(g)通入聚焦太阳能反应器,发生反应 CH4(g)+H2O(g)=CO(g)+3H2(g)△H1
已知:①CH4、H2、CO 的燃烧热(△H)分别为-a kJmol-1、-b kJmol-1、-c kJmol-1;
②H2O (l) =H2O(g); △H=+dkJmol-1
则△H1= ___________(用含字母a、b、c、d的代数式表示)kJmol-1。
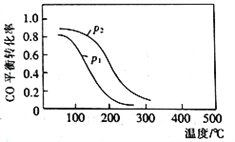
(2)用合成气生成甲醇的反应为:CO(g)+2H2(g)![]() CH3OH(g) △H2,在10L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200℃时n(H2)随时间的变化如下表所示:
CH3OH(g) △H2,在10L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200℃时n(H2)随时间的变化如下表所示:
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
①△H2_________ (填“>”“<”或“ = ”)0。
②下列说法正确的是____________ (填标号)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强p1<p2
③ 03 min内用CH3OH表示的反应速率v(CH3OH)=________mol L-1·min-1。
④ 200℃时,该反应的平衡常数K =_______。向上述200℃达到平衡的恒容密闭容器中再加入2 mol CO、2 mol H2、2 mol CH3OH,保持温度不变,则化学平衡____________(填“正向”、“逆向”或“不”)移动。
(3)甲烷、氧气和KOH溶液可组成燃料电池。标准状况下通入5.6 L甲烷,测得电路中转移1.2 mol电子,则甲烷的利用率为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu在稀硝酸中可以发生如下反应:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O 下列叙述正确的是()
A. HNO3在反应中失去电子
B. 氧化产物与还原产物的物质的量比为3:2
C. 发生氧化反应的硝酸占参加反应硝酸的1/4
D. 每1 mol HNO3参加反应,有3 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烯烃与氢气加成后得到2,2-二甲基丁烷,则该烯烃的名称是
A. 2,2-二甲基-3-丁烯 B. 2,2-二甲基-2-丁烯
C. 2,2-二甲基-1-丁烯 D. 3,3-二甲基-1-丁烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、d为四种由短周期元素组成的中性粒子,它们都有14个电子,且b、c、d都是共价型分子。回答下列问题:
(1)a单质可由原子直接构成,a单质可用作半导体材料,其原子核外电子排布式为________。
(2)b是双核化合物,常温下为无色无味气体,b的化学式为________________。人一旦吸入b气体后,就易引起中毒,是因为______________而中毒。
(3)c是双核单质,写出其电子式______________。c分子中所含共价键的类型为____________(填“极性键”或“非极性键”)。
(4)d是四核化合物,其结构式为________________;d分子内所含σ键的数目是________,π键的数目是______,σ键的强度比π键的强度________,原因是__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com