
【题目】一定温度下,0.1mol N2和0.3molH2在恒容的密闭容器中发生如下反应:N2(g)+3H2(g) ![]() 2NH3(g) △H<0下列说法不正确的是
2NH3(g) △H<0下列说法不正确的是
A. 达到平衡状态时,v正(NH3): v逆(N2)=2 : 1
B. c(N2):c(H2):c(NH3)=1:3:2时,说明反应已达到平衡状态
C. 容器内的压强不再变化时,说明反应已达到平衡状态
D. 升高温度时,v正(NH3)增大,v逆(NH3)增大
科目:高中化学 来源: 题型:
【题目】一种可充电锂-空气电池如图所示。当电池放电时,O2与Li+在多孔碳材料电极处生成Li2O2-x(x=0或1)。下列说法正确的是

A. 放电时,多孔碳材料电极为负极
B. 放电时,外电路电子由多孔碳材料电极流向锂电极
C. 充电时,电解质溶液中Li+向多孔碳材料区迁移
D. 充电时,电池总反应为Li2O2-x=2Li+(1-![]() )O2
)O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D 原子序数依次增加,X、Y、Z、W是由这四种元素中的两种元素组成的常见化合物,X为有刺激性气味的气体,Y为淡黄色固体,甲是由C元素形成的气体单质,乙为红棕色气体,上述物质之间的转化关系如下图所示(部分反应物或生成物省略)。下列说法正确的是

A. 原子半径大小顺序:D>C>B>A B. 最简单气态氢化物的稳定性:B>C
C. 图示转化关系涉及的反应均为氧化还原反应 D. 元素C、D形成的化合物中一定只含离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 1L0.lmol·L-1的氢氧化钾溶液中O—H键的数目为0.1NA
B. 0.5mol·L-1的碳酸钠溶液中CO32-的数目小于0.5NA
C. 4.6g金属钠与500mL0.2 mol·L-1稀盐酸充分反应,转移电子数为0.1 NA
D. 标准状况下,2.24L乙烯和甲烷混合气体中含有的氢原子数目为0.4 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】古瓷中所用颜料的成分一直是个谜,近年来科学家才得知大多为硅酸盐,如蓝紫色的硅酸铜钡(BaCuSi2Ox,铜为+2价),下列关于硅酸铜钡的说法不正确的是( )
A.可用氧化物形式表示为BaO·CuO·2SiO2
B.性质稳定,不易脱色
C.易溶解于强酸和强碱
D.x等于6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D、E、F,它们的原子序数依次增大;A元素的原子是半径最小的原子;B元素的最高价氧化物对应水化物与其气态氢化物反应生成一种盐X;D与A同主族,且与F同周期;F元素的最外层电子数是其次外层电子数的3/4倍,A、B、D、F这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物。D、E、F三种元素对应的最高价氧化物的水化物间两两皆能反应。请回答下列问题:
(1)写出B、C、E元素的名称B___、C___、E___。
(2)请写出含C质量分数最高的化合物的化学式:______ 。
(3)A、C、D、F四种元素可以形成两种可以互相反应的酸式盐(均由四种元素组成),这两种酸式盐的化学式分别为______、______。
(4)A、C、F间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为________________________。
(5)向含有a molE离子的氯化物溶液中加入含b molD的最高价氧化物对应水化物的溶液,生成沉淀的物质的量不可能为_______________________________ 。
①a mol ②b mol ③a/3 mol ④b/3 mol ⑤0⑥(4a-b)mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组为探究难溶性盐X(仅含三种元素)的组成和性质,设计并完成如下实验:
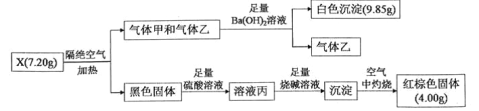
已知:气体甲和气体乙组成元素相同,物质的量之比为1:1。请回答:
(1)X的化学式为___________。
(2)溶液丙与H2O2溶液在酸性条件下反应的离子方程式是___________________________。
(3)写出利用流程图中某种物质将红棕色固体重新转化为黑色固体的化学方程式:____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com