
有一废水样品10 L,经分析得知含游离氯(Cl2)浓度为0.012 mol/L,其H+浓度为1×10-3 mol/L.已知Cl2+Na2SO3+H2O=Na2SO4+2HCl.现欲除去其中的游离氯,并成为中性溶液,问需加浓度为0.1 mol/L的Na2SO3溶液的体积是多少?需加入固体烧碱的质量是多少?
科目:高中化学 来源: 题型:阅读理解
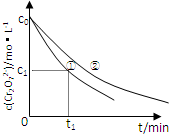 (2013?安徽)某酸性工业废水中含有K2Cr2O7.光照下,草酸(H2C2O4)能将其中的Cr2O72-转化为Cr3+.某课题组研究发现,少量铁明矾[Al2Fe(SO4)4?24H2O]即可对该反应起催化作用.为进一步研究有关因素对该反应速率的影响,探究如下:
(2013?安徽)某酸性工业废水中含有K2Cr2O7.光照下,草酸(H2C2O4)能将其中的Cr2O72-转化为Cr3+.某课题组研究发现,少量铁明矾[Al2Fe(SO4)4?24H2O]即可对该反应起催化作用.为进一步研究有关因素对该反应速率的影响,探究如下:| 实验 编号 |
初始 pH |
废水样品 体积/mL |
草酸溶液 体积/mL |
蒸馏水 体积/mL |
| ① | 4 | 60 | 10 | 30 |
| ② | 5 | 60 | 10 | 30 |
| ③ | 5 | 60 | 20 20 |
20 20 |
| 2(c0-c1) |
| t1 |
| 2(c0-c1) |
| t1 |
| 实验方案(不要求写具体操作过程) | 预期实验结果和结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)需加入浓度为0.1 mol·L-1的Na2SO3溶液多少升?
(2)需加入固体烧碱多少克?
查看答案和解析>>
科目:高中化学 来源:2013年全国普通高等学校招生统一考试理科综合能力测试化学(安徽卷解析版) 题型:实验题
某酸性工业废水中含有K2Cr2O7。光照下,草酸(H2C2O4)能将其中的Cr2O72-转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
(1)在25°C下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,作对比实验,完成以下实验设计表(表中不要留空格)。
|
实验编号 |
初始pH |
废水样品体积mL |
草酸溶液体积mL |
蒸馏水体积mL |
|
① |
4 |
60 |
10 |
30 |
|
② |
5 |
60 |
10 |
30 |
|
③ |
5 |
60 |
|
|
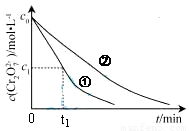
测得实验①和②溶液中的Cr2O72-浓度随时间变化关系如图所示。
(2)上述反应后草酸被氧化为 (填化学式)。
(3)实验①和②的结果表明 ;实验①中0~t1时间段反应速率v(Cr3+)= mol·L-1·min-1
(用代数式表示)。
(4)该课题组队铁明矾[Al2Fe(SO4)4·24H2O]中起催化作用的成分提出如下假设,请你完成假设二和假设三:
假设一:Fe2+起催化作用;
假设二: ;
假设三: ;
……
(5)请你设计实验验证上述假设一,完成下表中内容。
(除了上述实验提供的试剂外,可供选择的药品有K2SO4、FeSO4、Al2Fe(SO4)4·24H2O、Al2(SO4)3等,溶液中Cr2O72-的浓度可用仪器测定。)
|
实验方案(不要求写具体操作过程) |
预期实验结果和结论 |
|
|
|
查看答案和解析>>
科目:高中化学 来源: 题型:
有一废水样品10L,经分析得知含游离氯(Cl2)浓度为0.012mol/L,其H+浓度为1×10—3mol/L。已知Cl2+Na2SO3+H2O=Na2SO4+2HCl。现欲除去其中的游离氯,并成为中性溶液,问需加浓度为0.1mol/L的Na2SO3溶液的体积是多少?需加入固体烧碱的质量是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com