
【题目】I.NaCl溶液中混有Na2CO3、Na2SO4,为检验两种物质的存在,请你根据所选择的试剂,按实验步骤的先后顺序写出相应的化学方程式:
①______________________________;
②______________________________;
③________________________________。
II.取100.0 mLNa2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到16.84g沉淀,用过量稀硝酸处理后沉淀质量减少至6.99g,同时溶液中有气泡产生。试求:原混合液中Na2SO4的物质的量浓度为________________;(写出计算列式的过程)
【答案】Na2CO3+2HCl=2NaCl+CO2↑+H2O CO2+Ca(OH)2=CaCO3↓+H2O BaCl2+Na2SO4=BaSO4↓+2NaCl 0.3mol/L
【解析】
I.首先加入过量HCl,有气泡产生,该气体能够使澄清石灰水变浑浊,说明有Na2CO3,再滴加过量BaCl2溶液,最终有白色沉淀证明有Na2SO4;
II.混合溶液加入过量的氯化钡溶液,发生反应:BaCl2+Na2SO4=BaSO4↓+2NaCl、BaCl2+Na2CO3=BaCO3↓+2NaCl,得到16.84g白色沉淀为BaSO4、BaCO3,沉淀用过量稀HNO3处理,发生反应:BaCO3+2HNO3=Ba(NO3)2+CO2↑+H2O,最终6.99g沉淀为BaSO4,根据n=![]() 计算BaSO4的物质的量,而n(Na2SO4)=n(BaSO4),再根据c=
计算BaSO4的物质的量,而n(Na2SO4)=n(BaSO4),再根据c=![]() 计算c(Na2SO4)。
计算c(Na2SO4)。
I.首先向该物质的水溶液中滴加过量盐酸,有气体产生,该气体能够使澄清的石灰水变浑浊,证明溶液中含有Na2CO3,反应方程式为:Na2CO3+2HCl=2NaCl+CO2↑+H2O,CO2+Ca(OH)2=CaCO3↓+H2O,然后向溶液中加入过量BaCl2溶液,产生白色沉淀,证明含有Na2SO4,发生该反应的化学方程式为:Na2SO4+BaCl2=2NaCl+BaSO4↓;
II.混合溶液加入过量的氯化钡溶液,发生反应:BaCl2+Na2SO4=BaSO4↓+2NaCl、BaCl2+Na2CO3=BaCO3↓+2NaCl,得到16.84g白色沉淀为BaSO4、BaCO3的质量和,沉淀用过量稀HNO3处理,发生反应:BaCO3+2HNO3=Ba(NO3)2+CO2↑+H2O,最终6.99g沉淀为BaSO4,根据n=![]() 可知n(BaSO4)=
可知n(BaSO4)=![]() =0.03mol,根据S元素守恒可知n(Na2SO4)=n(BaSO4),所以根据c=
=0.03mol,根据S元素守恒可知n(Na2SO4)=n(BaSO4),所以根据c=![]() 可得c(Na2SO4)=
可得c(Na2SO4)=![]() =0.3mol/L。
=0.3mol/L。


科目:高中化学 来源: 题型:
【题目】能正确表示下列化学反应的离子方程式的是( )
A.硫酸铜溶液与氢氧化钡溶液反应:Ba2++![]() =BaSO4↓
=BaSO4↓
B.将NaHSO4溶液滴入Ba(OH)2溶液中至溶液呈中性:2H++![]() +2OH-+Ba2+=BaSO4↓+2H2O
+2OH-+Ba2+=BaSO4↓+2H2O
C.足量CO2通入澄清石灰水中:2OH-+CO2=H2O+![]()
D.碳酸氢钙溶液与足量氢氧化钠溶液反应:Ca2++![]() +OH-=CaCO3↓+H2O
+OH-=CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿主要成分是二硫化亚铁铜(CuFeS2)。黄铜矿经熔炼、煅烧后得到粗铜和炉渣,冶炼过程的主要反应有:

(1)二硫化亚铁铜也可以表示为CuS·FeS,其中硫元素的化合价是____。
(2)反应②中还原剂是________。
(3)某校学习小组用炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3等)制备铁红,进行如下实验。
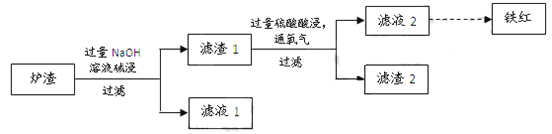
① 炉渣碱浸时反应的离子方程式是_____、_____。
② 滤渣1中加入硫酸并通入氧气可使FeO转化为Fe3+,该反应的离子方程式是________;为检验铁元素是否被氧化完全,应进行的实验是:取少量滤液2于试管中_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下CH4、H2S、NH3均为气体,分别有①11.2L H2S②16g CH4③1.204×1024个NH3分子,下列物理量大小比较正确的是( )
A. 体积:②>③>①
B. 密度:③>②>①
C. 质量:③>②>①
D. 原子总数:③>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
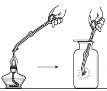
【题目】某实验小组同学把小块木炭在酒精灯上烧至红热,迅速投入热的浓硝酸中,发生剧烈反应,同时有大量红棕色气体产生,液面上木炭迅速燃烧发出亮光。经查阅资料可知浓硝酸分解产生NO2和O2。为了探究“液面上木炭迅速燃烧发出亮光”的原因,该小组同学用如图装置完成以下实验:
序号 | 实验I | 实验II |
集气瓶中所盛气体 | O2 | 加热浓硝酸 产生的气体 |
现象 | 木炭迅速燃烧发出亮光 | 木炭迅速燃烧发出亮光 |
下列说法正确的是
A. 浓硝酸分解产生的V(NO2):V(O2)=1:1
B. 红棕色气体的产生表明木炭与浓硝酸发生了反应
C. 能使液面上木炭迅速燃烧发出亮光的主要气体是氧气
D. 以上实验不能确定使液面上木炭迅速燃烧发出亮光的主要气体一定是NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠保存不当容易变质,某课外活动小组为了粗略测定过氧化钠的质量分数,他们称取10.0g样品,并设计用如图装置来测定过氧化钠的质量分数。

上图中的E和F构成量气装置,用来测定O2的体积。
(1)写出以下装置发生反应的化学方程式:
装置A:___________________________。
装置B:___________________________。
装置C:____________________________。
(2)NaOH溶液的作用是_________________________。
(3)为准确读出氧气的体积需以下操作,正确的顺序为_________。
A.调整量筒高度,使广口瓶E与量筒F内液面相平
B.将气体冷却至室温
C.平视,使凹液面最低点与视线水平相切再读数
读出量筒内水的体积后,折算成标准状况氧气的体积为1.12L,则样品中过氧化钠的质量分数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2和CO混合气体共8mol,通入足量Na2O2中,并且用电火花持续引爆,充分反应后,剩余气体1mol,则固体增重为多少克?( )
A.56gB.168gC.224gD.196g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(化学式为 NaNO2)是一种常用的防腐剂,回答下列问题:
(1)NaNO2 中 N 元素的化合价为_________.
(2)亚硝酸钠在 320°C 时能分解产生氧化钠固体、一氧化氮和一种常见的助燃性气体。该反应的化学方程式_________________。
(3)我国规定火腿肠中亚硝酸钠添加标准为每千克食品含量不超过 150 毫克,以此计算,200g 15%的亚硝酸钠溶液至少可用于生产火腿肠______千克。
(4)在酸性条件下,NaNO2与按物质的量 1:1 恰好完全反应,且I-被氧化为 I2时,产物中含氮的物质为________(填化学式)。
(5)工业废水中的 NaNO2 可用铝粉除去,已知此体系中包含 AI、NaAlO2、NaNO2、NaOH、NH3、H2O 六种物质。该反应的化学方程式为____________。
(6)某同学设计实验对工业产品中 NaNO2 的含量进行测定,你取固体样品 2g,完全溶解配制成溶液 100mL 取出 25mL 溶液用 0.100 mol/L 酸性 KMnO4 溶液进行滴定(杂质不与 KMnO4 反应),实验所得数据如下表所示:
滴定次数 | 1 | 2 | 3 | 4 |
消耗KMnO4溶液体积/mL | 20.70 | 20.02 | 20.00 | 19.98 |
该样品中亚硝酸钠的质量分数为_________.(已知:5NO2-+2MnO4-+6H+ = 5NO3-+2Mn2++3H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一种综合处理SO2废气的工艺流程.下列说法正确的是( )
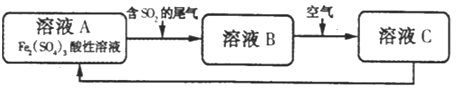
A.向B溶液中滴加KSCN溶液,溶液可能变为血红色
B.溶液B转化为溶液C发生的变化的离子方程式为4H+ + 2Fe2++O2=2Fe3++2H2O,
C.溶液酸性:A>B>C
D.加氧化亚铁可以使溶液C转化为溶液A
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com