
����Ŀ���������ƣ���ѧʽΪ NaNO2����һ�ֳ��õķ��������ش���������:
��1��NaNO2 �� N Ԫ�صĻ��ϼ�Ϊ_________.
��2������������ 320��C ʱ�ֽܷ���������ƹ��塢һ��������һ�ֳ�������ȼ�����塣�÷�Ӧ�Ļ�ѧ����ʽ_________________��
��3���ҹ��涨���ȳ��������������ӱ�Ϊÿǧ��ʳƷ���������� 150 ���ˣ��Դ˼��㣬200g 15��������������Һ���ٿ������������ȳ�______ǧ�ˡ�
��4�������������£�NaNO2�밴���ʵ��� 1:1 ǡ����ȫ��Ӧ����I��������Ϊ I2ʱ�������к���������Ϊ________���ѧʽ����
��5����ҵ��ˮ�е� NaNO2 �������۳�ȥ����֪����ϵ�а��� AI��NaAlO2��NaNO2��NaOH��NH3��H2O �������ʡ��÷�Ӧ�Ļ�ѧ����ʽΪ____________��
��6��ijͬѧ���ʵ��Թ�ҵ��Ʒ�� NaNO2 �ĺ������вⶨ����ȡ������Ʒ 2g����ȫ�ܽ����Ƴ���Һ 100mL ȡ�� 25mL ��Һ�� 0.100 mol/L ���� KMnO4 ��Һ���еζ������ʲ��� KMnO4 ��Ӧ����ʵ�������������±���ʾ:
����� | 1 | 2 | 3 | 4 |
����KMnO4��Һ���/mL | 20.70 | 20.02 | 20.00 | 19.98 |
����Ʒ���������Ƶ���������Ϊ_________.����֪:5NO2-+2MnO4-+6H+ = 5NO3-+2Mn2++3H2O��
���𰸡� +3 4NaNO2![]() 2Na2O+4NO��+O2�� 200 NO NaNO2+2Al+NaOH+H2O=2NaAlO2+NH3�� 69%
2Na2O+4NO��+O2�� 200 NO NaNO2+2Al+NaOH+H2O=2NaAlO2+NH3�� 69%
��������(1)�����ڻ��������������ϼ۴�����Ϊ�㣬�������������е�Ԫ�صĻ��ϼ�Ϊx����(+1)+x+(-2)��2=0�����x=+3���ʴ�Ϊ��+3��
(2)��Ϊ����������320��ʱ�ֽܷ���������ƹ��塢һ�����������һ�ֳ�������ȼ�����壬�ʷ�Ӧ�Ļ�ѧ����ʽΪ4NaNO2![]() 2Na2O+4NO��+O2����
2Na2O+4NO��+O2����
(3)��Ϊ�ҹ��涨��೦�������������ӱ�Ϊÿǧ��ʳƷ����������150���ˣ�����200g��15%������������Һ���ٿ�����������೦������Ϊ 200g��15%��![]() �T200kg���ʴ�Ϊ��200kg��
�T200kg���ʴ�Ϊ��200kg��
(4)�����ӱ�����Ϊ�ⵥ��ʱ�����еĵ�Ԫ�ػ��ϼ�������2�ۣ����ĵ�������2mol�����������е�Ԫ�ػ��ϼ���+3�ۣ�2mol���������Ƶõ�2mol����ʱ�����赪Ԫ�صĻ��ϼ۽�Ϊ+2�ۣ����Բ����к���������ΪNO���ʴ�Ϊ��NO��
(5)�������ƾ��������ԣ����������л�ԭ�ԣ����������£����߷���������ԭ��Ӧ����ƫ�����κͰ�����ˮ����Ӧ�Ļ�ѧ����ʽΪ��NaNO2+2Al+NaOH+H2O=2NaAlO2+NH3�����ʴ�Ϊ��NaNO2+2Al+NaOH+H2O=2NaAlO2+NH3����
(6)���ĸ�����ص����ʵ�����0.1mol/L��0.02L=0.002mol������ݷ���ʽ5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O��֪���������Ƶ����ʵ�����0.002mol��![]() =0.005mol����ԭ��Ʒ���������Ƶ����ʵ�����0.005mol��
=0.005mol����ԭ��Ʒ���������Ƶ����ʵ�����0.005mol��![]() =0.02mol��������Ϊ0.02mol��69g/mol=1.38g��������Ʒ���������Ƶ���������
=0.02mol��������Ϊ0.02mol��69g/mol=1.38g��������Ʒ���������Ƶ���������![]() ��100%=69.0%���ʴ�Ϊ��69.0%��
��100%=69.0%���ʴ�Ϊ��69.0%��


 ��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�����������ʹ��ˮ�е�OH-������Ŀ���ӵ��� ( )
A��Al3+ B��CO32- C��NH4�� D��Br��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һһ�������Ե���(����)
A. ��H������Һ B. c(OH��)<c(H��)����Һ
C. pH<7����Һ D. �������Al��Ӧ�ų�H2����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���������Ҵ�����������������ȼ�գ��õ�CO��CO2��ˮ��������Ϊ27.6g��������ˮ������Ϊ10.8g����CO�������ǣ�������
A.4.4g
B.1.4g
C.2.2g
D.��2.2g��4.4g֮��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾ��ԭ��أ�����˵����ȷ����(����)

A. ���Ӵ�п�缫ͨ����������ͭ�缫,������п�缫,�γɱպϵ�·
B. �����е�������������ͭ��Һ��Ǩ��
C. п�缫������ԭ��Ӧ
D. ͭ�缫�Ϸ����ĵ缫��ӦΪ2H����2e��===H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ƭ��ϡ���ᷴӦ��ȡ����ʱ�����д�ʩ����ʹ�����������ʼӴ����
A.����B.����ϡ���ᣬ����Ũ����
C.�μ�����Ũ����D.������Ƭ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ǽ��л����������ĸ���ͬԭ�ӣ���ԭ���ţ���̼ԭ�ӳ�Ϊ����̼ԭ�ӣ���ͼ��ʾ����X�к���һ������̼ԭ�ӣ���*��ǣ����ش��������⣺ 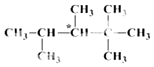
��1������X������������һ�ȴ��ﹲ���֣������������칹����ͬ����
��2����������̼ԭ�ӵ���ʽ����С�������Ļ�ѧʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ữ��MgCl2��FeCl3�����Һ����ε���NaOH��Һ�����ɵij������������NaOH��Һ�����ϵ����ͼ����ԭ�����Һ��MgCl2��FeCl3�����ʵ���֮��Ϊ�������� 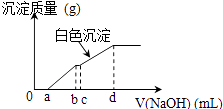
A.![]()
B.![]()
C.![]()
D.![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���Ҽ�����Һ���Ƿ����SO42-����ѡ�õĻ�ѧ�Լ�����Ϊ
A. KCl(aq)��HCl(aq) B. HNO3(aq)��KNO3(aq)
C. HCl(aq)��BaCl2(aq) D. NaNO3(aq)��HNO3(aq)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com