
����Ŀ��H2S������Դ������;��֮һ�ǻ����������õ�������Ӧԭ��Ϊ��2H2S��g��+O2��g���TS2��s��+2H2O��l����H=��632kJmol��1 �� ��ͼΪ����ĤH2Sȼ�ϵ�ص�ʾ��ͼ������˵����ȷ���ǣ� �� 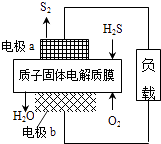
A.�缫aΪ��ص�����
B.�缫b�Ϸ����ĵ缫��ӦΪ��O2+2H2O+4e��=4 OH��
C.��·��ÿ����4mol���ӣ�����ڲ��ͷ�632kJ����
D.ÿ17gH2S���뷴Ӧ����1mol H+������Ĥ����������
���𰸡�D
���������⣺A����2H2S��g��+O2��g���TS2��s��+2H2O��Ӧ���ó�����H2Sʧ���ӷ���������Ӧ����aΪ��صĸ�������A����
B������O2�õ��ӷ�����ԭ��Ӧ�����Ե缫b�Ϸ����ĵ缫��ӦΪ��O2+4H++4e��=2H2O����B����
C����·��ÿ����4mol���ӣ�������1mol����������װ�ý���ѧ��ת��Ϊ���ܣ����Ե���ڲ��������ų���������C����
D��ÿ17g�� ![]() =0.5molH2S���뷴Ӧ��������0.25mol�����������O2+4H++4e��=2H2O��������1mol H+������Ĥ��������������D��ȷ��
=0.5molH2S���뷴Ӧ��������0.25mol�����������O2+4H++4e��=2H2O��������1mol H+������Ĥ��������������D��ȷ��
���Դ��ǣ�D��


 ������������ϵ�д�
������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧһ�����ڷ��ȷ�Ӧ����
A. ��������������Ȼ�茶���ķ�Ӧ
B. ��Ӧ�������������������͵ķ�Ӧ
C. ��ѧ���������յ������Ȼ�ѧ���γɷų��������ٵķ�Ӧ
D. ����Ҫ���Ⱦ��ܷ����ķ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʽ̼����þ[MgaAlb��OH��c��CO3��dxH2O]������������ȼ���� 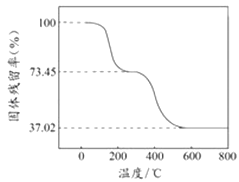
��1����ʽ̼����þ������ȼ���ã������������ȷֽ������մ��������� ��
��2��[MgaAlb��OH��c��CO3��dxH2O]�е�a��b��c��d�Ĵ�����ϵʽΪ ��
��3��Ϊȷ����ʽ̼����þ����ɣ���������ʵ�飺
��ȷ��ȡ3.390g��Ʒ������ϡ�����ַ�Ӧ������CO2 0.560L���ѻ���ɱ�״���£���
����ȡһ������Ʒ�ڿ����м��ȣ���Ʒ�Ĺ�������ʣ� ![]() ��100%�����¶ȵı仯��ͼ��ʾ����Ʒ��270��ʱ����ȫʧȥ�ᾧˮ��600�����ϲ�������Ϊ����������Ļ�����
��100%�����¶ȵı仯��ͼ��ʾ����Ʒ��270��ʱ����ȫʧȥ�ᾧˮ��600�����ϲ�������Ϊ����������Ļ�����
��������ʵ�����ݼ����ʽ̼����þ��Ʒ�е�n��OH������n��CO32������д��������̣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��CH3��CH�TCH2+HBr����CH3��CHBr��CH3����Ҫ�����1molij��A���ȼ�պ���Եõ�8mol CO2��4mol H2O������A�ڲ�ͬ�������ܷ�����ͼ��ʾ��һϵ�б仯�� 
��1��A�Ļ�ѧʽ�� �� A�Ľṹ��ʽ�� ��
��2��������Ӧ�У�������Ӧ��������Ӧ�����Ӧ���ͣ�
��3��д��C��D��E��H���ʵĽṹ��ʽ�� C �� D �� E �� H ��
��4��д��D����F��Ӧ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ�����
��1��ϡ���������þ��Ӧ��д�����ӷ���ʽ��
��2�������̼��������Һ��Ӧ��д�����ӷ���ʽ��
��3��Cu2++2OH��=Cu��OH��2����д����ѧ����ʽ��
��4���������������Ʊ���д����ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ��ͷ�����ʾ��ij�ֳ����Լ���ͨ�������£�������⣩����ת��������6��ת������һ��ʵ�ֵ�һ�������ǣ� ��
ѡ�� | W | X | Y | Z |
|
A | N2 | NH3 | NO | NO2 | |
B | Na | Na2O2 | NaOH | Na2CO3 | |
CC | Cu | CuSO4 | CuCl2 | Cu��OH��2 | |
D | Al | Al2��SO4��3 | AlCl3 | NaAlO2 |
A.A
B.B
C.C
D.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ɷ��Ǹ��л�ѧѧϰ���õķ���֮һ��ij��ѧ�о���ѧϰС����ѧϰ�ˡ���ѧ��Ӧԭ���������������µĹ����ܽ������ȷ���ǣ� �� ����0.1molL��1 CH3COOH��Һ�м������������ᣬƽ��������Ӧ�����ƶ�������̶����ڳ����£�pH=3�Ĵ�����Һ��pH=11��NaOH��Һ�������ϣ�����c��Na+��+c��H+��=c��OH����+c��CH3COO����
�۳����£�AgCl��ͬ���ʵ���Ũ�ȵ�CaCl2��NaCl��Һ�е��ܽ����ͬ���ܳ����£���֪�������ƽ�ⳣ��ΪKa�������ˮ��ƽ�ⳣ��ΪKh��ˮ�����ӻ�ΪKw�����У�KaKh=Kw ��
A.�٢ڢ�
B.�ڢ�
C.�ڢ�
D.�٢ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾA~E�������ʼ���ת����ϵ,����AΪ����ɫ����,BΪ���ʡ��ش���������:

��1��д�������ʵĻ�ѧʽ:A.___,B.___,C.____,D.____,E.____��
��2��д��B��C��D��E��Ӧ�����ӷ���ʽ:
B��C:____________________________________________________________;
D��E:____________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ��Ũ���ᷢ����Ӧ�Ļ�ѧ����ʽΪ��Cu +2H2SO4(Ũ)![]() CuSO4+SO2��+2H2O��������Ԫ�ر�________(����������������ԭ������ͬ)������__________��Ӧ��ŨH2SO4��_______��������___________�ԡ��ڸ÷�Ӧ�У���������32gCu����ת����_______mol ���� ��
CuSO4+SO2��+2H2O��������Ԫ�ر�________(����������������ԭ������ͬ)������__________��Ӧ��ŨH2SO4��_______��������___________�ԡ��ڸ÷�Ӧ�У���������32gCu����ת����_______mol ���� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com