
| A、每一条高分子链中都存在着化学键和分子间作用力 |
| B、它是线型结构 |
| C、网状结构中的高分子链间有化学键相互交联 |
| D、它的化学键键能特别大 |


 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:
| 物质(状态) | H2(g) | C2H4(g) | C2H3OH(l) |
| 燃烧热△H/kJ?mol-1 | -285.8 | -1411.0 | -1366.8 |
| A、-44.2kJ?mol-1 |
| B、+44.2kJ?mol-1 |
| C、-330kJ?mol-1 |
| D、+330kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
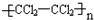 B.
B.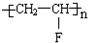 C.
C.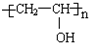
查看答案和解析>>
科目:高中化学 来源: 题型:
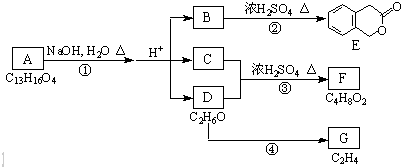
查看答案和解析>>
科目:高中化学 来源: 题型:
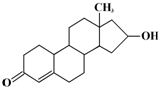 “诺龙”属于国际奥委会明确规定的违禁药品中合成代谢类的类固醇,其结构简式如图.下列关于“诺龙”的说法中不正确的是( )
“诺龙”属于国际奥委会明确规定的违禁药品中合成代谢类的类固醇,其结构简式如图.下列关于“诺龙”的说法中不正确的是( )| A、分子式是C18H26O2 |
| B、具有酚的化学性质 |
| C、具有烯的化学性质 |
| D、具有酮的化学性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
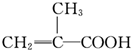 具有相同官能团的同分异构体的结构简式为
具有相同官能团的同分异构体的结构简式为 )有多种酯类的同分异构体.其中能与FeCl3溶液发生显色反应,且苯环上有2种一硝基取代物的同分异构体是
)有多种酯类的同分异构体.其中能与FeCl3溶液发生显色反应,且苯环上有2种一硝基取代物的同分异构体是查看答案和解析>>
科目:高中化学 来源: 题型:
| A、欲配制1.00 L 1.00 mol?L-1的NaCl溶液,可将58.5 g NaCl溶于1.00 L水中 |
| B、1 mol Cl2与足量的铁反应,转移的电子数为3NA |
| C、0.10mol Fe粉与足量水蒸气反应生成的H2分子数为0.10 NA |
| D、标准状况下,铝跟氢氧化钠溶液反应生成1 mol氢气时,转移的电子数为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com