
����Ŀ����ҩ����dz��������ҩ�������Ч�ɷ�Ϊ�����߰Ԫ F, ���������Ƹ�Ѫѹ�����ͷ�ۡ�ͷ�Ρ�ͻ���Զ�����֢���������� A Ϊ��ʼԭ�Ϻϳ�F ��һ�ַ�����

�ش��������⣺
(1) A �Ļ�ѧ����Ϊ________________��B����ʽΪ________________��
(2) C �й����ŵ�����Ϊ________ , C��D�ķ�Ӧ����Ϊ ______________��
(3)l molE ������_____________________molH2 �����ӳɷ�Ӧ��
(4) F ��NaOH ��Һ��Ӧ�Ļ�ѧ����ʽΪ ________________��
(5)B �ж���ͬ���칹�壬ͬʱ�������������Ĺ���________�֡�
�����ڷ����廯���� �ڿ���NaHCO3��Һ��Ӧ�ų� CO2����.���У��˴Ź���������4 ��壬�ҷ����֮��Ϊ1:2:6:1�Ľṹ��ʽΪ _________________��д��һ�ּ��ɣ���
(6)��֪��![]() д����AΪԭ���Ʊ�������
д����AΪԭ���Ʊ�������![]() �ϳ�·��____________________________ �������Լ���ѡ��
�ϳ�·��____________________________ �������Լ���ѡ��
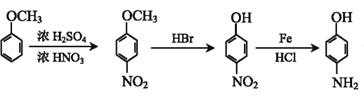
���𰸡������� C9H10O2 �Ȼ����Ѽ� ȡ����Ӧ 8 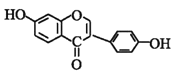 +2NaOH ��
+2NaOH ��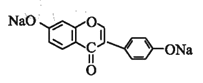 +2 H2O 14
+2 H2O 14 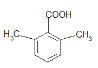 ��
�� 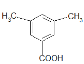 ��
�� 
��������
�л���AΪ![]() ����ѧ����Ϊ�����ѣ���������������[(AC)2O]��ZnCl2��Һ�����·�����λȡ������B��BΪ
����ѧ����Ϊ�����ѣ���������������[(AC)2O]��ZnCl2��Һ�����·�����λȡ������B��BΪ![]() ��B������Ϣ�еķ�Ӧ����
��B������Ϣ�еķ�Ӧ����![]() ��
��![]() ��
��![]() ����ȡ������D��DΪ
����ȡ������D��DΪ ��D������Ϣ�еķ�Ӧ���ɣ�E��HBr����ȡ������
��D������Ϣ�еķ�Ӧ���ɣ�E��HBr����ȡ������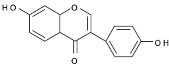 ���������Ϸ������
���������Ϸ������
(1)�ɷ�����֪��AΪ![]() ����ѧ����Ϊ�����ѣ�BΪ
����ѧ����Ϊ�����ѣ�BΪ![]() ������ʽΪC9H10O2��
������ʽΪC9H10O2��
(2��CΪ![]() ��������Ϊ�Ȼ����Ѽ���C��DΪ������ȡ����Ӧ��
��������Ϊ�Ȼ����Ѽ���C��DΪ������ȡ����Ӧ��
(3)EΪ![]() ��E���������������ֱ���3molH2�����ӳɷ�Ӧ��E�л���һ��̼̼˫����һ���ʻ����ֱ���1 molH2�����ӳɷ�Ӧ�����Թ�����8 molH2��
��E���������������ֱ���3molH2�����ӳɷ�Ӧ��E�л���һ��̼̼˫����һ���ʻ����ֱ���1 molH2�����ӳɷ�Ӧ�����Թ�����8 molH2��
(4)FΪ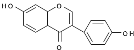 �������������ǻ������Ժ�NaOH ��Һ��Ӧ����ѧ����ʽΪ��
�������������ǻ������Ժ�NaOH ��Һ��Ӧ����ѧ����ʽΪ�� +2NaOH ��
+2NaOH �� +2H2O
+2H2O
(5)BΪ![]() ������ʽΪC9H10O2��B��ͬ���칹������ڷ����廯���˵����һ���������ڿ���NaHCO3��Һ��Ӧ�ų�CO2���壬����һ���Ȼ��������������̼ԭ�ӣ���һ������������Ϲ�����ȡ������һ���Ȼ������������������ڱ��������ڡ��䡢�����ֽṹ���Ȼ��������ֽṹ�зֱ���2��3��1�ֹ�6�ֽṹ���ڶ��������������������ȡ������һ���Ȼ���һ���һ������ڡ��䡢��3�ֽṹ�������������������������ȡ������һ������һ���Ȼ������Ǽ��ϣ����ڡ��䡢3�ֽṹ�������������ֻ��һ��ȡ������������һ���һ����Ȼ��ֱ������һ�������̼ԭ���ϣ���2�ֽṹ������6+3+3+2=14�֣��˴Ź���������4 ��壬�ҷ����֮��Ϊ1:2:6:1�Ľṹ��ʽӦ�������������Ǹ߶ȶԳƽṹ�����������Ľṹʽ�У�
������ʽΪC9H10O2��B��ͬ���칹������ڷ����廯���˵����һ���������ڿ���NaHCO3��Һ��Ӧ�ų�CO2���壬����һ���Ȼ��������������̼ԭ�ӣ���һ������������Ϲ�����ȡ������һ���Ȼ������������������ڱ��������ڡ��䡢�����ֽṹ���Ȼ��������ֽṹ�зֱ���2��3��1�ֹ�6�ֽṹ���ڶ��������������������ȡ������һ���Ȼ���һ���һ������ڡ��䡢��3�ֽṹ�������������������������ȡ������һ������һ���Ȼ������Ǽ��ϣ����ڡ��䡢3�ֽṹ�������������ֻ��һ��ȡ������������һ���һ����Ȼ��ֱ������һ�������̼ԭ���ϣ���2�ֽṹ������6+3+3+2=14�֣��˴Ź���������4 ��壬�ҷ����֮��Ϊ1:2:6:1�Ľṹ��ʽӦ�������������Ǹ߶ȶԳƽṹ�����������Ľṹʽ�У� ��
��  ��
��
(6)�����Ʒ�����������Ϣ��֪![]() �еķ��ǻ�����
�еķ��ǻ�����![]() ��HBr����ȡ�����ɣ���λ��-NH2����
��HBr����ȡ�����ɣ���λ��-NH2����![]() �ȷ������������������ٷ�����ԭ�õ������Ǹ���ת������������AΪԭ���Ʊ�������
�ȷ������������������ٷ�����ԭ�õ������Ǹ���ת������������AΪԭ���Ʊ�������![]() �ϳ�·��Ϊ��
�ϳ�·��Ϊ��
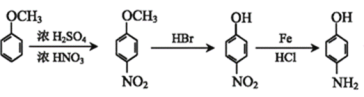 ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
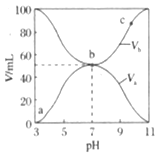
����Ŀ��25������20 mL 0.1 mol��L1 MOH��Һ�еμ�0.1 mol��L1 CH3COOH��Һ, ������Һ��pH(��Ӧ����M)����������(��Ӧ����N)�仯��ͼ��ʾ������������ȷ����
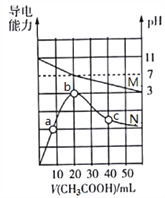
A. MOH�������Kb��1.0��1021
B. b����Һ�У�c(CH3COO)�� c(CH3COOH)��0.1 mol��L1
C. ˮ�����ӻ�����Kw��b��c��a
D. c����Һ�У�c(CH3COO)��c(M+)��c(H+)��c(OH)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����H2��O2��������Na2CO3���ȼ�ϵ�أ����õ�ⷨ�Ʊ� Fe(OH)2��װ������ͼ��ʾ�����е����������Ϸֱ�Ϊ����ʯī��ͨ��һ��ʱ����Ҳಣ�����в��������İ�ɫ������������˵����ȷ����
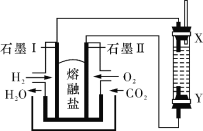
A. ʯī�缫�����ĵ缫��ӦʽΪO2+4e-=2O2-
B. X�����缫
C. ��������1mol Fe�ܽ⣬ʯī����H2 22.4 L
D. �������������ͨ���廥����X��Y��������Ҳ����, ʵ�鷽����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ϊ���¡���ѹ��������Ϊ���¡������������������о�����1 mol N2��3 mol H2����ʼʱ���������¶ȡ������ͬ��һ��ʱ���Ӧ�ﵽƽ�⣬Ϊʹ�������е�N2��ƽ�������е����ʵ���������ͬ�����д�ʩ�п��е��� ( )
A.��������г���һ�����ĺ���
B.���������г���һ������N2
C.�������������¶�
D.�����������ѹǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Դ�ǹ��ϵ���̼������Դ�����Ҵ�Ϊԭ�Ͽ�ͨ�����ַ������⣬���������Ӧ��ǰ�����ش��������⣺
��һ���Ҵ�����������
ԭ����C2H5OH(g)+3H2O(g)![]() 2CO2(g)+6H2(g)��H1
2CO2(g)+6H2(g)��H1
��Ni/����ʯ����������2L���������У��ֱ���ˮ����Ϊ2:1��4:1��6:1��8:1Ͷ�ϣ��Ҵ�����ʼ���ʵ�����ͬ������Ӧ��ͬʱ�����Ҵ�ת�������¶ȱ仯�Ĺ�ϵ��ͼ��ʾ��
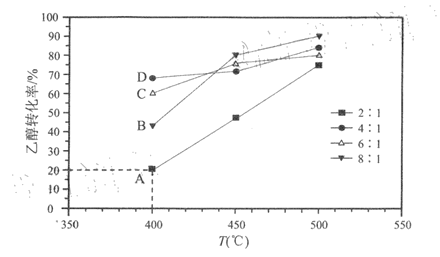
��֪�������ˮ���ӻ�ռ�ݴ����������λ�����·�Ӧ���ʽ��ͣ���ͼ��ˮ����Ϊ2:1ʱ��������Ѵﵽƽ��״̬��
(1)��Ӧ����H1________0(������������<��)�����Ҵ�����ʼ���ʵ���Ϊn0mol����K(400��)=______________���г�����ʽ����
(2)400��ʱ��ˮ���ȹ��߲������Ҵ�ת����ԭ����____________________________��B��C��D�����У�һ��δ�ﵽƽ��״̬����______________�����ţ���
�������Ҵ���������
ԭ����C2H5OH(g)+![]() O2(g)
O2(g)![]() 2CO2(g)+3H2(g) ��H2
2CO2(g)+3H2(g) ��H2
(3)��֪H2(g)+![]() O2(g)
O2(g)![]() H2O(g) ��H3������H2=_____(�ú���H1����H3��ʽ�ӱ�ʾ)�����ܱ�������ͨ��һ�������Ҵ����������ﵽƽ��״̬������������������������ƽ����Է���������_________����������������С������������)��
H2O(g) ��H3������H2=_____(�ú���H1����H3��ʽ�ӱ�ʾ)�����ܱ�������ͨ��һ�������Ҵ����������ﵽƽ��״̬������������������������ƽ����Է���������_________����������������С������������)��
�������Ҵ���ⷨ����
�Ҵ���ⷨ�������������Ҵ��������⣬�����Դ�ˮ�л���⣬�ҵ���Ҵ������ѹ�ȵ��ˮ�����۵�ѹҪ�ͺܶࡣ
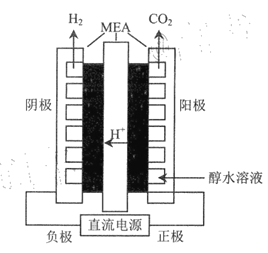
(4)������ͼ��ʾװ��(MEAΪ���ӵ�Ĥ�缫������Ҵ����⣬�����ĵ缫��ʽӦΪ___________��������ÿת��lmol���ӣ����Բ���________L��������״���£���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������м������ʣ��������Na2O����Na2O2����Al(OH)3����Na2CO3����H2O����CO2�����Ҵ�����Cu����NaOH��Һ��
��1���������ڵ���ʵ���___________����д��ţ���ͬ�������ڼ������������_______��
��2������ⷴӦ�����ӷ���ʽΪ______________________________________��
��3��Na2O2���ܷ������з�Ӧ��������������2Na2O2+2CO2=2Na2CO3+O2���÷�Ӧ�У��������뻹ԭ�������ʵ���֮��Ϊ��______��
��4�����ó������أ�KO2������������д������CO2��Ӧ�Ļ�ѧ����ʽ�����������ת�Ƶķ������Ŀ______________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ɫ��ѧʵ���������ã�ij��ѧ��ʦΪ������������Ʒ�Ӧ���������ͼ��ʾװ��������������صĿα�ʵ��������ȸ���Ԥ�ȣ��������ڳ�Բ��ʱ������ͨ�����������ɼ����Ż�ȼ�գ��������������̡����������������(����)
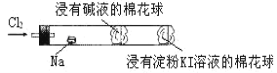
A.���Ż�ȼ�ղ�����ɫ���棬�����ɴ�������
B.���в���һ�Ž���NaOH��Һ���������������չ�������������������Ⱦ����
C.���Ҷ˽��е���KI��Һ��������ɫ�仯���ж������Ƿ�Һ��ȫ����
D.ʵ���������Ԫ��ԭ�Ӳ������DZ���ԭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ҵ��ˮ�д��ڴ�����Na+��Cl����Cu2+��SO42-������ȥ���е�Cu2+��SO42-����ƹ���������ͼ��ʾ��

����˵������ȷ����
A.NaOH�������dz�ȥCu2+B.�Լ�a ΪNa2CO3���Լ�bΪBaCl2
C.����ͼ�У�����xΪ����D.�Լ�cΪ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����Ũ�Ⱦ�Ϊ![]() ������ֱ�Ϊ
������ֱ�Ϊ![]() ��
��![]() ��
��![]() ��Һ��
��Һ��![]() ��Һ����ͬ����Ȼ�ϣ�����
��Һ����ͬ����Ȼ�ϣ�����![]() ��
��![]() ��
��![]() ����Һ��
����Һ��![]() �Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ� ��
�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ� ��
A. ![]()
B. b�㣬![]()
C. a��b��c���㣬c��ʱˮ�������![]() ���
���
D. ![]() ������У����ܴ���
������У����ܴ���![]()
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com