
| A. | pH=3的盐酸中,其c(H+)是pH=1的盐酸中的3倍 | |
| B. | 1mol/L0.5L的 AlCl3溶液中,阳离子的物质的量大于0.5mol | |
| C. | 同温度同物质的量浓度时,HF比HCN易电离,则NaF溶液的 pH 比 NaCN 溶液大 | |
| D. | 在由水电离出的c(H+)=1×10-12mol/L的溶液中,K+、ClO-、SO42-一定能大量共存 |
分析 A.溶液中c(H+)=10-pH;
B.氯化铝溶液中铝离子水解,阳离子物质的量增大;
C.酸越弱对应盐水解程度越大;
D.在由水电离出的c(H+)=1×10-12mol/L的溶液可能是酸或碱,抑制了水的电离.
解答 解:A.溶液中c(H+)=10-pH,pH=1的盐酸溶液中c(H+)=0.1mol/L,pH=3的盐酸中c(H+)=0.001mol/L,所以pH=1的盐酸中,其c(H+)是pH=3的盐酸的100倍,故A错误;
B.氯化铝溶液中铝离子水解,Al3++3H2O?Al(OH)3+3H+,1mol/L0.5L的 AlCl3溶液中,阳离子的物质的量大于0.5mol,故B正确;
C.同温度同物质的量浓度时,HF比HCN易电离,HF酸性大于HCN,则NaF溶液中氟离子水解程度比CN-离子水解程度小,所以溶液的 pH 比 NaCN 溶液小,故C错误;
D.在由水电离出的c(H+)=1×10-12mol/L的溶液可能是酸或碱,ClO-在酸溶液中不能大量共存,故D错误;
故选B.
点评 本题考查了弱电解质电离平衡、盐类水解、溶液酸碱性判断、离子共存的理解应用,注意水解过程中离子数目的变化,掌握基础是解题关键,题目难度中等.


 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:选择题
| A. | ①⑥⑦ | B. | ③⑥⑦ | C. | ③⑤⑦ | D. | ⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
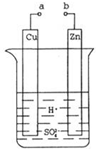 原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置.
原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2SO3溶液(BaCl2) | B. | FeCl2溶液(KSCN) | ||
| C. | 海带灰过滤所得的溶液(淀粉溶液) | D. | NaOH溶液(CaCl2) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3溶液和少量Ba(OH)2溶液混合:HCO3-+OH-+Ba2+═H2O+BaCO3↓ | |
| B. | 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH -═2 Al(OH)3↓+3BaSO4↓ | |
| C. | 向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- | |
| D. | 钠与CuSO4溶液反应:2Na+Cu2+═Cu↓+2Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
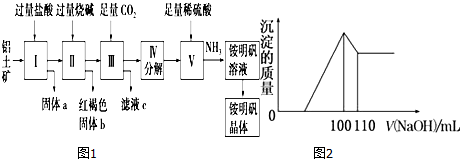
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com