
【题目】下列用电子式表示化合物的形成过程正确的是( )
A.![]()
B.![]()
C.![]()
D.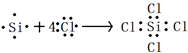
【答案】C
【解析】解:A.二氧化碳是氧原子和碳原子之间通过共价键形成的共价化合物,形成过程为: ![]() ,故A错误;B.硫化钠是硫离子和钠离子之间通过离子键形成的离子化合物,形成过程为:
,故A错误;B.硫化钠是硫离子和钠离子之间通过离子键形成的离子化合物,形成过程为: ![]() ,故B错误;
,故B错误;
C.H2O为共价化合物,各原子达到稳定结构,用电子式表示形成过程为 ![]() ,故C正确;
,故C正确;
D.四氯化硅中所有原子最外层都满足8电子稳定结构;用电子式表示四氯化硅的形成过程为: 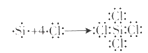 ,故D错误;
,故D错误;
故选:C.
A.二氧化碳是氧原子和碳原子之间通过共价键形成的共价化合物,存在C=O;
B.硫化钠为离子化合物,2个钠离子不能合写;
C.水为共价化合物,氧原子与两根氢原子分别共用1对电子;
D.四氯化硅中氯原子最外层有8个电子.


科目:高中化学 来源: 题型:
【题目】下列反应方程式书写正确的是( )
A.甲醛和足量银氨溶液充分反应:HCHO+2Ag(NH3)2++2O﹣ ![]() ?HCOO﹣+NH4++2Ag↓+H2O+3NH3
?HCOO﹣+NH4++2Ag↓+H2O+3NH3
B.往苯酚钠溶液中通入少量二氧化碳气体: ![]()
C.向盛有硫酸铜水溶液的试管里加入过量氨水:Cu2++4NH3?H2O═[Cu(NH3)4]2++4H2O
D.溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br﹣+Ag+═AgBr↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向a L密闭容器中加入1mol X气体和2mol Y气体,发生如下反应:X(g)+2Y(g)2Z(g),此反应达到平衡的标志是( )
A.容器内气体密度不随时间变化
B.v(X):v(Y)=1:2
C.容器内X、Y、Z的浓度不随时间变化
D.单位时间消耗0.1molX同时生成0.2molZ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是合成抗心律失常药物泰达隆的一种中间体,可通过以下方法合成: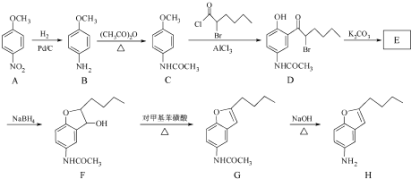
(1)D中的含氧官能团名称为(写两种).
(2)F→G的反应类型为 .
(3)写出同时满足下列条件的C的一种同分异构体的结构简式 .
①能发生银镜反应;
②能发生水解反应,其水解产物之一能与FeCl3溶液发生显色反应;
③分子中只有4种不同化学环境的氢.
(4)E经还原得到F,E的分子是为C14H17O3N,写出E的结构简式 .
(5)已知:①苯胺( ![]() )易被氧化
)易被氧化 ![]() 请以甲苯和(CH3CO)2O为原料制备
请以甲苯和(CH3CO)2O为原料制备 ![]() ,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干).
,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100mL FeI2溶液中逐渐通入Cl2 , 会依次生成Cl﹣、I2、Fe3+、IO3﹣ , 其中Fe3+、I2的物质的量随n(Cl2)的变化如图所示,请回答下列问题: 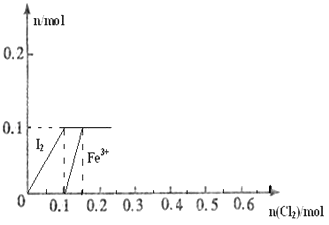
(1)由图可知,I﹣、Fe2+、I2三种粒子的还原性由强到弱的顺序为>> .
(2)当n(Cl2)=0.12mol时,溶液中的离子主要为 , 从开始通入Cl2到n(Cl2)=0.12mol时的总反应的化学方程式为 .
(3)当溶液中n(Cl﹣):n(IO3﹣)=8:1时,通入的Cl2在标准状况下的体积为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于碱金属元素的表述正确的是( )
A. 碱金属是对应周期中金属性最强的元素B. 从上至下单质氧化性逐渐减弱
C. Li、Na、K单质均应保存在煤油中D. Li、Na、K燃烧均生成过氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从能量的变化和反应的快慢等角度研究反应:2H2+O2=2H2O.
(1)为了加快反应速率,不可以采取的措施有(填序号,下同). A.使用催化剂 B.提高氧气的浓度
C.提高反应的温度 D.降低反应的温度
(2)已知该反应为放热反应,如图能正确表示该反应中能量变化的是 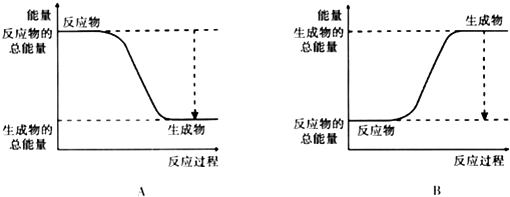
(3)从断键和成键的角度分析上述反应中能量的变化.已知化学键的键能如表:
化学键 | H﹣H | O=O | H﹣O |
键能kJmol﹣1 | 436 | 496 | 463 |
由此计算2mol H2在氧气中燃烧生成气态水放出的热量 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属的叙述中正确的是
A. 金属元素的原子只有还原性,离子只有氧化性
B. 含金属元素的离子不一定都是阳离子
C. “真金不怕火炼”是指金的熔点高
D. 金属元素单质在常温下均为固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能与SO2气体发生反应,但无沉淀产生的是
①氯水,②Ba(OH)2溶液,③石灰水,④Na2CO3溶液,⑤稀硫酸,⑥Na2SO3溶液。
A. 只有① B. ①③④ C. ④⑤⑥ D. ①④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com