
(15分)某学习小组依据反应:SO2(g)+ Cl2(g) SO2Cl2(g) △H<0,设计制备磺酰氯(SO2Cl2)的装置如下图,有关信息如下表所示。
SO2Cl2(g) △H<0,设计制备磺酰氯(SO2Cl2)的装置如下图,有关信息如下表所示。


(1)若用浓盐酸与二氧化锰为原料制取Cl2,反应的化学方程式为___________。
(2)B仪器的作用是________________。
(3)为了便于混合物的分离且提高反应物的转化率,A装置的反应条件最好选择_____。
a.冰水浴 b.常温 c.加热至69.1℃
(4)如果通入的Cl2或SO2含有水蒸气,氯气和二氧化硫可能发生反应的化学方程式为_____________。
(5)实验时先通入干燥的Cl2将A装置中的空气赶走,再缓慢通入干燥的SO2,即发生反应。充分反应后,继续通入Cl2使装置中的SO2进入烧杯中被吸收。分离产物后,向获得的SO2Cl2中加水,出现白雾,振荡、静置得到无色溶液W。
①经分析SO2Cl2与H2O反应属于非氧化还原反应,写出该反应的化学方程式___________。
②无色溶液W中的阴离子除含少量OH-外,还含有其它两种阴离子,检验溶液W中这两种阴离子方法是_______________________________________________。
③反应完成后,在W溶液、烧杯中分别滴加过量的BaCl2溶液,均出现白色沉淀,此沉淀不溶于稀盐酸,经过滤、洗涤、干燥,称量得到的固体质量分别为Xg、Yg。
(6)计算SO2+ Cl2 SO2Cl2反应中,SO2的转化率____________(用含X、Y的代数式表示)。
SO2Cl2反应中,SO2的转化率____________(用含X、Y的代数式表示)。
(1)MnO2 + 4HCl(浓) MnCl2 + Cl2 ↑+ 2H2O
MnCl2 + Cl2 ↑+ 2H2O
(2)冷凝SO2Cl2 (3)a
(4)SO2+Cl2+2H2O H2SO4+2HCl
H2SO4+2HCl
(5)① SO2Cl2+2H2O H2SO4+2HCl
H2SO4+2HCl
②取少量W溶液于试管中,加入过量Ba(NO3)2溶液,有不溶于稀硝酸的白色沉淀产生,说明溶液中含有SO42,过滤,向滤液中滴加HNO3酸化,再加入AgNO3溶液,产生白色沉淀,则说明溶液中有Cl
(6)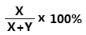
【解析】
试题分析:由图确定B起冷凝的作用,为了便于物质的分离,结合题给各种物质的熔沸点,及平衡角度,温度越低越有利于SO2Cl2生成,选择冰水浴更利于分离SO2Cl2,(5)通入的SO2,部分转化为SO2Cl2,部分被碱液吸收,结合SO2Cl2的性质,与水反应的方程式表示为SO2Cl2+2H2O H2SO4+2HCl,所得W溶液中除了还有OH-,还含有Cl-和SO42-,检验的方法为:取少量W溶液于试管中,加入过量Ba(NO3)2溶液,有不溶于稀硝酸的白色沉淀产生,说明溶液中含有SO42,过滤,向滤液中滴加HNO3酸化,再加入AgNO3溶液,产生白色沉淀,则说明溶液中有Cl。向W溶液和烧杯中溶液滴加过量的BaCl2溶液,均产生BaSO4沉淀,由元素守恒,SO2Cl2的S完全转化为BaSO4:关系为S ~ BaSO4,烧杯中的SO2先被氯气氧化为SO42-,再转化为BaSO4,关系亦为S
H2SO4+2HCl,所得W溶液中除了还有OH-,还含有Cl-和SO42-,检验的方法为:取少量W溶液于试管中,加入过量Ba(NO3)2溶液,有不溶于稀硝酸的白色沉淀产生,说明溶液中含有SO42,过滤,向滤液中滴加HNO3酸化,再加入AgNO3溶液,产生白色沉淀,则说明溶液中有Cl。向W溶液和烧杯中溶液滴加过量的BaCl2溶液,均产生BaSO4沉淀,由元素守恒,SO2Cl2的S完全转化为BaSO4:关系为S ~ BaSO4,烧杯中的SO2先被氯气氧化为SO42-,再转化为BaSO4,关系亦为S BaSO4,所以SO2的总量为(X+Y)/233g/mol,转化为SO2Cl2的SO2的量为X/233g/mol,则二氧化硫的转化率为
BaSO4,所以SO2的总量为(X+Y)/233g/mol,转化为SO2Cl2的SO2的量为X/233g/mol,则二氧化硫的转化率为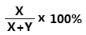 。
。
考点:物质的制备实验、反应条件的确定、物质间的反应及转化率的计算。
考点分析: 考点1:物质的制备 考点2:卤素 考点3:氧族元素 试题属性

科目:高中化学 来源:2014-2015四川省资阳市高一上学期学期期末化学试卷(解析版) 题型:选择题
在含有Fe3+、Fe2+、Al3+、Cl-的稀溶液中,加入足量的Na2O2固体,充分反应后再加入过量的稀盐酸,溶液中离子数目变化最小的是
A.Al3+ 、Cl- B.Al3+ C.Fe2+、Cl- D.Fe3+
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市高一上学期期末考试化学试卷(解析版) 题型:填空题
在25℃、100kPa条件下,将15L O2通入10L CO和H2的混合气中,使其完全燃烧,干燥后,恢复至原来的温度和压强。
(1)若剩余气体的体积是15L,则原CO和H2的混合气中:V(CO)= ___________L;V(H2)= ___________L。
(2)若剩余气体的体积为a L,求原混合气体中CO和H2的体积比。
(3)若剩余气体的体积为b L,计算b的取值范围。
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市高一上学期期末考试化学试卷(解析版) 题型:选择题
已知一个SO2分子的质量为n kg,一个SO3分子的质量为m kg(设两种分子中S、O原子分别具有相同的中子数),若以硫原子质量的1/32作标准,SO2的相对分子质量为
A. B.
B. C.
C. D.
D.
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市高一上学期期末考试化学试卷(解析版) 题型:选择题
支持固态氨是分子晶体的事实是
A.氮原子不能形成阳离子 B.氢离子不能单独存在
C.常温下氨是气态物质 D.氨极易溶于水
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市石景山区高三一模理综化学试卷(解析版) 题型:选择题
用右图所示装置检验对应气体时,不能达到目的的是

生成的气体 | 试剂X | 试剂Y | |
A | 电石与水反应制取的乙炔 | CuSO4溶液 | Br2的CCl4溶液 |
B | 木炭与浓H2SO4加热制取的二氧化碳 | 饱和NaHCO3溶液 | 澄清石灰水 |
C | CH3CH2Br与NaOH乙醇溶液共热制取的乙烯 | 水 | KMnO4酸性溶液 |
D | C2H5OH与浓H2SO4加热至170℃制取的乙烯 | NaOH溶液 | Br2的CCl4溶液 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市丰台区高三一模理综化学试卷(解析版) 题型:实验题
(14分)铁及其化合物在日常生活中有广泛应用。
(1)写出Fe(OH)2转化为Fe(OH)3的化学方程式 。
(2)绿矾(FeSO4·7H2O)是补血剂的原料,易变质。检验绿矾是否变质的试剂是
设计实验检验绿矾是否完全变质
(3)利用绿矾制备还原铁粉的工业流程如下:

①干燥过程主要是为了脱去游离水和结晶水,过程中会有少量FeCO3·nH2O在空气中被氧化为FeOOH,该反应的化学方程式为
②取干燥后的FeCO3样品12.49g ,焙烧,最终得到还原铁粉6.16g,计算样品中杂质FeOOH的质量
(4)以羰基化合物为载体运用化学平衡移动原理分离、提纯某纳米级活性铁粉(含有一些不反应的杂质),反应装置如下图。
Fe(s)+5CO(g) 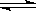 Fe(CO)5(g) ΔH<0
Fe(CO)5(g) ΔH<0

T1 T2(填“>”、“<”或“=”),判断理由是
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三第二次模拟理综化学试卷(解析版) 题型:选择题
下列说法不正确的是
A. 的分子式为C17H24O3
的分子式为C17H24O3
B.结构为…—CH=CH—CH=CH—CH=CH—CH=CH—…的高分子化合物,其单体是乙炔
C.有机硅聚醚( )可由单体
)可由单体 和
和 缩聚而成
缩聚而成
D.等质量的甲醇、甲醛、甲醚完全燃烧时的耗氧量依次递增
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com