
【题目】如图所示,甲池的总反应式为N2H4+O2===N2+2H2O。下列说法正确的是( )
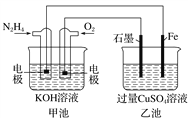
A. 甲池中负极上的电极反应式为N2H4-4e-===N2+4H+
B. 乙池中石墨电极上发生的反应为4OH--4e-===2H2O+O2↑
C. 甲池溶液pH增大,乙池溶液pH减小
D. 甲池中每消耗0.1 mol N2H4乙池电极上则会析出6.4 g固体
【答案】B
【解析】A项,甲池为原电池,由总反应式可得,通N2H4的电极为负极,发生失电子氧化反应生成N2,电解质溶液为KOH溶液,所以负极上的电极反应式为:N2H4+4OH--4e-=N2+4H2O,故A错误;B项,乙池为电解池,石墨电极为阳极,发生失电子氧化反应,电解质溶液为硫酸铜溶液,所以石墨电极上发生的反应为2H2O-4e-=4H++O2↑,故B正确;C项,乙池总反应为:2CuSO4+2H2O![]() 2Cu+2H2SO4+O2↑,因生成硫酸,所以酸性增强,pH减小,由甲池总反应N2H4+O2=N2+2H2O可得,若忽略生成的水造成的溶液体积增大,则碱性不变,pH不变,若考虑生成的水造成的溶液体积增大,则碱性减弱,pH减小,故C错误;D项,由N2H4+4OH--4e-=N2+4H2O得,甲池中每消耗0.1molN2H4失去0.4mol电子,乙池析出Cu的反应为:Cu2++2e-=Cu,串联电路中根据得失电子守恒可得,生成0.2molCu,质量为12.8g,故D错误。
2Cu+2H2SO4+O2↑,因生成硫酸,所以酸性增强,pH减小,由甲池总反应N2H4+O2=N2+2H2O可得,若忽略生成的水造成的溶液体积增大,则碱性不变,pH不变,若考虑生成的水造成的溶液体积增大,则碱性减弱,pH减小,故C错误;D项,由N2H4+4OH--4e-=N2+4H2O得,甲池中每消耗0.1molN2H4失去0.4mol电子,乙池析出Cu的反应为:Cu2++2e-=Cu,串联电路中根据得失电子守恒可得,生成0.2molCu,质量为12.8g,故D错误。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述中,正确的是
A. 制取及观察Fe(OH)2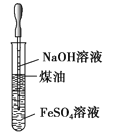
B. 比较两种物质的热稳定性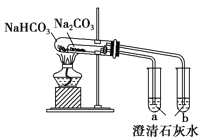
C. 实验室制取NH3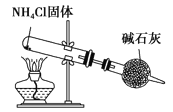
D. 分离沸点不同且互溶的液体混合物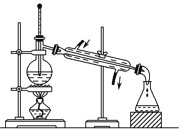
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中可用如下反应制取氯气:2KMnO4+16HCl(浓)= 2KCl+2MnCl2+5Cl2↑+8H2O,此反应中氧化剂与还原剂的物质的量之比为( )
A.1:8B.1:5C.2:5D.5:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将以下4份溶液分别置于如图的装置中,其他条件相同时,灯泡最亮的是( )
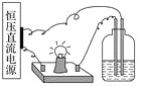
A. 100 mL 1 mol·L-1的盐酸
B. 100 mL 2 mol·L-1的蔗糖溶液
C. 100 mL 1 mol·L-1的氯化钠溶液
D. 30 mL 1 mol·L-1的氯化钙溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电化学装置的说法正确的是
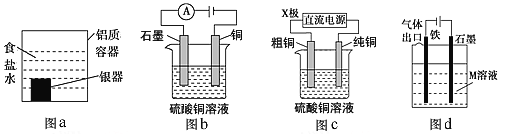
A. 利用图a装置处理银器表面的黑斑Ag2S,银器表面的反应为Ag2S+2e-=2Ag+S2-
B. 图b电解一段时间,铜电极溶解,石墨电极上有亮红色物质析出
C. 图c中的X极若为负极,则该装置可实现粗铜的精炼
D. 图d中若M是海水,该装置是通过“牺牲阳极的阴极保护法”使铁不被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
A.所用NaOH已吸潮
B.配制溶液时容量瓶中残留少量蒸馏水
C.有少量NaOH溶液残留在烧杯内
D.向容量瓶加水时眼睛一直俯视液面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的电离过程为H2O![]() H++OH-,在25℃、35℃时其离子积分别为K(25℃)=1.0×10-14、K(35℃)=2.1×10-14,则下列说法中正确的是
H++OH-,在25℃、35℃时其离子积分别为K(25℃)=1.0×10-14、K(35℃)=2.1×10-14,则下列说法中正确的是
A. 在35℃时,纯水中c(H+)>c(OH-) B. c(H+)随着温度的升高而降低
C. 水的电离过程是吸热过程 D. 水的电离度α(25℃)>α(35℃)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中和热的测定实验(如图)。
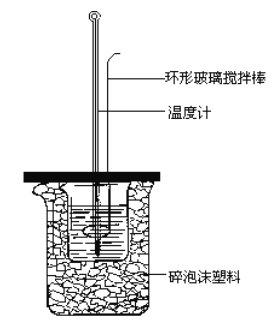
(1)量取反应物时,取50mL0.50mol·L-1的盐酸,还应加入的试剂是______(填序号)。
A.50mL0.50mol·L-1NaOH溶液 B.50mL0.55mol·L-1NaOH溶液 C.1.0gNaOH固体
(2)在实验过程中,该同学需要测定并记录的实验数据有____(填序号)。
A.盐酸的浓度 B.盐酸的温度 C.氢氧化钠溶液的浓度 D.氢氧化钠溶液的温度E.水的比热容 F.反应后混合溶液的终止温度
(3)测得(1)放出1.43kJ的热量,则表示该反应中和热的热化学方程式是___________________________________。
(4)实验中若用60mL0.5mol·L-1盐酸溶液跟50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量______ (填“相等”、“不相等”),所求中和热_______ (填“相等”、“不相等”);
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com