
����Ŀ���к��ȵIJⶨʵ�飨��ͼ����
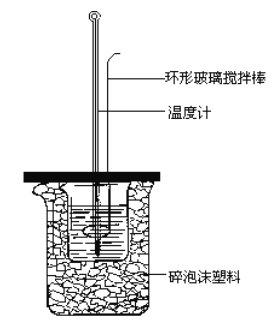
��1����ȡ��Ӧ��ʱ��ȡ50mL0.50mol��L-1�����ᣬ��Ӧ������Լ���______������ţ���
A��50mL0.50mol��L-1NaOH��Һ B��50mL0.55mol��L-1NaOH��Һ C��1.0gNaOH����
��2����ʵ������У���ͬѧ��Ҫ�ⶨ����¼��ʵ��������____������ţ���
A�������Ũ�� B��������¶� C������������Һ��Ũ�� D������������Һ���¶�E��ˮ�ı����� F����Ӧ������Һ����ֹ�¶�
��3�������1���ų�1.43kJ�����������ʾ�÷�Ӧ�к��ȵ��Ȼ�ѧ����ʽ��___________________________________��
��4��ʵ��������60mL0��5mol��L��1������Һ��50mL0��55mol��L��1NaOH��Һ���з�Ӧ��������ʵ����ȣ����ų�������______ �����ȡ���������ȡ����������к���_______ �����ȡ���������ȡ�����
���𰸡� B B D F NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)��H=57.2kJ/mol ����� ���
�����������������������Ҫ�о�����к��ȵIJⶨ���ص㿼���к��Ȳⶨ�������Ȼ�ѧ����ʽ��д��ʵ���������Ȼ���֪ʶ�ͻ������ܣ����鿼���ԡ��к�����������������ʵ���ۺϷ���������
��������1���к�����ǿ��ǿ��ϡ��Һ��ȫ��Ӧ����1molҺ̬ˮʱ�ͷŵ����������Բ���ѡ��NaOH���壬ͬʱΪ��ȷ��HCl��ȫ��Ӧ�������Ҫ�����Թ�����NaOHϡ��Һ������ѡ��B�𰸡���ȷ�𰸣�B����2��ʵ������г��˸���������ϡ��Һ��Ũ�Ⱥ�����⣬��Ҫ�����ͼ�¼�����ݰ���ϡ�����ϩNaOH��Һ����ʼ�¶ȡ�ʵ�����������������¶ȡ���ȷ�𰸣�BDF����3������ʵ����֪������ϡ��ҺŨ�Ⱥ������֪����Ӧ����Һ̬ˮ0.025mol����˷�Ӧ����1molҺ̬ˮʱ�ͷŵ�����Ϊ1.43kJ��0.025mol=57.2 kJ/mol �����Ա�ʾ�÷�Ӧ�к��ȵ��Ȼ�ѧ����ʽ��NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)��H=57.2kJ/mol ����ȷ�� ��NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)��H=57.2kJ/mol����4��������60mL0��5mol��L��1������Һ��50mL0��55mol��L��1NaOH��Һ���з�Ӧ��ʱ���μӷ�Ӧ�ķ�Ӧ����࣬����ͷŵ��������࣬�����������վ�������1molҺ̬ˮ�����к��ȣ������к��Ȳ��䡣��ȷ�𰸣�����ȡ���ȡ�


 ��ǰ����ϵ�д�
��ǰ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ���׳ص��ܷ�ӦʽΪN2H4��O2===N2��2H2O������˵����ȷ����(����)
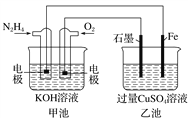
A. �׳��и����ϵĵ缫��ӦʽΪN2H4��4e��===N2��4H��
B. �ҳ���ʯī�缫�Ϸ����ķ�ӦΪ4OH����4e��===2H2O��O2��
C. �׳���ҺpH�����ҳ���ҺpH��С
D. �׳���ÿ����0.1 mol N2H4�ҳص缫���������6.4 g����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.2molMn02��50mL12mol/L�����Ϻ���ȣ���Ӧ��ȫ�������µ���Һ�м�������AgNO3��Һ������AgCl�������ʵ���Ϊ������������Ļӷ����� ��
A. ����0.3mol B. ��0.3mol C. ���� 0.3mol���� 0.6mol D. ���� 0.6mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ȷ����(����)
A. �����۵�ĸߵͣ�
B. �۵��ɸߵ��ͣ�Na>Mg>Al
C. Ӳ���ɴ�С�����ʯ>̼����>�����
D. �������ɴ�С��NaF>NaCl>NaBr>NaI
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ�ֳ����ĵ��ʣ��ҡ���Ϊ��ѧ�����Ļ�����ס��ҡ���������Ԫ�� X �����������µ�ת����ϵ�����ֲ��P��Ӧ��������ȥ���������ж���ȷ����:
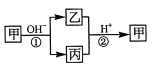
A�� XԪ�ؿ���ΪAl B�� X Ԫ�ز�һ��Ϊ�ǽ���Ԫ��
C����Ӧ��������Ϊ���淴Ӧ D����Ӧ������һ��Ϊ������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������Լ��Ϳ��Լ����NaOH����H2SO4����CuSO4����NaCl�������ʵ���Һ�������ȼ��������������( )
A.��B.��C.��D.��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ںϽ����������ȷ����( )
A.�Ͻ�һ���������ֻ���ֽ����ۺ϶��ɵ�
B.�ճ��������õ������Ӳ������ͭ�Ͻ�
C.���Ͻ��Ӳ�ȱ����Ĵ��۵�����ĸ�
D.�̴���˾ĸ�춦���ɴ�ͭ������ɵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���̼���ƺ�̼�����Ƶ�˵������ȷ����
A.̼���Ƶ����ȶ��Ա�̼������ǿ
B.��ͬ�¶�ʱ��̼���Ƶ��ܽ�ȴ���̼������
C.ͬ�¶ȡ�ͬ���ʵ���Ũ��ʱ��̼������Һ���Դ���̼��������Һ
D.̼������һ�������¿�ת��Ϊ̼���ƣ���̼���Ʋ���ת��Ϊ̼������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij��ɫ��Һ�л����ص���NaOH��Һֱ����������������������������NaOH��Һ����Ĺ�ϵ����ͼ��ʾ���ɴ�ȷ����ԭ��Һ�к��е���������
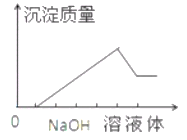
A. Mg2+��Al3+��Fe3+ B. H+��Mg2+��Al3+
C. H+��Ba2+��Al3+ D. ֻ��Mg2+��Al3+
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com