
(13分)碳氧化物、氮氧化物、二氧化硫的处理与利用是世界各国研究的热点问题。
(1)消除汽车尾气中的NO、CO,有利于减少PM2.5的排放。已知如下信息:
I.
II.N2(g)+ O2(g)  2NO(g) ΔH1
2NO(g) ΔH1
2CO(g) + O2(g) 2CO2 (g) ΔH2= -565 kJ·mol-1
2CO2 (g) ΔH2= -565 kJ·mol-1
①ΔH1= 。
②在催化剂作用下NO和CO转化为无毒气体,写出反应的热化学方程式
③一定条件下,单位时间内不同温度下测定的氮氧化物转化率如图1所示。
温度高于710K时,随温度的升高氮氧化物转化率降低的原因可能是

(2)测定汽车尾气常用的方法有两种。
①方法1:电化学气敏传感器法。其中CO传感器的工作原理如图2所示,则工作电极的反应式为
②方法2:氧化还原滴定法。用H2O2溶液吸收尾气,将氮氧化物转化为强酸,用酸碱中和滴定法测定强酸浓度。写出NO与H2O2溶液反应的离子方程式
(3)工业上可以用NaOH溶液或氨水吸收过量的SO2,分别生成NaHSO3、NH4HSO3,其水溶液均呈酸性。相同条件下,同浓度的两种酸式盐的水溶液中c(SO32-)较小的是,用文字和化学用语解释原因 。
(13分,未标分数的空每空2分,合理即给分)
(1)① +183kJ·mol-1
②2CO(g)+2NO(g) 2CO2 (g)+N2 (g) ΔH=-748 kJ·mol-1
2CO2 (g)+N2 (g) ΔH=-748 kJ·mol-1
③温度升高到710K时,单位时间内反应达平衡,该反应是放热反应,升高温度,平衡向左移动,转化率降低
(2)①CO-2e-+H2O CO2+2H+
CO2+2H+
②2NO+3H2O2 2NO3-+2H2O+2H+
2NO3-+2H2O+2H+
(3)NH4HSO3(1分)
HSO3- H+ +SO32-,NH4+水解使c(H+)增大,电离平衡逆向移动,c(SO32-)浓度减小。
H+ +SO32-,NH4+水解使c(H+)增大,电离平衡逆向移动,c(SO32-)浓度减小。
【解析】
试题分析:(1)①化学反应的焓变等于反应物的键能之和减去生成物的键能之和,根据信息Ⅰ中的数据计算反应N2(g)+ O2(g)  2NO(g)的ΔH1=+183kJ·mol-1。②在催化剂作用下NO和CO转化为无毒气体N2和CO2,利用信息II.i N2(g)+ O2(g)
2NO(g)的ΔH1=+183kJ·mol-1。②在催化剂作用下NO和CO转化为无毒气体N2和CO2,利用信息II.i N2(g)+ O2(g)  2NO(g) ΔH1=+183kJ·mol-1,ii 2CO(g) + O2(g)
2NO(g) ΔH1=+183kJ·mol-1,ii 2CO(g) + O2(g) 2CO2 (g) ΔH2= -565 kJ·mol-1,根据盖斯定律:ii—i得反应的热化学方程式为2CO(g)+2NO(g)
2CO2 (g) ΔH2= -565 kJ·mol-1,根据盖斯定律:ii—i得反应的热化学方程式为2CO(g)+2NO(g) 2CO2 (g)+N2 (g) ΔH=-748 kJ·mol-1;③温度高于710K时,随温度的升高氮氧化物转化率降低的原因可能是温度升高到710K时,单位时间内反应达平衡,该反应是放热反应,升高温度,平衡向左移动,转化率降低。(2)①CO传感器的工作原理为酸性CO燃料电池,CO发生氧化反应,在原电池的负极参加反应,电极反应式为CO-2e-+H2O
2CO2 (g)+N2 (g) ΔH=-748 kJ·mol-1;③温度高于710K时,随温度的升高氮氧化物转化率降低的原因可能是温度升高到710K时,单位时间内反应达平衡,该反应是放热反应,升高温度,平衡向左移动,转化率降低。(2)①CO传感器的工作原理为酸性CO燃料电池,CO发生氧化反应,在原电池的负极参加反应,电极反应式为CO-2e-+H2O CO2+2H+,O2发生还原反应,作正极,电极反应式为O2+4e-+4H+==2H2O;② NO与H2O2溶液反应生成硝酸和水,离子方程式为2NO+3H2O2
CO2+2H+,O2发生还原反应,作正极,电极反应式为O2+4e-+4H+==2H2O;② NO与H2O2溶液反应生成硝酸和水,离子方程式为2NO+3H2O2 2NO3-+2H2O+2H+;(3)相同条件下,同浓度的NaHSO3、NH4HSO3的水溶液中c(SO32-)较小的是NH4HSO3,原因HSO3-
2NO3-+2H2O+2H+;(3)相同条件下,同浓度的NaHSO3、NH4HSO3的水溶液中c(SO32-)较小的是NH4HSO3,原因HSO3- H+ +SO32-,NH4+水解使c(H+)增大,电离平衡逆向移动,c(SO32-)浓度减小。
H+ +SO32-,NH4+水解使c(H+)增大,电离平衡逆向移动,c(SO32-)浓度减小。
考点:考查反应热的计算、盖斯定律,化学平衡,燃料电池及电解质溶液中的离子平衡。
考点分析: 考点1:化学反应与能量 考点2:化学平衡状态及移动 考点3:盐类水解 试题属性

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015四川省资阳市高二上学期学期期末化学试卷(解析版) 题型:填空题
(5分)已知下列反应的反应热为
① CH3COOH(l)+2O2(g) = 2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol
② H2(g)+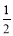 O2(g) = H2O(l) ΔH2=-285.8 kJ/mol
O2(g) = H2O(l) ΔH2=-285.8 kJ/mol
(1)已知1.2 g固体C充分燃烧生成CO2放出热量为39.35 kJ,请写出C的燃烧热化学方程式(碳的燃烧热用ΔH3表示): ;
(2)计算反应:2C(s)+2H2(g)+O2(g) = CH3COOH(l)的反应热ΔH。(要有计算过程)
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市高一上学期期末考试化学试卷(解析版) 题型:选择题
化学反应的离子方程式正确的是
A.醋酸溶液与NaOH反应:OH-+H+→H2O
B.硝酸溶液和碳酸氢钠反应:H++2CO32-→CO2↑+H2O
C.将溴水加入KI溶液中:Br2+2I-→I2+2Br-
D.CO2通入澄清石灰水:2OH-+CO2→H2O+CO32-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市石景山区高三一模理综化学试卷(解析版) 题型:实验题
(13分)孔雀石主要成分是Cu2(OH)2CO3,还含少量FeCO3及Si的化合物,实验室以孔雀石为原料制备硫酸铜晶体的步骤如下:

(1)步骤Ⅰ中涉及的反应用离子方程式表示为_____________________________。
(2)步骤Ⅱ中试剂①是__________(填代号)。
a.KMnO4 b.H2O2 c.Fe粉 d.KSCN
(3)步骤Ⅲ加入CuO的目的是___________________________。
(4)步骤Ⅳ获得硫酸铜晶体,需要经过_________、_________、过滤等操作。
(5)孔雀石与焦炭一起加热可以生成Cu及其它无毒物质,写出该反应的化学方程式_____________。
(6)测定硫酸铜晶体(CuSO4·xH2O)中结晶水的x值:称取2.4g硫酸铜晶体,加热至质量不再改变时,称量粉末的质量为1.6g。则计算得x=______(计算结果精确到0.1)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市石景山区高三一模理综化学试卷(解析版) 题型:选择题
下列有关海水综合利用的说法中,不正确的是
A.用氯气从海水中提溴的关键反应是:Cl2+2Br—===2Cl—+Br2
B.海水中含有钾元素,只需经过物理变化就可以得到钾单质
C.海水中的Na+、Cl—结晶成NaCl的过程,形成了化学键
D.从海水中可以得到氯化镁,再经过电解可制金属镁
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市丰台区高三一模理综化学试卷(解析版) 题型:选择题
X、Y、Z为短周期非金属元素,其相关性质如下,下列叙述正确的是
元素 | X | Y | Z |
单质与H2反应条件 | 暗处爆炸 | 光照 | 高温、高压、催化剂 |
常温下氢化物水溶液的pH | 小于7 | 小于7 | 大于7 |
A.Z的氢化物分子间存在氢键 B.最外层电子数Z>Y
C.气态氢化物的稳定性Y>X D.Y的含氧酸均为强酸
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三第二次模拟理综化学试卷(解析版) 题型:推断题
(10分)某科研小组利用石油分馏产品经下列路线,合成一种新型香料。
已知X分子中碳氢质量比为24:5,A、E都是X的裂解产物,且二者互为同系物,D与饱和NaHCO3溶液反应产生气体。

信息提示:卤代烃在强碱水溶液中发生水解(取代)反应生成醇。如:

(1)X分子为直链结构,X的名称为 ;C中官能团的名称为 。
(2)①—⑥的反应中,下列反应类型存在且数目由多到少的是 。(用字母和“﹥”写出)
A.加成反应 B.加聚反应 C.取代反应 D.氧化反应
(3)B与D在浓硫酸作用下,生成甲,则与甲同类别的同分异构体的有 种(不包括甲)。
(4)写出⑥的化学反应方程式 。
(5)E可能发生下列选项中的某种反应,写出能反应的化学方程式 。
A.皂化反应 B.与乙酸的酯化反应
C.加聚反应 D.与银氨溶液的银镜反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省西安市高三下学期第一次月考理综化学试卷(解析版) 题型:选择题
下列根据实验操作和现象所得出的结论正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向硅酸钠溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去 | 2 min后,试管里出现凝胶 | 稳定性:盐酸>硅酸 |
B | 向某溶液中先滴加KSCN溶液,再滴加少量氯水 | 先无明显现象,后溶液变成血红色 | 溶液中含有Fe3+,没有Fe2+ |
C | 常温下,向浓硫酸中投入铁片 | 铁片不溶解 | 常温下,铁不与浓硫酸反应 |
D | 向盛有碘水的试管中加入CCl4后充分振荡静置 | 液体分层,上层基本无色,下层紫色 | 碘在CCl4中的溶解度较大 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省湛江市高三高考测试(一)理综化学试卷(解析版) 题型:选择题
水溶液中能大量共存的一组离子是
A.Ca2+、H+、Cl-、HCO3- B.H+、K+、S2-、ClO-
C.Fe2+、Na+、SO42-、NO3- D.Cu2+、Ag+、SO42- 、OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com