
【题目】在b L Al2(SO4)3和(NH4)2SO4的混合溶液中加入a mol BaCl2,恰好使溶液中的SO42-﹣离子完全沉淀;如加入足量强碱并加热可得到c mol NH3,则原溶液中的Al3+浓度(mol/L)为
A. (2a-c)/b B. (2a-c)/2b C. (2a-c)/3b D. (2a-c)/6b
【答案】C
【解析】
根据SO42-+Ba2+=BaSO4↓计算溶液中的SO42-离子的物质的量,根据NH4++OH-![]() NH3↑+H2O计算NH4+的物质的量,再根据c=n/V计算SO42-离子、NH4+离子浓度,再利用电荷守恒计算原溶液中的Al3+浓度。
NH3↑+H2O计算NH4+的物质的量,再根据c=n/V计算SO42-离子、NH4+离子浓度,再利用电荷守恒计算原溶液中的Al3+浓度。
向bL混合溶液中加入amolBaCl2,恰好使溶液中的SO42-离子完全沉淀,则根据SO42-+Ba2+=BaSO4↓可知c(SO42-)=a/b mol/L。向bL混合溶液中加入足量强碱并加热可得到cmolNH3,则根据NH4++OH-![]() NH3↑+H2O可知c(NH4+)=c/b mol/L。又溶液显电性,设原溶液中的Al3+浓度为x,如果忽略水的电离,则由电荷守恒可知x×3+c/b mol/L×1=a/b mol/L×2,解得x=(2a-c)/3b mol/L,答案选C。
NH3↑+H2O可知c(NH4+)=c/b mol/L。又溶液显电性,设原溶液中的Al3+浓度为x,如果忽略水的电离,则由电荷守恒可知x×3+c/b mol/L×1=a/b mol/L×2,解得x=(2a-c)/3b mol/L,答案选C。


科目:高中化学 来源: 题型:
【题目】生物界和非生物界具有统一性是因为
A. 构成细胞的各种化合物在非生物中都存在
B. 生物界和非生物界都具有新陈代谢
C. 构成细胞的无机物在非生物界是都存在
D. 构成细胞的各种化学元素在无机自然界中都能找到
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】4 ℃下,把质量A g摩尔质量为M g·mol-1的可溶性盐RCln 溶解在V mL水中,恰好形成该温度下的饱和溶液,密度为ρ g·cm-3,下列关系式错误的是
A. 溶质的质量分数ω=A/(A+V)×100%
B. 溶质的物质的量浓度c=1 000ρ A/(MA+MV) mol·L-1
C. 该温度下此盐的溶解度S=100A/V g
D. 1 mL该溶液中n(Cl-)=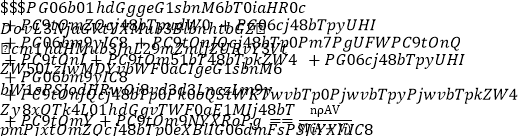 mol
mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将13.0 g锌投入250mL某浓度的盐酸中,锌和盐酸恰好完全反应。求:
(1)反应中生成的H2在标准状况下的体积。__
(2)所用盐酸中HCl的物质的量浓度。_____________
(3)需用多少体积的36.5%的浓盐酸(ρ =1.20 g/mL)来配置上述盐酸。_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Ba(OH)2和NaOH的混合溶液中逐渐通入CO2气体至过量,生成沉淀的物质的量(n)和通入CO2气体的(V) 的关系如图所示,试回答:

(1)0到a点之间的反应的离子方程式__________
(2)a到b点之间的反应的离子方程式__________
(3)b点之后的反应的离子方程式______________
(4)c 点CO2的体积__________mL(同温同压下)。
(5) 混合溶液中Ba(OH)2和NaOH 的物质的量之比为__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用混有硫酸亚铁和硫酸镁等杂质的锰矿(含MnO2、MnCO3)生产硫酸锰,实验室模拟生产过程如下:
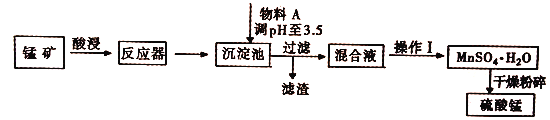
(完全沉淀离子的pH值:Fe3+为3.5,Fe2+为9.5,Mn2+为10.8,Mg2+为11.6)
(1)酸浸中加入的酸是________(填化学式,下同),提高酸浸速率的方法是____(任写一种),从经济效益考虑,物料A可能是___________。
(2)反应器中发生氧化还原反应的离子方程式是___________________ 。
(3)硫酸锰和硫酸镁的溶解度曲线如图所示:
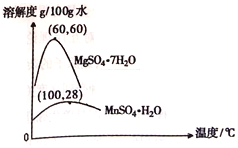
①操作I为:在_____℃下蒸发结晶、趁热过滤。其趁热过滤目的是__________;
②为了得到更纯净的一水合硫酸锰,需将晶体置于过滤器中,用_____进行洗涤(本空格从以下选择)
a.蒸馏水 b.稀硫酸 c.饱和硫酸锰溶液 d.氢氧化钠溶液
(4)MnSO4·H2O在1150℃高温下易分解,产物是Mn304、含硫化合物、水,在该条件下硫酸锰晶体分解反应的化学方程式是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是由4个碳原子结合成的6种有机物(氢原子没有画出)
![]()
(1) 写出有机物(a)的系统命名法的名称___________________。
(2) 有机物(a)有一种同分异构体,试写出其结构简式__________________。
(3) 上述有机物中与(c)互为同分异构体的是________(填代号)。
(4) 任写一种与(e)互为同系物的有机物的结构简式____________。
(5) 上述有机物中不能与溴反应并使其褪色的有________(填代号)。
(6) (a)(b)(c)(d)四种物质中,4个碳原子一定处于同一平面的有________(填代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:2Zn(s) + O2(g) =2ZnO(s) ΔH1=-702.2kJ/mol
Hg(l) + ![]() O2(g) =HgO(s) ΔH2=-90.7kJ/mol
O2(g) =HgO(s) ΔH2=-90.7kJ/mol
由此可知Zn(s) + HgO(s) = ZnO(s) + Hg(l)的ΔH3 ,其中ΔH3的值是( )
A. -260.4 kJ/mol B. -254.6 kJ/mol
C. -438.9 kJ/mol D. -441.8 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制溴苯可用如图装置。请回答下列问题:
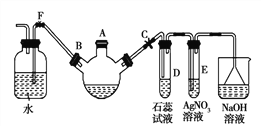
(1)关闭F夹,打开C夹,向装有少量苯的三口烧瓶的A口加少量溴,再加少量铁屑,塞住A口,则三口烧瓶中发生的有机化学反应方程式为____。
(2)D试管内出现的现象为______;E试管内出现的现象为______。
(3)待三口烧瓶中仍有气泡冒出时打开F夹,关闭C夹,可看到的现象是__________。
(4)从溴苯中除去溴,用NaOH溶液处理后再洗涤,反应的离子方程式为_________。
(5)乙苯的甲基氢原子可以在光照条件下和Cl2发生取代反应,试写出该单取代产物发生消去反应的化学方程式_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com