
��11�֣����淴Ӧ ����һ�������´ﵽƽ�⣬���� �����������仯���������������С���������䡱������ո�
����һ�������´ﵽƽ�⣬���� �����������仯���������������С���������䡱������ո�
��1�������¶ȣ�Bת����___________��v������ ___________��v���棩___________��
��2��ʹ�ô�����A�����ʵ���___________����v������������v���棩____________��
��3�������¶Ⱥ�ѹǿ�������ϡ�����壬��C�����ʵ���___________��A��ת����___________��
��4�������¶Ⱥ�����������ϡ�����壬��A��ת����___________��v������_____________��
��5�����¶Ⱥ�������䣬��Ӧ������Ӧ��ʼ��ƽ�⣬������仯�����У�������������ܶ�___________��ѹǿ___________��
18����1����С����������2�����䣻��С��3����С����С��4�����䣻���䣨5�����䣻��С
��������
�����������1������Ӧ�Ƿ��ȷ�Ӧ�����������¶ȣ����淴Ӧ���ʶ�����ƽ�����淴Ӧ������У�B��ת���ʽ��͡���2��ʹ�ô�����ֻ�ܼӿ컯ѧ��Ӧ���ʣ����ܸı�ƽ�⣬��A�����ʵ������䣬v���棩��С����3�������¶Ⱥ�ѹǿ���䣬����������壬�������ݻ���������ƽ���淴Ӧ������У�C�����ʵ�����A��ת���ʶ��Ǽ�С�ġ���4�������¶Ⱥ�������䣬����������壬���ʵ�Ũ�Ȳ��䣬ƽ�ⲻ�ƶ���A��ת���ʲ��䣬v���������䣻��5���ܶ��ǻ�����������������ݻ��ı�ֵ���ڷ�Ӧ�������������ݻ�ʼ���Dz���ģ�����������������ܶȲ��䣬��ѹǿ�Ǽ�С�ġ�
���㣺���黯ѧƽ��״̬���ƶ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ�������̳�ʵ��ѧУ��һ10��ѧ����п��Ի�ѧ���������棩 ���ͣ�ѡ����
��ѧʵ����ƺͲ�����ʮ������ʦ����ȫ����ͻ����������⡣���в�����������ȷ����( )
A��������ʱ��ˮ���ռ���������ֵ������������ɿ��Թ��ϵ���Ƥ��
B�������巢��װ����ֱ�ӵ�ȼ��Ȳ����ʱ�������ȼ�����Ȳ����Ĵ���
C��ʵ����������еķ�Һ������ˮ���ų�ʵ���ң�������Ⱦʵ����
D�����Թ��е�Һ�����ʱ��ͣ�ƶ��Թܻ�������Ƭ�����Ⱪ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ĸ�һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�����������9��5g�������5��6������״���£����������Ħ��������
A��38 B��38g��mol-1 C��19 D��19g��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ĸ�һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
һ�����SO42-���Լ���
A��BaCl2 ��ϡHNO3 B��AgNO3 ��ϡHNO3 C�� ϡHCl BaCl2 D��AgNO3 ϡHCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������к�ƽ���߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
��11�֣���1��ij���º����������µĿ��淴Ӧ��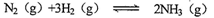 ��H<O����ʼ����amol N2 ��bmol H2���ﵽƽ���N2��H2��NH3�����ʵ����ֱ�Ϊ1 mol��3 mol��10 moL,�ش��������⣺
��H<O����ʼ����amol N2 ��bmol H2���ﵽƽ���N2��H2��NH3�����ʵ����ֱ�Ϊ1 mol��3 mol��10 moL,�ش��������⣺
��a=___________��b=___________��
��ƽ����ٳ���5 mol NH3����ѧƽ�⽫��__________�ƶ�������ҡ����ƶ��������ٴ���ƽ��ʱN2�İٷֺ���_______���>������<������=����ԭƽ��ʱN2�İٷֺ�����
��ƽ����������¶ȣ���ƽ����________����������ҡ��������ƶ���������ѹǿ����ƽ����________����������ҡ��������ƶ���
��2��ij���º�ѹ�����µĿ��淴Ӧ��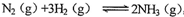 ����ʼ����1 mol N2��
����ʼ����1 mol N2��
3 molH2 ��16 mol NH3���������ݻ�ΪVL���ﵽƽ���N2��H2��NH3�����ʵ����ֱ�Ϊamol��b mol��cmol����ʱ�������ݻ�Ϊ��1VL���ش��������⣺
����ʼʱ��Ӧ����v������____���>������<������=����v���棩��
��ƽ��ʱa=________��b=_______��
����ƽ����ٳ���3��6 mol NH3�����½���ƽ��ʱ�������ݻ�Ϊ_____________L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������к�ƽ���߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��Ӧ��������ϵ�������仯��ͼ��ʾ������˵���������

A����Ӧ���̿ɱ�ʾΪ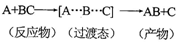
B��E1Ϊ��Ӧ���ƽ�����������̬���������Ϊ����Ӧ�Ļ��
C������Ӧ����ЧӦΪ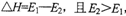 ����������ӦΪ���ȷ�Ӧ
����������ӦΪ���ȷ�Ӧ
D����ͼ���淴Ӧ����ЧӦ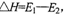 ��Ϊ���ȷ�Ӧ
��Ϊ���ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������к�ƽ���߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��101 kPa��25��ʱ���з�Ӧ���Ȼ�ѧ����ʽ��
H2(g) + 1/2O2(g) =H2O(g) ��H=-241.8kJ/mol��
H2(g) + 1/2O2(g) =H2O(1) ��H=-285.8kJ/mol����˵���д������
A��H2ȼ������1mol H2O (g)ʱ���ų�241��8 kJ������
B��H2��ȼ����Ϊ-285��8 kJ
C��O2ǰ���1/2��ʾ�μӷ�Ӧ��O2�����ʵ���
D��1 molҺ̬ˮ���ˮ����ʱ����44 kJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������к�ƽ����һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����������������п����������Һ�ֱ����������Ȼ�����Һ��Ӧ�������ɵ����ᱵ������������Ϊ1:2:3����������������Һ��SO42�������ʵ���Ũ�ȱ�Ϊ
A��1:2:3 B��1:6:9 c��1:3:3 D��1:3:6
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com