
【题目】对可逆反应N2(g)+3H2(g)2NH3(g)△H<0,下列图象正确的是( )
A.
B.
C.
D.
【答案】C
【解析】解:A、压强增大反应速率增大,先到达平衡,故压强P2>P1,增大压强平衡向气体体积减小的方向移动进行,氨气的体积分数增大,图象与实际不相符,故A错误;
B、升高温度平衡向逆反应方向移动,氮气的转化率降低,图象中温度越高氮气的转化率越大,与实际不相符,故B错误;
C、增大氮气的浓度,瞬间正反应速率增大,逆反应速率不变,平衡向正反应方向移动,图象与实际相符合,故C正确;
D、催化剂同等程度增大反应速率,不改变化学平衡,缩短到达平衡的时间,图象中没有使用催化剂到达平衡的时间短,与实际不符,故D错误,
故选C.
A、压强增大反应速率增大,平衡向气体体积减小的方向移动,氨气的体积分数增大;
B、升高温度平衡向逆反应方向移动,氮气的转化率降低;
C、增大氮气的浓度,瞬间正反应速率增大,逆反应速率不变,平衡向正反应方向移动;
D、催化剂同等程度增大反应速率,不改变化学平衡,缩短到达平衡的时间.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂.请填空.
(1)如图1是常见仪器的部分结构.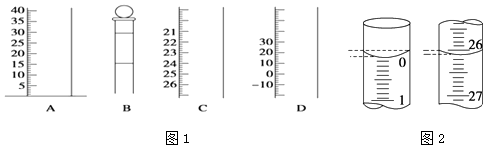
①写出仪器名称BC
②使用前需检查是否漏水的仪器有 .
(2)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视 . 滴定终点时,锥形瓶中颜色变化为 , 且半分钟内颜色不复原.
(3)下列操作中可能使所测NaOH溶液的浓度数值偏低的是
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(4)若滴定开始和结束时,酸式滴定管中的液面如图2所示,所用盐酸溶液的体积为mL.
(5)某学生根据3次实验分别记录有关数据如表:
滴定 | 待测NaOH溶液的体积/mL | 0.100 0mol/L盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 25.11 | 25.11 |
第二次 | 25.00 | 0.56 | 30.56 | 30.00 |
第三次 | 25.00 | 0.22 | 25.11 | 24.89 |
依据表数据列式计算该NaOH溶液的物质的量浓度 . (保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取Na2CO3和 NaOH 的混合液 100ml,先向其中滴加 Ba(OH)2溶液至不产生沉淀为止,再向其中滴加稀盐酸至沉淀消失,产生的沉淀的质量与消耗盐酸的体积如图所示:

(1)原混合液中 Na2CO3的物质的量______mol;
(2)原混合液中 Na2CO3与 NaOH 的物质的量浓度比为______;
(3)稀盐酸的物质的量浓度为______molL-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,设pH=5的H2SO4溶液中由水电离出的H+浓度为c1;pH=5的Al2(SO4)3溶液中由水电离出的H+浓度为c2 , 则C1/C2= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]X、Y、Z、W、R五种短周期非金属元素原子序数依次增大,X、Y、Z、W为同周期元素且未成对电子数之比为1:2:3:2,R和Z同主族。请回答下列问题:
(1)Z的基态原子的价层电子排布图为______________________________。
(2)Z、W、R 三种元素的电负性由大到小的顺序为_____________(用元素符号表示)。
(3)W的常见氢化物的氢键的键能小于HF氢键的键能,但W的常见氢化物常温下为液态而HF常温下为气态的原因是_______________________________。
(4)某种分子式为Y4Z4W8的物质(该物质中同种原子的化学环境完全相同,不含碳碳双键)是一种威力极强的炸药,则可推知其结构简式为_________________________。
(5)XR是一种耐磨材料,可由X的三溴化物和R的三溴化物于高温下在氧气的氛围中合成。
①X的三溴化物分子中X原子的杂化方式为_______________,R的三溴化物分子的空间构型的名称为_____________________。
②合成XR的化学方程式为_____________________。
(6)Y与W形成的某种常见化合物的晶胞如图, 该晶体中分子的配位数为__________________,若晶胞的棱长为a nm,阿伏加德罗常数的值为NA,晶体的密度为______g/cm3。
该晶体中分子的配位数为__________________,若晶胞的棱长为a nm,阿伏加德罗常数的值为NA,晶体的密度为______g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸亚铬,通常以二水盐[Cr(CH3COO)2]2·2H2O的形式存在,是深红色晶体,潮湿时易被氧化。不溶于冷水,微溶于乙醇。醋酸亚铬的一种实验室制备装置和实验步骤如下:

易被氧化。不W 于冷水,微游于乙M。
①连接装置,检查装置气密性,加入药品
②__________________________,A中反应液变浅蓝色后,停止滴入盐酸,向C中通入N2
③打开a,关闭b,保持通入N2,再次滴入盐酸
④待C中有大量红色晶体析出,停止滴入盐酸
⑤取C中物质,抽滤,依次用水、乙醇洗涤沉淀,干燥,称重
回答下列问题:
(1)装置A的名称为_______________,导管c的作用是________________________。
(2)补充步骤②中的实验操作__________________________________。
(3)步骤②中Zn与K2Cr2O7反应的离子方程式为____________________________________。
(4)步骤③中出现的现象是______________________,保持通入N2的目的是______________________。
(5)洗涤时依次用水、乙醇,目的依次为___________________________________。
(6)铬离子会污染水,常温下处理上述实验中多余Cr2+时,可向溶液中通入足量的___________(填物质名称或化学式)再加入碱调节pH为6,此时溶液中残留的Cr3+浓度为__________mol/L。已知:Ksp[Cr(OH)3] =6.3×10-31
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语或物质的性质描述正确的是( )
A. 如图的键线式表示烃的名称为3-甲基-4-乙基-7-甲基辛烷

B. 符合分子式为C4H10O的醇有5种不同的结构
C. 乙烯在一定条件下能发生加成反应、加聚反应,被酸性高锰酸钾溶液氧化,也能在一定条件下生成环氧乙烷
D. 治疗疟疾的青蒿素的结构简式如图,分子式是C15H20O5

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学探究学习小组拟利用如图所示装置(部分固定装置已略去)测定某黑色铜硫化物样品的化学式,按照如下步骤进行了实验。

步骤一:利用右图所示装置,高温灼烧1.6gCuxSy至固体质量不再变化,得到红色固体和一种能使品红 溶液褪色的气体。
步骤二:将D中所得溶液按下述流程进行处理。
煮沸D中溶液并冷却→配制250mL溶液→取25.00mL溶液,滴入2-3滴酚酞溶液→滴定,消耗0.1 molL-1NaOH溶液20.00mL。
请回答下列问题:
(1)A装置中发生反应的化学方程式为_______________________。停止加热后还需继续通入一段时间的O2,其目的是________________________。
(2)仪器a的作用为________________。装置D中反应的化学方程式为__________________________。
(3)步骤二中配制溶液时所需的玻璃仪器除玻璃棒和烧杯外,还有___________;判断滴定终点的现象是____________________________。
(4)利用题中提供的数据可计算得出该铜硫化物的化学式为_______________。
(5)有同学认为可将装置D改为装有足量碱石灰的干燥管,通过测定反应前后干燥管的增重来计算硫元素的含量。你认为此方案(填“合理”或“不合理”),原因是____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com