
【题目】25°C时,某化学实验小组同学向用大理石和稀盐酸制备CO2后的残留液中滴加碳酸钠溶液,在溶液中插入pH传感器,测得pH变化曲线如图所示。下列说法不正确的是( )

A.开始时溶液pH=2是因为残留液中还有盐酸剩余
B.BC段表示随着碳酸钠溶液的滴入,CaCO3沉淀的质量逐渐增加
C.滴入500滴碳酸钠溶液后溶液中c(OH-)>c(H+)
D.AB发生的反应为:Ca2+ + CO32-== CaCO3↓
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是( )
A.元素Y、Z、W形成的离子具有相同电子层结构,其离子半径依次增大
B.39 g Z2Y2中含有的离子数约为1.204×1024
C.元素Z、R的氧化物的水化物之间相互反应生成的盐一定是正盐
D.元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验。实验装置如图所示:(固定装置已略去)

(1)A中反应的化学方程式为 。
(2)F烧杯中的溶液通常是 。
(3)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是 。
(4)实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是 。
(5)为说明浓硫酸中的水是否影响B装置现象的判断,还须进行一次实验。实验方案为 。
(6)将57.6g的Cu片加入50mL 18 mol/L的H2SO4溶液中并加热,被还原的H2SO4的物质的量为_________
A.小于0.45 mol
B.等于0.45 mol
C.在0.45 mol和0.90 mol之间
D.等于0.90 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在密闭容器中发生反应:
2SO2(g)+O2(g)![]() 2SO3(g) △H =-196 kJ/mol
2SO3(g) △H =-196 kJ/mol
请填空:(填>、=、<;增大、减小、不变)
(1)当容器体积不变,①向容器中充入1mol SO2和0.5mol O2,②向容器中充入1mol SO3。两种情况下反应分别达到平衡后,放出和吸收的热量分别为Q1和Q2,则Q1+Q2____________98KJ。
①中达到平衡后,再向容器中加入1mol SO2和0.5mol O2,重新达到平衡,O2体积分数___________。
②中达到平衡后分离出部分SO3,重新平衡后,SO3的浓度________。
(2)保持压强不变,①向容器中充入1mol SO2和0.5mol O2,②向容器中充入1mol SO3,反应达到平衡时,SO2和O2的转化率前者________后者;再向容器中充入1mol SO2和0.5mol O2,重新达到平衡后,SO2的浓度________、O2物质的量_________原平衡的2倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量浓度相同的下列各溶液,由水电离出的c(OH-)由大到小的顺序正确的是
①NaHCO3 ②NaHSO4 ③Na2SO4 ④Na2CO3
A. ①②③④ B. ④③①② C. ④①③② D. ①④③②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为2 L的密闭容器中,有反应:mA(g)+nB(g)![]() pC(g)+qD(g),经过5分钟达到平衡,此时,各物质的变化为:A减少了1 mol·L-1, B的平均反应速率vB=1/15 mol·(L·min)-1,C增加了2/3 mol·L-1,这时,若增加系统压强,发现A与C的百分含量不变,则m∶n∶p∶q为( )
pC(g)+qD(g),经过5分钟达到平衡,此时,各物质的变化为:A减少了1 mol·L-1, B的平均反应速率vB=1/15 mol·(L·min)-1,C增加了2/3 mol·L-1,这时,若增加系统压强,发现A与C的百分含量不变,则m∶n∶p∶q为( )
A.3∶1∶2∶2
B.1∶3∶2∶2
C.1∶3∶2∶1
D.1∶1∶1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20 mL pH=14的溶液,然后用1 mol·L-1的盐酸滴定,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法不正确的是 ( )
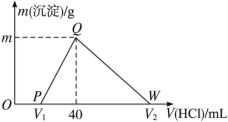
A.原合金质量为0.92 g B.图中V2为100
C.沉淀的质量m为1.56 g D.OP段发生的反应为:OH-+H+=== H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学反应的△H=-122kJmol-1,△S=+231Jmol-1K-1,则此反应在下列哪种情况下可自发进行( )
A. 在任何温度下都能自发进行 B. 在任何温度下都不能自发进行
C. 仅在高温下自发进行 D. 仅在低温下自发进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com