
分析 (1)Ba(OH)2溶液与过量NaHCO3溶液反应生成碳酸钡、碳酸钠和水;
(2)NaHSO4溶液和NaHCO3溶液反应生成二氧化碳、水;
(3)根据NaHSO4与NaHCO3这两种物质的物质量的浓度相同时,最后的溶液中必有硫酸根离子,不可能只剩下氢氧化钠;
根据NaHSO4与NaHCO3这两种物质的物质量的浓度相同时,最后的溶液中必有硫酸根离子,不可能只剩下氢氧化钠;
(4)有两种可能,第一种可能是c[Ba(OH)2]=c(NaHSO4)=2c(NaHCO3);第二种可能是c[Ba(OH)2]=c(NaHCO3)=2c(NaHSO4)分别进行计算.
解答 解:(1)Ba(OH)2溶液与过量NaHCO3溶液反应生成碳酸钡、碳酸钠和水,离子方程式为Ba2++2OH-+2HCO3-=BaCO3↓+2H2O+CO32-,故答案为:Ba2++2OH-+2HCO3-=BaCO3↓+2H2O+CO32-;
(2)NaHSO4溶液和NaHCO3溶液反应生成二氧化碳、水,离子方程式为H++HCO3-=H2O+CO2↑,故答案为:H++HCO3-=H2O+CO2↑;
(3)NaHSO4与NaHCO3这两种物质的物质量的浓度相同时混合发生反应:2NaHSO4+2NaHCO3=Na2SO4+Na2CO3,Na2SO4、Na2CO3的物质的量与Ba(OH)2的物质的量相等,最后的溶液中必有硫酸根离子,不可能只剩下氢氧化钠,
故答案为:NaHSO4、NaHCO3;
(4)第一种可能,设c[Ba(OH)2]=c(NaHSO4)=2c(NaHCO3)=x;
2NaHSO4 +2NaHCO3=2Na2SO4 +2H2O+2CO2↑
0.1x 0.05x 0.05x
Na2SO4 +Ba(OH)2 =BaSO4↓+2NaOH
0.05x 0.05x 0.1x
NaHSO4 +Ba(OH)2 =BaSO4↓+NaOH+2H2O
0.05x 0.05x 0.05x
与Ba(OH)2 恰好反应生成BaSO4和NaOH,则有$\frac{0.15xmol}{0.3L}$=0.9mol•L-1,解得x=1.8mol•L-1,所以 c[Ba(OH)2]=c(NaHSO4)=1.8mol/L,c(NaHCO3)=0.9mol/L,
第二种可能,设c[Ba(OH)2]=c(NaHCO3)=2c(NaHSO4)=x;
2NaHSO4 +2NaHCO3=2Na2SO4 +2H2O+2CO2↑
0.05x 0.1x 0.05x
Na2SO4 +Ba(OH)2 =BaSO4↓+2NaOH
0.05x 0.05x 0.1x
NaHCO3 +Ba(OH)2 =BaCO3↓+NaOH+2H2O
0.05x 0.05x 0.05x
与Ba(OH)2 恰好反应生成BaSO4、BaCO3和NaOH,则有$\frac{0.15xmol}{0.3L}$=0.9mol•L-1,解得x=1.8mol•L-1,所以c[Ba(OH)2]=c(NaHCO3)=1.8mol/L,c(NaHSO4)=0.9mol/L.
故答案为:0.9 mol•L-1或1.8mol•L-1 .
点评 本题考查离子方程式的书写及离子方程式有关计算,为高频考点,明确反应实质及各个物理量关系是解本题关键,注意(4)题计算,题目难度中等.


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ①③ | C. | ①⑤ | D. | ③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 小苏打---NaHCO3 | B. | 明矾---Al2(SO4)3•12H2O | ||
| C. | 铁红---Fe3O4 | D. | 芒硝---Na2SO4•10H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li、Be、B原子最外层电子数依次增多 | |
| B. | P、S、Cl元素最高正化合价依次升高 | |
| C. | N、P、F原子半径依次增大 | |
| D. | Na、K、Rb的金属性依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
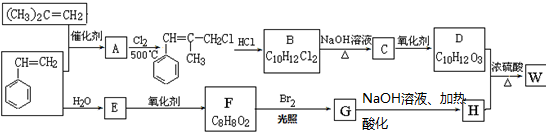 ,
,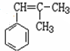 ; F的结构简式为
; F的结构简式为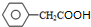 ;
;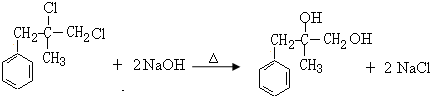 ;D+H→W的化学方程式为
;D+H→W的化学方程式为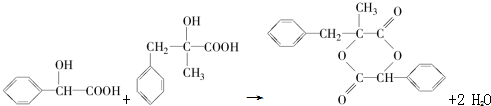 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,1molCH4分子中含有8NA个电子 | |
| B. | 常温常压下,11.2LO3中含有0.5NA个O3分子 | |
| C. | 0.1mol/LNa2SO4溶液中含Na+的数目为0.2NA | |
| D. | Na2O2与水反应产生1molO2时,转移2NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 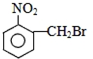 | B. | 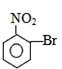 | C. | 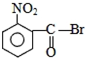 | D. | 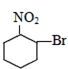 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 焦糖烯能使溴水褪色 | |
| B. | “半成品碳”是碳元素的一种新单质 | |
| C. | 蔗糖溶液与新制的氢氧化铜悬浊液混合加热有砖红色沉淀生成 | |
| D. | 焦糖烯是一种新型的烯经 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 开发新能源,如太阳能、风能等,减少对化石能源的依赖,也减少对大气的污染 | |
| B. | 直径接近于2.5×10-6m的颗粒物(PM2.5)分散在空气中形成的混合物具有丁达尔效应 | |
| C. | 实施“煤改气”、“煤改电”等清洁燃料改造工程,有利于保护环境 | |
| D. | 汽油发动机工作时会产生一定量的NO和CO,采用三元催化装置可以减少污染物的排放 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com