
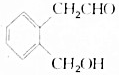
 .A可以被新制Cu(OH)2氧化为B;B能在浓硫酸存在和加热时发生分子内的酯化反应生成C,C分子中有一个含氧的六元环.回答下列问题:
.A可以被新制Cu(OH)2氧化为B;B能在浓硫酸存在和加热时发生分子内的酯化反应生成C,C分子中有一个含氧的六元环.回答下列问题: .
. +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$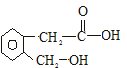 +Cu2O↓+2H2O.
+Cu2O↓+2H2O.分析 根据题意, 可以被新制Cu(OH)2氧化得B为
可以被新制Cu(OH)2氧化得B为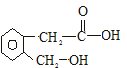 ;B能在浓硫酸存在和加热时发生分子内的酯化反应生成C,C分子中有一个含氧的六元环,所以C为
;B能在浓硫酸存在和加热时发生分子内的酯化反应生成C,C分子中有一个含氧的六元环,所以C为 ,据此答题.
,据此答题.
解答 解:根据题意, 可以被新制Cu(OH)2氧化得B为
可以被新制Cu(OH)2氧化得B为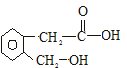 ;B能在浓硫酸存在和加热时发生分子内的酯化反应生成C,C分子中有一个含氧的六元环,所以C为
;B能在浓硫酸存在和加热时发生分子内的酯化反应生成C,C分子中有一个含氧的六元环,所以C为 ,
,
(1)A的结构简式为 ,
,
A.在一定条件下,A中的苯环与醛基都能与氢气加成,所以1molA最多可以和4molH2发生加成反应,故A正确;
B.A中没有酚羟基,所以A不能使FeCl3溶液显紫色,A中羟基邻位碳上没有氢原子,所以也不能发生消去反应,故B正确;
C.根据苯环上所有原子都可以共面,单键可以旋转可知,A分子中所有碳原子可能共平面,故C正确;
D.A中只有醛基和羟基,不能发生缩聚反应形成高分子化合物,故D错误;
故选D;
(2)根据上面的分析可知,C的结构简式为 ,
,
故答案为: ;
;
(3) 与新制Cu(OH)2反应的化学方程式为
与新制Cu(OH)2反应的化学方程式为 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$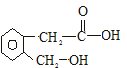 +Cu2O↓+2H2O,
+Cu2O↓+2H2O,
故答案为: +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$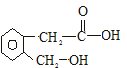 +Cu2O↓+2H2O;
+Cu2O↓+2H2O;
(4)根据条件①含有苯环,且苯环上有两个取代基团;②可发生水解反应,则说明有酯基;③苯环上有两种不同化学环境的氢原子,说明苯环有两个处于对位的基团或三个分布对称的基团,所以符合条件的A的同分异构体的结构为苯环对位上连有-OOCH、-CH2CH3,或-OOCCH3、-CH3,或-CH2OOCH、-CH3,或-COOCH3、-CH3,或为苯环上连有三个处于间位的基团-OOCH、-CH3、-CH3,所以共有5种,
故答案为:5.
点评 本题考查有机物的结构和性质,题目难度中等,本题注意有条件的同分异构体的书写方法,这是易错点.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯元素的相对原子质量为$\frac{12b}{a}$ | |
| B. | mg该氯原子的物质的量一定是$\frac{m}{(a{N}_{A})}$mol | |
| C. | 该氯元素的摩尔质量是aNA | |
| D. | ng该氯原子所含的电子数为$\frac{n}{a}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol 对苯二甲酸中含有双键的数目为0.2NA | |
| B. | 标准状况下,11.2 L甲醛所含的σ键数目为2NA | |
| C. | 2mol NO和1mol O2混合,在密闭容器中充分反应后,容器内的分子数等于2NA | |
| D. | 1mol Fe 与足量的硝酸反应,转移的电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
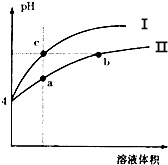
| A. | Ⅰ为氯化铵溶液稀释时pH值变化曲线 | |
| B. | b点比c点溶液的导电能力强 | |
| C. | a点溶液中c(H+)+c(NH3•H2O)=c(OH-) | |
| D. | b点比a点溶液中的水的电离程度大,但两点的KW相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 (g)△H=-106kJ•mol-1
(g)△H=-106kJ•mol-1 +AgO 快
+AgO 快| A. | 反应的活化能等于106kJ•mol-1 | |
| B. | AgO2也是反应的催化剂 | |
| C. | 增大乙烯浓度能显著提高环氧乙烷的生成速率 | |
| D. | 理论上0.7mol乙烯参与反应最多可得到0.6mol环氧乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 将镁、铝的混合物共0.2mol,溶于200mL4mol•L-1的盐酸溶液中,然后再滴加2mol•L-1的NaOH溶液.请回答下列问题:,
将镁、铝的混合物共0.2mol,溶于200mL4mol•L-1的盐酸溶液中,然后再滴加2mol•L-1的NaOH溶液.请回答下列问题:,查看答案和解析>>
科目:高中化学 来源: 题型:解答题

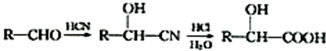
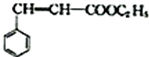
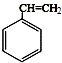 ;C 的化学名称为苯乙醛.
;C 的化学名称为苯乙醛.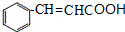 +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$ +H2O.
+H2O.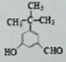
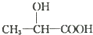 )的路线(其他试剂任选)
)的路线(其他试剂任选)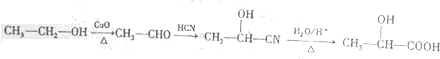 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com