

���� ��1�������Na2[Fe��CN��5��NO��]����������Ϊ�����ӣ����ݺ�������Ų�������д��
��2��������д������������������ӵ����Ӽ�������֮��ļ��Թ��ۼ��������Ӻ���֮�����λ����
��3����ʯīϩ��̼ԭ����Χ���������ۼ����ݴ��ж�̼ԭ�ӵ��ӻ���ʽ��
�ڸ����������ʵ��ӻ����ͷ������ۼ����ͣ�
�۸��ݾ�̯�����㾧����Mԭ����Ŀ��C60����������ȷ����ѧʽ��
��4��������е縺������Ԫ�غ͵�������С��Ԫ���γɵ�һ�����ӻ�����Ϊ�����ƣ����ݾ�����Na2O���ṹ��֪����������Ĵ��������ӣ�������ȫ���ھ����ڣ��������������������������4��������λ����4������һ����������Χ���������������Ϊ���㹹�ɵļ������������壮�þ����к���4�������ӣ�
��5���ס��Ҷ��ܺͱ��γ�ԭ�Ӹ�����Ϊ1��3�ij������ֱ���CO32-��NO3-������ԭ�Ӻ��Ҽ����Ӷ���Ϊ3�ԣ�
��� �⣺��1����ԭ��ʧȥ�����4s�ܼ�2�����ӣ�Ȼ��ʧȥ3d�ܼ��ϵ�1�������γ�Fe3+����������Ų�ʽΪ��1s22s22p63s23p63d5��[Ar]3d5��
�ʴ�Ϊ��1s22s22p63s23p63d5��[Ar]3d5��
��2��A��Na+��[Fe��CN��5��NO��]2-֮��������Ӽ�����A��ѡ��
B�������Na2[Fe��CN��5��NO��]�в����ڽ������ʣ�����������Bѡ��
C��N��O��FԪ�صĵ縺�Խ�ǿ����Ӧ���⻯����⻯������γ�����������Na2[Fe��CN��5��NO��]�в������������Cѡ��
D��̼��ԭ�Ӽ��γɼ��Թ��ۼ�����D��ѡ��
E��NO���ӡ�CN-��Fe3+�γ���λ������E��ѡ��
�ʴ�Ϊ��BC��
��3����ʯīϩ��̼ԭ����Χ���������ۼ���̼ԭ�ӵ��ӻ���ʽΪsp2��
�ʴ�Ϊ��sp2�ӻ���
�ڽ��ʯ��̼ԭ����sp3�ӻ����γ������ӻ������ȫ���γɦҼ���ʯī��̼ԭ����sp2�ӻ����γ������ӻ����������һ��Ϊ�ӻ���p����������ӻ�����γɦҼ�����δ�ӻ�p����γɦм�������ʯī��C-C���ļ����̣�
�ʴ�Ϊ��Cԭ��֮���γ��˴�м���
�۾����У�Mԭ�Ӹ���=8+12��$\frac{1}{4}$+1=12��C60����=8��$\frac{1}{8}$+6��$\frac{1}{2}$=4����C60��Mԭ�Ӹ���֮��=4��12=1��3���仯ѧʽΪ M3C60��
�ʴ�Ϊ��M3C60��
��4��������е縺������Ԫ�غ͵�������С��Ԫ���γɵ�һ�����ӻ�����Ϊ�����ƣ����ݾ�����Na2O���ṹ��֪N��Na+����N��O2-��=2��1�����Զ�������Ĵ��������ӣ�����ɫ��ΪO2-��������ȫ���ھ����ڣ�����ɫ��ΪNa+���ӣ��������������������������4��������λ����4������һ����������Χ���������������Ϊ���㹹�ɵļ������������壨�����壩���þ����к���4�������ӣ�������$\frac{{a}^{3}���ѡ�{N}_{A}}{62}$=4�����a=$\root{3}{\frac{248}{��{N}_{A}}}$��
�ʴ�Ϊ�������壨�����壩��$\root{3}{\frac{248}{��{N}_{A}}}$��
��5���ס��Ҷ��ܺͱ��γ�ԭ�Ӹ�����Ϊ1��3�ij������ֱ���CO32-��NO3-������ԭ�Ӻ��Ҽ����Ӷ���Ϊ3�ԣ�CO32-���еĵ��Ӷ���=3+$\frac{4+2-2��3}{2}$=3��NO3-���еĵ��Ӷ���=$\frac{5+1-2��3}{2}$=3�����Զ���ƽ�������νṹ��
�ʴ�Ϊ��ƽ�������Σ�
���� �����Ƕ����ʽṹ�����ʵĿ��飬�漰��������Ų�����ѧ�����ӻ�����������ṹ����㣬�����ṹ��ѧ���Ŀռ�������һ����Ҫ��ע�����þ�̯�����м��㣬��Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
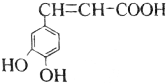
| A�� | ��÷����廯�������ʽ��ͬ�����������༰��Ŀ����ͬ�ұ����ϵ�һ�ȴ���ֻ�����ֵ��л���Ľṹ��4�֣������ǿռ��칹�� | |
| B�� | ������ֻ�ܼӾ۳ɸ߷��ӻ����� | |
| C�� | ������������5mol���������ӳɷ�Ӧ | |
| D�� | 1mol��������������Na2CO3��Һ��Ӧ��������3molCO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2ͨ�뵽 CaCl2��Һ�� | |
| B�� | NH3ͨ�� AlCl3��Һ�� | |
| C�� | ����֬�ް���Na2O2��ĩ������ͨ������������̼ | |
| D�� | ϡ����μӵ�Fe��OH��3������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | X��Y����γ����ӻ����� | |
| B�� | �����۵㣺Y��W��X | |
| C�� | ����������Ӧˮ��������ԣ�Z��W | |
| D�� | Y��W�γɵĵ������Ӿ����ƻ�ˮ�ĵ���ƽ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɫ�ļ�����Һ�У�CrO42-��K+��Na+��SO42- | |
| B�� | ���д���ClO-����Һ�У�K+��H+��I-��SO42 | |
| C�� | -ʹpH��ֽ������Һ�У�NH4+��Na+��SO42-��Cl- | |
| D�� | ˮ���������c��H+��=10-12mol•L-1����Һ�У�Na+��Fe2+��SO42-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C20H30O2��C22H30O2 | B�� | C22H32O2��C20H30O2 | ||
| C�� | C22H30O2��C20H30O2 | D�� | C20H30O2��C22H32O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
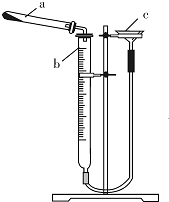 ��ʽ̼��ͭ��һ�־��й㷺��;�Ļ�����Ʒ����Ҫ���ڹ���ӫ��ۼ������ͭ�ε�����ȣ�
��ʽ̼��ͭ��һ�־��й㷺��;�Ļ�����Ʒ����Ҫ���ڹ���ӫ��ۼ������ͭ�ε�����ȣ�| ʵ����� | ��Ʒ����/g | CO2���/mL��������ɱ�״���£� |
| 1 | 0.542 | 44.82 |
| 2 | 0.542 | 44.80 |
| 3 | 0.542 | 44.78 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
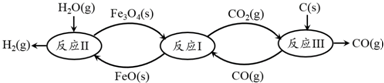
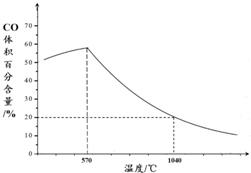

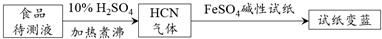
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ��Ӧʱ��/min | n��MgSO4��/mol | n��CO��/mol | n��CO2��/mol |
| 0 | 2.00 | 2.00 | 0 |
| 2 | 0.80 | ||
| 4 | 1.20 |
| A�� | ��Ӧ��0��2 min�ڵ�ƽ������Ϊv��SO2��=0.6 mol•L-1•min-1 | |
| B�� | ��Ӧ��2��4 min��������������ܶ�û�б仯 | |
| C�� | �������¶ȣ���Ӧ��ƽ�ⳣ����Ϊ1.00��������ӦΪ���ȷ�Ӧ | |
| D�� | ���������������䣬��ʼʱ�������г���1.00 mol MgSO4��1.00 mol CO������ƽ��ʱn��CO2����0.60 mol |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com