
| A. | NaHSO4溶于水:NaHSO4?Na++H++SO42- | |
| B. | 次氯酸电离:HClO═ClO-+H+ | |
| C. | HF溶于水:HF+H2O?H3O++F- | |
| D. | NH4Cl溶于水:NH4++H2O?NH3•H2O+H+ |
分析 A.硫酸氢钠为强电解质,完全电离,用等号;
B.次氯酸为弱电解质,部分电离,用可逆号;
C.氢氟酸为弱电解质,部分电离,在水溶液中电离生成水合氢离子和氟离子;
D.氯化铵为强电解质,完全电离生成氨根离子和氯离子.
解答 解:A.NaHSO4为强电解质溶于水,完全电离,电离方程式:NaHSO4=Na++H++SO42-,故A错误;
B.次氯酸为弱电解质,部分电离,用可逆号:HClO?ClO-+H+,故B错误;
C.氢氟酸为弱电解质,部分电离,电离方程式:HF+H2O?H3O++F-,故C正确;
D.氯化铵电离方程式为:NH4Cl=NH4++Cl-,故D错误;
故选:C.
点评 本题考查了离子方程式的书写,侧重考查盐类的水解和弱电解质的电离,明确电解质的强弱及电离方式是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 钠与硫酸铜溶液反应会置换出红色的铜 | |
| B. | 常温下干燥氯气与铁不反应,可以用钢瓶储存液氯 | |
| C. | CO2、NO2、SO2都能与H2O反应,其反应原理相同 | |
| D. | C、N、S三种单质直接与O2反应都能生成两种氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食品添加剂对人体的健康均无害,所以不用严格控制用量 | |
| B. | 棉、麻、丝、毛的主要成分都是纤维素 | |
| C. | 光纤的主要成分是二氧化硅 | |
| D. | 农业施肥所用的碳铵和尿素均属于无机物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
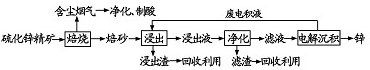
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
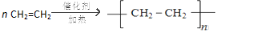 .
.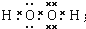 ;将乙加入浅绿色酸性溶液中,溶液变为棕黄色,写出该反应的离子方程式.
;将乙加入浅绿色酸性溶液中,溶液变为棕黄色,写出该反应的离子方程式. .与PH3相比,DC2易液化的主要原因是NH3中有氢键;
.与PH3相比,DC2易液化的主要原因是NH3中有氢键;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com